Cleocin 150mg, 300mg Clindamycin Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä ovat Cleocin 300 mg hydrokloridikapselit?
Cleocin Hydrochloride -kapselit sisältävät antibioottia, joka on tarkoitettu herkkien anaerobisten bakteerien aiheuttamien vakavien infektioiden hoitoon. Cleocin 150mg Hydrochloride on tarkoitettu myös vakavien infektioiden hoitoon, jotka johtuvat herkistä streptokokki-, pneumokokki- ja stafylokokkikannoista. Sen käyttö tulee varata vain penisilliiniallergisille potilaille tai muille potilaille, joille penisilliini ei lääkärin arvion mukaan sovellu. Cleocin Hydrochloride on saatavana yleisessä muodossa.
Mitkä ovat Cleocin 300 mg hydrokloridikapseleiden sivuvaikutukset?
Cleocin Hydrochloridin yleisiä sivuvaikutuksia ovat:
- Clostridium difficile koliitti,
- vatsakipu,
- pseudomembranoottinen koliitti,
- esofagiitti,
- pahoinvointi,
- oksentelua,
- ripuli,
- ihottuma,
- nokkosihottuma,
- vakavat allergiset reaktiot (anafylaksia),
- yliherkkyysreaktiot,
- kutina,
- emättimen vuoto ja epämukavuus,
- ihon turvotus,
- ihon ja silmien keltaisuus (keltaisuus),
- epänormaalit maksan toimintakokeet ja
- nivelkipu.
Lääkeresistenttien bakteerien kehittymisen vähentämiseksi ja CLEOCIN 300 mg HCl:n ja muiden antibakteeristen lääkkeiden tehokkuuden ylläpitämiseksi CLEOCIN 300 mg HCl:a tulee käyttää vain sellaisten infektioiden hoitoon tai ehkäisyyn, joiden on todistettu tai epäillään olevan bakteerien aiheuttamia.
VAROITUS
Clostridium difficileen liittyvää ripulia (CDAD) on raportoitu käytettäessä lähes kaikkia antibakteerisia aineita, mukaan lukien CLEOCIN HCl, ja sen vaikeusaste voi vaihdella lievästä ripulista kuolemaan johtavaan paksusuolentulehdukseen. Hoito antibakteerisilla aineilla muuttaa paksusuolen normaalia kasvistoa, mikä johtaa C. difficlen liikakasvuun.
Koska CLEOCIN 150 mg HCl -hoitoon on liittynyt vakava paksusuolentulehdus, joka voi päättyä kuolemaan, se tulee varata vakaville infektioille, joissa vähemmän myrkylliset mikrobilääkkeet eivät sovellu, kuten KÄYTTÖAIHEET JA KÄYTTÖ osio. Sitä ei tule käyttää potilailla, joilla on ei-bakteeri-infektioita, kuten useimmat ylempien hengitysteiden infektiot.
C. difficle tuottaa toksiineja A ja B, jotka edistävät CDAD:n kehittymistä. Hypertoksiinia tuottavat C. difficle -kannat lisäävät sairastuvuutta ja kuolleisuutta, koska nämä infektiot voivat olla vastustuskykyisiä antimikrobiselle hoidolle ja saattavat vaatia kolektomiaa. CDAD on otettava huomioon kaikilla potilailla, joilla on ripuli antibioottien käytön jälkeen. Huolellinen sairaushistoria on tarpeen, koska CDAD:n on raportoitu esiintyvän yli kaksi kuukautta antibakteeristen aineiden annon jälkeen.
Jos CDAD:ta epäillään tai varmistetaan, jatkuva antibioottien käyttö, joka ei ole suunnattu C. difficileä vastaan, saattaa olla tarpeen lopettaa. Asianmukainen neste- ja elektrolyyttihallinta, proteiinilisä, C. difficilen antibioottihoito ja kirurginen arviointi tulee aloittaa kliinisen aiheen mukaan.
KUVAUS
Klindamysiinihydrokloridi on klindamysiinin hydratoitu hydrokloridisuola. Klindamysiini on puolisynteettinen antibiootti, joka tuotetaan linkomysiinin kantayhdisteen 7(R)-hydroksyyliryhmän 7(S)-kloorisubstituutiolla.
CLEOCIN HCl -kapselit sisältävät klindamysiinihydrokloridia, joka vastaa 75 mg, 150 mg tai 300 mg klindamysiiniä.
Ei-aktiiviset aineet: 75 mg - maissitärkkelys, FD&C sininen no. 1, FD&C keltainen nro. 5, gelatiini, laktoosi, magnesiumstearaatti ja talkki; 150 mg - maissitärkkelys, FD&C sininen no. 1, FD&C keltainen nro. 5, gelatiini, laktoosi, magnesiumstearaatti, talkki ja titaanidioksidi; 300 mg - maissitärkkelys, FD&C sininen no. 1, gelatiini, laktoosi, magnesiumstearaatti, talkki ja titaanidioksidi.
Rakennekaava on esitetty alla:
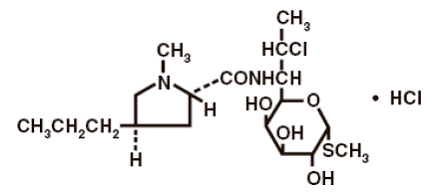
Klindamysiinihydrokloridin kemiallinen nimi on Metyyli-7-kloori-6,7,8-trideoksi-6-(1-metyyli-trans-4-propyyli-L-2-pyrrolidiinikarboksamido)-1-tio-L-treo-a- D-galakto-oktopyranosidimonohydrokloridi.
INDIKAATIOT
Klindamysiini on tarkoitettu herkkien anaerobisten bakteerien aiheuttamien vakavien infektioiden hoitoon.
Klindamysiini on tarkoitettu myös vakavien infektioiden hoitoon, jotka johtuvat herkistä streptokokki-, pneumokokki- ja stafylokokkikannoista. Sen käyttö tulee varata vain penisilliiniallergisille potilaille tai muille potilaille, joille penisilliini ei lääkärin arvion mukaan sovellu. VAROITUKSESSA kuvatun paksusuolentulehduksen riskin vuoksi ennen klindamysiinin valitsemista lääkärin tulee harkita infektion luonnetta ja vähemmän myrkyllisten vaihtoehtojen (esim. erytromysiini) soveltuvuutta.
Anaerobit: Vakavat hengitystieinfektiot, kuten empyeema, anaerobinen keuhkotulehdus ja keuhkoabsessi; vakavat iho- ja pehmytkudosinfektiot; septikemia; vatsansisäiset infektiot, kuten vatsakalvontulehdus ja vatsansisäinen absessi (jotka ovat tyypillisesti seurausta anaerobisista organismeista, jotka asuvat normaalissa ruoansulatuskanavassa); naisen lantion ja sukupuolielinten infektiot, kuten endometriitti, nongonokokki-munasarjan paise, lantion selluliitti ja leikkauksen jälkeinen emättimen mansettitulehdus.
Streptokokit: Vakavat hengitystieinfektiot; vakavat iho- ja pehmytkudosinfektiot.
Stafylokokit: Vakavat hengitystieinfektiot; vakavat iho- ja pehmytkudosinfektiot.
Pneumokokit: Vakavat hengitystieinfektiot.
Bakteriologisia tutkimuksia tulisi suorittaa taudinaiheuttajat ja niiden herkkyys klindamysiinille määrittämiseksi.
Lääkeresistenttien bakteerien kehittymisen vähentämiseksi ja CLEOCIN HCl:n ja muiden antibakteeristen lääkkeiden tehokkuuden säilyttämiseksi CLEOCIN HCl:a tulee käyttää vain sellaisten infektioiden hoitoon tai ehkäisyyn, joiden todistetaan tai epäillään olevan herkkien bakteerien aiheuttamia. Kun viljely- ja herkkyystiedot ovat saatavilla, ne tulee ottaa huomioon valittaessa tai muuttaessa antibakteerista hoitoa. Tällaisten tietojen puuttuessa paikallinen epidemiologia ja herkkyysmallit voivat vaikuttaa hoidon empiiriseen valintaan.
ANNOSTELU JA HALLINNOINTI
Jos merkittävää ripulia ilmenee hoidon aikana, tämän antibiootin käyttö on lopetettava (ks LAATIKKO VAROITUS ).
Aikuiset
Vakavat infektiot - 150-300 mg 6 tunnin välein. Vakavammat infektiot - 300-450 mg 6 tunnin välein.
Lapsipotilaat (lapsille, jotka pystyvät nielemään kapseleita):
Vakavat infektiot 8-16 mg/kg/vrk (4-8 mg/lb/vrk) jaettuna kolmeen tai neljään yhtä suureen annokseen. Vakavammat infektiot - 16-20 mg/kg/vrk (8-10 mg/lb/vrk) jaettuna kolmeen tai neljään yhtä suureen annokseen.
Ruokatorven ärsytyksen välttämiseksi CLEOCIN 300 mg HCl -kapselit tulee ottaa lasillisen vettä kera.
CLEOCIN HCl -kapselit eivät sovellu lapsille, jotka eivät pysty nielemään niitä kokonaisina. Kapselit eivät tarjoa tarkkoja mg/kg-annoksia, joten klindamysiinipalmitaattioraaliliuosta voi olla tarpeen käyttää joissakin tapauksissa.
Vakavat anaerobisten bakteerien aiheuttamat infektiot hoidetaan yleensä CLEOCIN PHOSPHATE® Steriil Solution -liuoksella. Kliinisesti sopivissa olosuhteissa lääkäri voi kuitenkin päättää aloittaa hoidon tai jatkaa hoitoa CLEOCIN 150 mg HCl -kapseleilla.
β-hemolyyttisten streptokokki-infektioiden tapauksessa hoitoa tulee jatkaa vähintään 10 päivää.
MITEN TOIMITETAAN
CLEOCIN HCl -kapselit on saatavana seuraavina vahvuuksina, väreinä ja kokoina:
75 mg Vihreät 100 pullot NDC 0009-0331-02
150 mg Vaaleansiniset ja vihreät 100 pullot NDC 0009-0225-02
300 mg Vaaleansiniset 100 pullot NDC 0009-0395-14
Säilytä kontrolloidussa huoneenlämmössä 20–25 °C (68–77 °F) [katso USP ].
Jakelija: Pharmacia & Upjohn Co, Division of Pfizer Inc, NY, NY 10017. Tarkistettu 2017
SIVUVAIKUTUKSET
Seuraavia reaktioita on raportoitu klindamysiinin käytön yhteydessä.
Infektiot ja infektiot: Clostridium difficile -koliitti
Ruoansulatuskanava: Vatsakipu, pseudomembranoottinen koliitti, esofagiitti, pahoinvointi, oksentelu ja ripuli (ks. LAATIKKO VAROITUS ). Pseudomembranoottisen paksusuolitulehduksen oireet voivat ilmaantua antibakteerisen hoidon aikana tai sen jälkeen (ks VAROITUKSET ). Ruokatorven haavaumia on raportoitu. Epämiellyttävää tai metallista makua on raportoitu oraalisen annon jälkeen.
Yliherkkyysreaktiot: Yleistyneet lievät tai kohtalaiset morbilliformin kaltaiset (makulopapulaariset) ihottumat ovat yleisimmin raportoituja haittavaikutuksia. Vesiculobulloosia ihottumaa sekä urtikariaa on havaittu lääkehoidon aikana. Vakavia ihoreaktioita, kuten toksinen epidermaalinen nekrolyysi, joista osa on johtanut kuolemaan, on raportoitu (ks. VAROITUKSET ). Akuutti yleistynyt eksantematoottinen pustuloos (AGEP), erythema multiforme, joista osa muistuttaa Stevens-Johnsonin oireyhtymää, anafylaktinen sokki, anafylaktinen reaktio ja yliherkkyys, on myös raportoitu.
Iho ja limakalvot: Kutinaa, vaginiittia, angioedeemaa ja harvinaisia exfoliatiivisia ihottumia on raportoitu. (Katso Yliherkkyysreaktiot .)
Maksa: Klindamysiinihoidon aikana on havaittu keltaisuutta ja poikkeavuuksia maksan toimintakokeissa.
Munuaiset: Vaikka klindamysiinin suoraa yhteyttä munuaisvaurioon ei ole osoitettu, munuaisten vajaatoimintaa, josta on osoituksena atsotemia, oliguria ja/tai proteinuria, on havaittu.
Hematopoieettinen: Ohimenevää neutropeniaa (leukopeniaa) ja eosinofiliaa on raportoitu. Agranulosytoosista ja trombosytopeniasta on raportoitu. Mitään suoraa etiologista yhteyttä samanaikaiseen klindamysiinihoitoon ei voitu tehdä millään edellä mainitulla.
Immuunijärjestelmä: Lääkereaktioita, joihin liittyy eosinofiliaa ja systeemisiä oireita (DRESS), on raportoitu.
Tuki- ja liikuntaelimistö: Moniniveltulehdustapauksia on raportoitu.
HUUMEIDEN VUOROVAIKUTUKSET
Klindamysiinillä on osoitettu olevan neuromuskulaarisia salpaavia ominaisuuksia, jotka voivat tehostaa muiden hermo-lihassalpaajien vaikutusta. Siksi sitä tulee käyttää varoen potilailla, jotka saavat tällaisia aineita.
Klindamysiini metaboloituu pääasiassa CYP3A4:n ja vähemmässä määrin CYP3A5:n välityksellä päämetaboliitiksi klindamysiinisulfoksidiksi ja vähäiseksi metaboliitiksi N-desmetyyliklindamysiiniksi. Siksi CYP3A4:n ja CYP3A5:n estäjät voivat suurentaa klindamysiinin pitoisuuksia plasmassa ja näiden isoentsyymien induktorit voivat pienentää klindamysiinin pitoisuuksia plasmassa. Jos läsnä on vahvoja CYP3A4-estäjiä, tarkkaile haittavaikutuksia. Vahvojen CYP3A4-indusoijien, kuten rifampisiinin, läsnä ollessa on seurattava tehon heikkenemistä.
In vitro -tutkimukset osoittavat, että klindamysiini ei estä CYP1A2:ta, CYP2C9:ää, CYP2C19:ää, CYP2E1:tä tai CYP2D6:ta ja vain kohtalaisesti inhiboi CYP3A4:ää.
Klindamysiinin ja erytromysiinin välillä on osoitettu antagonismia in vitro. Mahdollisen kliinisen merkityksen vuoksi näitä kahta lääkettä ei tule antaa samanaikaisesti.
VAROITUKSET
Katso LAATIKKO VAROITUS
Clostridium Difficilen liittyvä ripuli
Clostridium difficileen liittyvää ripulia (CDAD) on raportoitu käytettäessä lähes kaikkia antibakteerisia aineita, mukaan lukien CLEOCIN 300 mg HCl, ja sen vaikeusaste voi vaihdella lievästä ripulista kuolemaan johtavaan paksusuolentulehdukseen. Hoito antibakteerisilla aineilla muuttaa paksusuolen normaalia kasvistoa, mikä johtaa C. difficlen liikakasvuun.
C. difficle tuottaa toksiineja A ja B, jotka edistävät CDAD:n kehittymistä. Hypertoksiinia tuottavat C. difficle -kannat lisäävät sairastuvuutta ja kuolleisuutta, koska nämä infektiot voivat olla vastustuskykyisiä antimikrobiselle hoidolle ja saattavat vaatia kolektomiaa. CDAD on otettava huomioon kaikilla potilailla, joilla on ripuli antibioottien käytön jälkeen. Huolellinen sairaushistoria on tarpeen, koska CDAD:n on raportoitu esiintyvän yli kaksi kuukautta antibakteeristen aineiden annon jälkeen.
Jos CDAD:ta epäillään tai varmistetaan, jatkuva antibioottien käyttö, joka ei ole suunnattu C. difficileä vastaan, saattaa olla tarpeen lopettaa. Asianmukainen neste- ja elektrolyyttihallinta, proteiinilisä, C. difficilen antibioottihoito ja kirurginen arviointi tulee aloittaa kliinisen aiheen mukaan.
Anafylaktiset ja vakavat yliherkkyysreaktiot
Anafylaktisia sokkeja ja anafylaktisia reaktioita on raportoitu (ks HAITTAVAIKUTUKSET ).
Vakavia yliherkkyysreaktioita, mukaan lukien vakavia ihoreaktioita, kuten toksinen epidermaalinen nekrolyysi (TEN), lääkereaktio, johon liittyy eosinofiliaa ja systeemisiä oireita (DRESS), ja Stevens-Johnsonin oireyhtymä (SJS), joista osa on johtanut kuolemaan, on raportoitu (ks. HAITTAVAIKUTUKSET ).
Jos ilmenee tällainen anafylaktinen tai vakava yliherkkyysreaktio, lopeta hoito pysyvästi ja aloita asianmukainen hoito.
Aiempi herkkyys lääkkeille ja muille allergeeneille tulee selvittää huolellisesti.

Käyttö aivokalvontulehduksessa
Koska klindamysiini ei diffundoidu riittävästi aivo-selkäydinnesteeseen, lääkettä ei tule käyttää aivokalvontulehduksen hoidossa.
VAROTOIMENPITEET
Kenraali
Tähän mennessä saatujen kokemusten tarkastelu viittaa siihen, että iäkkäiden potilaiden alaryhmä, johon liittyy vakava sairaus, saattaa sietää ripulia huonommin. Kun klindamysiini on indikoitu näille potilaille, heitä on seurattava huolellisesti suolen tiheyden muutosten varalta.
CLEOCIN 300 mg HCl:ää tulee määrätä varoen henkilöille, joilla on ollut maha-suolikanavan sairaus, erityisesti paksusuolentulehdus.
CLEOCIN 300 mg HCl:ää tulee määrätä varoen atooppisille henkilöille.
Indikoituja kirurgisia toimenpiteitä tulee suorittaa antibioottihoidon yhteydessä.
CLEOCIN 150mg HCl:n käyttö johtaa toisinaan ei-herkkien organismien, erityisesti hiivojen, liikakasvuun. Jos superinfektioita ilmaantuu, kliinisen tilanteen mukaan on ryhdyttävä asianmukaisiin toimenpiteisiin.
Klindamysiinin annoksen muuttaminen ei ehkä ole tarpeen potilailla, joilla on munuaissairaus. Klindamysiinin puoliintumisajan on havaittu pidentyneen potilailla, joilla on kohtalainen tai vaikea maksasairaus. Tutkimusten perusteella kuitenkin oletettiin, että kun sitä annetaan kahdeksan tunnin välein, kertymistä tapahtuu harvoin. Siksi annoksen muuttaminen potilailla, joilla on maksasairaus, ei ehkä ole tarpeen. Maksaentsyymimääritykset on kuitenkin tehtävä säännöllisesti hoidettaessa potilaita, joilla on vaikea maksasairaus.
75 mg ja 150 mg kapselit sisältävät FD&C keltaista nro. 5 (tartratsiini), joka voi aiheuttaa allergisen tyyppisiä reaktioita (mukaan lukien keuhkoastma) tietyillä herkillä henkilöillä. Vaikka yleinen FD&C keltaisen esiintyvyys ei. 5 (tartratsiini) herkkyys yleisväestössä on alhainen, se nähdään usein potilailla, joilla on myös yliherkkyys aspiriinille.
CLEOCIN 150 mg HCl:n määrääminen ilman todistettua tai vahvasti epäiltyä bakteeri-infektiota tai profylaktista indikaatiota ei todennäköisesti hyödytä potilasta ja lisää lääkeresistenttien bakteerien kehittymisen riskiä.
Laboratoriotestit
Pitkäaikaisen hoidon aikana tulee suorittaa määräajoin maksan ja munuaisten toimintakokeita ja verenkuva.
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Klindamysiinillä ei ole tehty pitkäaikaisia eläintutkimuksia karsinogeenisuuden arvioimiseksi. Suoritetut genotoksisuustestit sisälsivät rotan mikrotumatestin ja Ames Salmonella -reversiotestin. Molemmat testit olivat negatiivisia.
Hedelmällisyystutkimukset rotilla, joita hoidettiin suun kautta annoksella 300 mg/kg/vrk (noin 1,6 kertaa suurin suositeltu aikuisen ihmisen annos mg/m2:n perusteella), ei osoittanut vaikutuksia hedelmällisyyteen tai pariutumiskykyyn.
Raskaus
Teratogeeniset vaikutukset
Kliinisissä tutkimuksissa raskaana olevilla naisilla klindamysiinin systeemiseen käyttöön toisen ja kolmannen raskauskolmanneksen aikana ei ole liittynyt synnynnäisten epämuodostumien lisääntymistä.
Klindamysiiniä tulee käyttää raskauden ensimmäisen kolmanneksen aikana vain, jos se on selvästi tarpeen. Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia raskaana olevilla naisilla ensimmäisen raskauskolmanneksen aikana. Koska eläinten lisääntymistutkimukset eivät aina ennusta ihmisen vastetta, tätä lääkettä tulee käyttää raskauden aikana vain, jos se on selvästi tarpeen.
Rotilla ja hiirillä tehdyt lisääntymistutkimukset, joissa käytettiin klindamysiinin oraalisia annoksia enintään 600 mg/kg/vrk (3,2 ja 1,6 kertaa suurin suositeltu aikuisen ihmisen annos, joka perustuu mg/m²:iin) tai klindamysiinin ihonalaisia annoksia enintään 250 mg/kg /vrk (1,3-kertainen ja 0,7 kertaa suurin suositeltu aikuisen ihmisannos mg/m²:n perusteella) ei osoittanut näyttöä teratogeenisuudesta.
Imettävät äidit
Klindamysiinin on raportoitu erittyvän äidinmaitoon välillä 0,7-3,8 mikrog/ml. Klindamysiinillä voi olla haitallisia vaikutuksia imetettävän lapsen ruuansulatuskanavan floraan. Jos imettävä äiti vaatii oraalista tai suonensisäistä klindamysiiniä, se ei ole syy imetyksen lopettamiseen, mutta vaihtoehtoinen lääke voi olla parempi. Tarkkaile vauvaa mahdollisten haitallisten vaikutusten varalta ruoansulatuskanavan kasvistossa, kuten ripulia, kandidiaasia (sammas, vaippaihottuma) tai harvoin verta ulosteessa, mikä viittaa mahdolliseen antibioottihoitoon liittyvään paksusuolentulehdukseen.
Imetyksen kehitys- ja terveyshyötyjä tulee harkita sekä äidin klindamysiinin kliinistä tarvetta ja klindamysiinin tai äidin taustalla olevan sairauden mahdollisia haitallisia vaikutuksia imetettävään lapseen.
Käyttö lapsille
Kun CLEOCIN 300 mg HCl:a annetaan lapsiväestölle (syntyvistä 16-vuotiaisiin), elinjärjestelmän toimintojen asianmukainen seuranta on toivottavaa.
Geriatrinen käyttö
Klindamysiinin kliinisissä tutkimuksissa ei ollut riittävästi 65-vuotiaita ja sitä vanhempia potilaita sen määrittämiseksi, reagoivatko he eri tavalla kuin nuoremmat potilaat. Muut raportoidut kliiniset kokemukset osoittavat kuitenkin, että useimpien antibioottien yhteydessä havaittu antibiootteihin liittyvä paksusuolitulehdus ja ripuli (johtuen Clostridium difficilestä) esiintyy useammin vanhuksilla (> 60-vuotiaat) ja voivat olla vakavampia. Näitä potilaita tulee seurata huolellisesti ripulin kehittymisen varalta.
Klindamysiinin farmakokineettiset tutkimukset eivät ole osoittaneet kliinisesti merkittäviä eroja nuorten ja iäkkäiden potilaiden välillä, joilla on normaali maksan toiminta ja normaali (ikää mukautettu) munuaisten toiminta suun kautta tai suonensisäisen annon jälkeen.
YLIANNOSTUS
Merkittävää kuolleisuutta havaittiin hiirillä 855 mg/kg:n laskimonsisäisellä annoksella ja rotilla suun kautta tai ihonalaisesti annetulla noin 2618 mg/kg:n annoksella. Hiirillä havaittiin kouristuksia ja masennusta.
Hemodialyysi ja peritoneaalidialyysi eivät poista klindamysiiniä tehokkaasti seerumista.
VASTA-AIHEET
CLEOCIN 150mg HCl on vasta-aiheinen henkilöille, jotka ovat aiemmin olleet yliherkkiä klindamysiiniä tai linkomysiiniä sisältäville valmisteille.
KLIININEN FARMAKOLOGIA
Ihmisen farmakologia
Imeytyminen
Seerumitasotutkimukset 150 mg:n oraalisella klindamysiinihydrokloridiannoksella 24 normaalilla aikuisella vapaaehtoisella osoittivat, että klindamysiini imeytyi nopeasti suun kautta annetun annon jälkeen. Keskimääräinen seerumin huipputaso 2,50 mcg/ml saavutettiin 45 minuutissa; seerumitasot olivat keskimäärin 1,51 mcg/ml 3 tunnin kohdalla ja 0,70 mcg/ml 6 tunnin kohdalla. Suun kautta annetun annoksen imeytyminen on käytännössä täydellinen (90 %), eikä samanaikainen ruoan anto muuta seerumin pitoisuuksia merkittävästi. seerumin tasot ovat olleet tasaisia ja ennustettavissa henkilöstä toiseen ja annoksesta toiseen. Seerumitasotutkimukset CLEOCIN 150 mg HCl:n useiden annosten jälkeen enintään 14 päivän ajan eivät osoita merkkejä lääkkeen kertymisestä tai muuttuneesta metaboliasta. Terveet vapaaehtoiset ovat sietäneet hyvin jopa 2 grammaa klindamysiiniä päivässä 14 päivän ajan, paitsi että ruoansulatuskanavan sivuvaikutusten ilmaantuvuus on suurempi suuremmilla annoksilla.
Jakelu
Klindamysiinin pitoisuudet seerumissa nousivat lineaarisesti annoksen kasvaessa. Seerumin pitoisuudet ylittävät MIC-arvon (minimi inhiboiva pitoisuus) useimpien indikoitujen organismien osalta vähintään kuuden tunnin ajan tavallisesti suositeltujen annosten annon jälkeen. Klindamysiini jakautuu laajalti kehon nesteisiin ja kudoksiin (mukaan lukien luut). Merkittäviä klindamysiinipitoisuuksia ei saavuteta aivo-selkäydinnesteessä edes tulehtuneiden aivokalvojen läsnä ollessa.
Aineenvaihdunta
Ihmisen maksan ja suoliston mikrosomeilla tehdyt in vitro -tutkimukset osoittivat, että klindamysiini metaboloituu pääasiassa sytokromi P450 3A4:n (CYP3A4) vaikutuksesta, ja CYP3A5:n osuus on vähäinen, jolloin muodostuu klindamysiinisulfoksidia ja vähäistä metaboliittia, N-desmetyyliklindamysiiniä.
Erittyminen
Keskimääräinen biologinen puoliintumisaika on 2,4 tuntia. Noin 10 % bioaktiivisuudesta erittyy virtsaan ja 3,6 % ulosteisiin; loppuosa erittyy bioinaktiivisina metaboliitteina.
Erikoispopulaatiot
Munuaisten vajaatoiminta
Klindamysiinin puoliintumisaika seerumissa on hieman pidentynyt potilailla, joiden munuaisten toiminta on selvästi heikentynyt. Hemodialyysi ja peritoneaalidialyysi eivät poista klindamysiiniä tehokkaasti seerumista.
Käyttö vanhuksilla
Iäkkäillä vapaaehtoisilla (61-79-vuotiaat) ja nuoremmilla aikuisilla (18-39-vuotiaat) tehdyt farmakokineettiset tutkimukset osoittavat, että ikä ei yksinään muuta klindamysiinin farmakokinetiikkaa (puhdistuma, eliminaation puoliintumisaika, jakautumistilavuus ja seerumin pitoisuus-aikakäyrän alla oleva pinta-ala ) klindamysiinifosfaatin suonensisäisen annon jälkeen. Klindamysiinihydrokloridin oraalisen annon jälkeen eliminaation puoliintumisaika pitenee noin 4,0 tuntiin (vaihteluväli 3,4–5,1 tuntia) vanhuksilla verrattuna 3,2 tuntiin (vaihteluväli 2,1–4,2 tuntia) nuoremmilla aikuisilla. Imeytymisaste ei kuitenkaan eroa ikäryhmien välillä, eikä annostusta tarvitse muuttaa iäkkäille potilaille, joilla on normaali maksan toiminta ja normaali (iän mukaan sovitettu) munuaisten toiminta1.
Mikrobiologia
Toimintamekanismi
Klindamysiini estää bakteerien proteiinisynteesiä sitoutumalla ribosomin 50S-alayksikön 23S-RNA:han. Klindamysiini on bakteriostaattinen.
Resistanssi
Resistenssi klindamysiinille johtuu useimmiten ribosomaalisen 23S-RNA:n spesifisten emästen modifikaatiosta. Klindamysiinin ja linkomysiinin välinen ristiresistenssi on täydellinen. Koska näiden antibakteeristen lääkkeiden sitoutumiskohdat menevät päällekkäin, linkosamidien, makrolidien ja streptogramiini B:n välillä havaitaan joskus ristiresistenssiä. Makrolidilla indusoituvaa resistenssiä klindamysiinille esiintyy joissakin makrolidiresistenttien bakteerien isolaateissa. Stafylokokkien ja beetahemolyyttisten streptokokkien makrolidiresistentit isolaatit tulee seuloa klindamysiiniresistenssin induktion suhteen käyttämällä D-aluetestiä.
Antimikrobinen aktiivisuus
Klindamysiinin on osoitettu olevan aktiivinen useimpia seuraavien mikro-organismien isolaatteja vastaan sekä in vitro että kliinisissä infektioissa, kuten KÄYTTÖAIHEET JA KÄYTTÖ osio.
Gram-positiiviset bakteerit
Staphylococcus aureus (metisilliinille herkät kannat) Streptococcus pneumoniae (penisilliinille herkät kannat) Streptococcus pyogenes
Anaerobiset bakteerit
Clostridium perfringens Fusobacterium necrophorum Fusobacterium nucleatum Peptostreptococcus anaerobius Prevotella melaninogenica
Vähintään 90 % alla luetelluista mikro-organismeista osoittavat in vitro minimiinhiboivia pitoisuuksia (MIC), jotka ovat pienempiä tai yhtä suuria kuin klindamysiinille alttiiden MIC-raja-arvo organismien, jotka ovat samantyyppisiä kuin taulukossa 1 esitetyt. Klindamysiinin tehokkuus kliinisten sairauksien hoidossa Näiden mikro-organismien aiheuttamia infektioita ei ole osoitettu riittävissä ja hyvin kontrolloiduissa kliinisissä tutkimuksissa.
Gram-positiiviset bakteerit
Staphylococcus epidermidis (metisilliinille herkät kannat) Streptococcus agalactiae Streptococcus anginosus Streptococcus mitis Streptococcus oralis
Anaerobiset bakteerit
Actinomyces israelii Clostridium clostridioforme Eggerthella lenta Finegoldia (Peptostreptococcus) magna Micromonas (Peptostreptococcus) micros Prevotella bivia Prevotella intermedia Propionibacterium acnes
Herkkyystestausmenetelmät
Kliinisen mikrobiologian laboratorion tulee toimittaa lääkärille paikallisissa sairaaloissa ja vastaanottoalueilla käytettävien mikrobilääkkeiden kumulatiiviset in vitro -herkkyystestien tulokset määräaikaisraportteina, jotka kuvaavat sairaalasta ja yhteisöstä hankittujen patogeenien herkkyysprofiilia, mikäli mahdollista. Näiden raporttien pitäisi auttaa lääkäriä valitsemaan antibakteerinen lääke hoitoon.
Laimennustekniikat
Kvantitatiivisia menetelmiä käytetään antimikrobisten vähimmäisinhibitoristen pitoisuuksien (MIC) määrittämiseen. Nämä MIC-arvot antavat arvioita bakteerien herkkyydestä antimikrobisille yhdisteille. MIC-arvot on määritettävä käyttämällä standardoitua testimenetelmää2,3 (liemi ja/tai agar). MIC-arvot tulee tulkita taulukossa 1 annettujen kriteerien mukaisesti.
Diffuusiotekniikat
Kvantitatiiviset menetelmät, jotka edellyttävät vyöhykkeiden halkaisijoiden mittaamista, voivat myös tarjota toistettavia arvioita bakteerien herkkyydestä antimikrobisille yhdisteille. Vyöhykkeen koko on määritettävä standardoidulla menetelmällä2,5. Tässä menetelmässä käytetään 2 mikrogrammalla klindamysiiniä kyllästettyjä paperilevyjä bakteerien herkkyyden klindamysiinille testaamiseen. Levyjen diffuusion keskeytyskohdat on esitetty taulukossa 1.
Anaerobiset tekniikat
Anaerobisten bakteerien herkkyys klindamysiinille voidaan määrittää standardoidulla testimenetelmällä2,4. Saadut MIC-arvot on tulkittava taulukossa 1 annettujen kriteerien mukaisesti.
Herkkä (S ) -raportti osoittaa, että mikrobilääke todennäköisesti estää patogeenin kasvua, jos antimikrobinen lääke saavuttaa pitoisuuden, joka on tavallisesti saavutettavissa infektiokohdassa. Välituotteen (I) raportti osoittaa, että tulosta on pidettävä epäselvänä, ja jos mikro-organismi ei ole täysin herkkä vaihtoehtoisille, kliinisesti toteuttamiskelpoisille lääkkeille, testi on toistettava. Tämä kategoria tarkoittaa mahdollista kliinistä soveltuvuutta kehon kohteisiin, joissa lääke on fysiologisesti keskittynyt tai tilanteissa, joissa voidaan käyttää suuria lääkeannoksia. Tämä kategoria tarjoaa myös puskurivyöhykkeen, joka estää pieniä, hallitsemattomia teknisiä tekijöitä aiheuttamasta suuria tulkintaeroja. Resistantin (R) raportti osoittaa, että mikrobilääke ei todennäköisesti estä patogeenin kasvua, jos antimikrobinen lääke saavuttaa pitoisuuden, joka on tavallisesti saavutettavissa infektiokohdassa; tulee valita muu hoitomuoto.
Laadunvalvonta
Standardoidut herkkyystestimenetelmät edellyttävät laboratoriokontrollien käyttöä määrityksessä käytettyjen tarvikkeiden ja reagenssien tarkkuuden ja tarkkuuden sekä testin suorittavien henkilöiden tekniikoiden valvomiseksi ja varmistamiseksi.2,3,4,5 Standardin klindamysiinijauheen tulee tarjota MIC-alueet taulukossa 2. Levydiffuusiotekniikassa, jossa käytetään 2 mcg:n klindamysiinilevyä, tulee saavuttaa taulukossa 2 esitetyt kriteerit.
anaerobit voidaan testata joko liemen mikrolaimennus- tai agarlaimennusmenetelmillä. NA=Ei sovellu ATCC® on American Type Culture Collectionin rekisteröity tavaramerkki
VIITTEET
1. Smith RB, Phillips JP: CLEOCIN HCl:n ja CLEOCIN-fosfaatin arviointi ikääntyneessä väestössä. Upjohn TR 8147-82-9122-021, joulukuu 1982.
2. CLSI. Performance Standards for Antimikrobial Susceptibility Testing: 26th ed. CLSI-lisäosa M100S. Wayne, PA: Clinical and Laboratory Standards Institute; 2016.
3. CLSI. Aerobisesti kasvavien bakteerien antimikrobisen herkkyystestien laimennusmenetelmät; Hyväksytty standardi – kymmenes painos. CLSI-asiakirja M07-A10. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.
4. CLSI. Anaerobisten bakteerien antimikrobisen herkkyyden testausmenetelmät; Hyväksytty Standard-Eighth Edition. CLSI-asiakirja M11-A8. Wayne, PA: Clinical and Laboratory Standards Institute; 2012
5. CLSI. Antimikrobisten levyjen herkkyystestien suorituskykystandardit; Hyväksytty Standard - kahdestoista painos. CLSI-asiakirja M02-A12. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.
POTILASTIEDOT
Potilaita tulee neuvoa, että antibakteerisia lääkkeitä, mukaan lukien CLEOCIN HCl, tulee käyttää vain bakteeri-infektioiden hoitoon. Ne eivät hoida virusinfektioita (esim. flunssaa). Kun CLEOCIN HCl on määrätty bakteeri-infektion hoitoon, potilaille tulee kertoa, että vaikka on yleistä, että olo paranee hoidon alussa, lääkettä tulee ottaa täsmälleen ohjeiden mukaan. Annosten väliin jättäminen tai koko hoitojakson suorittamatta jättäminen voi (1) heikentää välittömän hoidon tehokkuutta ja (2) lisätä todennäköisyyttä, että bakteerit kehittävät resistenssiä eikä niitä voida hoitaa CLEOCIN 150mg HCl:lla tai muilla antibakteerisilla lääkkeillä tulevaisuudessa.
Ripuli on yleinen antibioottien aiheuttama ongelma, joka yleensä loppuu, kun antibioottihoito lopetetaan. Joskus antibioottihoidon aloittamisen jälkeen potilaille voi ilmaantua vetisiä ja verisiä ulosteita (vatsakouristuksella ja kuumeella tai ilman) jopa kahden tai useamman kuukauden kuluttua viimeisen antibioottiannoksen ottamisesta. Jos näin tapahtuu, potilaiden tulee ottaa yhteyttä lääkäriin mahdollisimman pian.
