Luvox 100mg, 50mg Fluvoxamine Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mikä on Luvox (fluvoksamiinimaleaatti) ja miten sitä käytetään?
Luvox 100mg on reseptilääke, jota käytetään pakko-oireisen häiriön oireiden hoitoon. Luvoxia voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Luvox 100mg kuuluu lääkeryhmään, jota kutsutaan masennuslääkkeiksi, SSRI:iksi.
Ei tiedetä, onko Luvox 100 mg turvallinen ja tehokas alle 8-vuotiaille lapsille.
Mitkä ovat Luvoxin mahdolliset sivuvaikutukset?
Luvox voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- ahdistus,
- kilpa ajatuksia,
- riskinottoa,
- unihäiriöt (unettomuus),
- äärimmäisen onnellisuuden tai ärtyneisyyden tunne,
- näön hämärtyminen,
- putkinäkö,
- silmäkipu tai turvotus,
- nähdä halo pyöreitä valoja,
- kouristukset (kohtaukset),
- painon tai ruokahalun muutokset,
- helppo mustelma tai epätavallinen verenvuoto,
- päänsärky,
- hämmennystä,
- muistiongelmia,
- vakava heikkous,
- koordinaation menetys,
- epävakaa olo,
- erittäin jäykät (jäykät) lihakset,
- korkea kuume,
- hikoilu,
- hämmennystä,
- nopeat tai epätasaiset sydämenlyönnit,
- vapina,
- huimaus,
- agitaatio,
- hallusinaatiot,
- hikoilu,
- vapina
- nopea syke,
- lihasten jäykkyys,
- nykiminen,
- pahoinvointi,
- oksentelua ja
- ripuli
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Luvox 50mg:n yleisimmät sivuvaikutukset ovat:
- uneliaisuus,
- huimaus,
- vapina,
- ahdistunut olo,
- masentunut,
- unihäiriöt (unettomuus),
- ärtynyt vatsa,
- kaasu,
- ruokahalun menetys,
- pahoinvointi,
- oksentelua,
- ripuli,
- kuiva suu,
- ammottava,
- kipeä kurkku,
- lihaskipu,
- hikoilu,
- ihottuma,
- raskaat kuukautiset,
- vähentynyt seksihalu,
- epänormaali siemensyöksy ja
- vaikeuksia saada orgasmi
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Luvoxin mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
Itsemurha- ja masennuslääkeaineet
Masennuslääkkeet lisäsivät plaseboon verrattuna itsemurha-ajattelun ja -käyttäytymisen (itsetuhoisuuden) riskiä lapsilla, nuorilla ja nuorilla aikuisilla lyhytaikaisissa masennushäiriön (MDD) ja muiden psykiatristen häiriöiden tutkimuksissa. Jokaisen, joka harkitsee Fluvox 50mgamine Maleate -tablettien tai minkä tahansa muun masennuslääkkeen käyttöä lapsella, nuorella tai nuorella aikuisella, on tasapainotettava tämä riski kliinisen tarpeen kanssa. Lyhytaikaiset tutkimukset eivät osoittaneet lisääntynyttä itsemurhariskiä masennuslääkkeillä lumelääkkeeseen verrattuna yli 24-vuotiailla aikuisilla; 65-vuotiailla ja sitä vanhemmilla aikuisilla masennuslääkkeiden riski pieneni lumelääkkeeseen verrattuna. Masennus ja tietyt muut psykiatriset häiriöt liittyvät itsemurhariskin lisääntymiseen. Kaiken ikäisiä potilaita, jotka saavat masennuslääkehoitoa, tulee seurata asianmukaisesti ja tarkkailla kliinisen pahenemisen, itsemurha-ajattelun tai epätavallisten käyttäytymismuutosten varalta. Perheille ja omaishoitajille tulee kertoa, että heitä on tarkkailtava tarkasti ja kommunikoida lääkärin kanssa. Fluvox 50mgamine Maleate -tabletteja ei ole hyväksytty käytettäväksi lapsipotilailla paitsi potilailla, joilla on pakko-oireinen häiriö (OCD). [Katso VAROITUKSET JA VAROTOIMET - Kliininen paheneminen ja itsemurhariski ].
KUVAUS
Fluvoksamiinimaleaatti on selektiivinen serotoniinin (5-HT) takaisinoton estäjä (SSRI), joka kuuluu kemialliseen sarjaan, aralkyyliketonien 2-aminoetyylioksiimieettereihin.
Se on kemiallisesti nimetty 5-metoksi-4'-(trifluorimetyyli)valerofenoni-(E)-O-(2-aminoetyyli)oksiimimaleaatiksi (1:1) ja sen empiirinen kaava on C15H21O2N2F3•C4H4O4. Sen molekyylipaino on 434,41. Rakennekaava on:
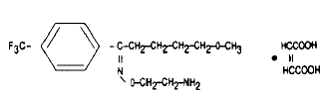
Fluvox 100mgamine maleate on valkoinen tai luonnonvalkoinen, hajuton, kiteinen jauhe, joka liukenee niukasti veteen, liukenee hyvin etanoliin ja kloroformiin ja on käytännössä liukenematon dietyylieetteriin.
Fluvoksamiinimaleaattitabletteja on saatavana 25 mg:n, 50 mg:n ja 100 mg:n vahvuuksina oraaliseen käyttöön. Vaikuttavan aineen, fluvox 100mgamine maleaatin, lisäksi jokainen tabletti sisältää seuraavat inaktiiviset aineet: karnaubavaha, hypromelloosi, mannitoli, polyetyleeniglykoli, polysorbaatti 80, esigelatinoitu tärkkelys (peruna), piidioksidi, natriumstearyylifumaraatti, tärkkelys (koraani), ja titaanidioksidia. 50 mg ja 100 mg tabletit sisältävät myös synteettisiä rautaoksideja.
INDIKAATIOT
Pakko-oireinen häiriö
Fluvoksamiinimaleaattitabletit on tarkoitettu pakko-oireiden ja pakko-oireiden hoitoon potilailla, joilla on pakko-oireinen häiriö (OCD), joka on määritelty DSM-III-R:ssä tai DSM-IV:ssä. Pakko- tai pakkomielteet aiheuttavat huomattavaa ahdistusta, ovat aikaa vieviä tai häiritsevät merkittävästi sosiaalista tai ammatillista toimintaa.
Pakko-oireiselle häiriölle on ominaista toistuvat ja jatkuvat ideat, ajatukset, impulssit tai mielikuvat (pakkomielle), jotka ovat ego-dystonisia ja/tai toistuvia, tarkoituksenmukaisia ja tahallisia käyttäytymismalleja (pakko-oireita), jotka henkilö pitää liiallisina tai kohtuuttomina.
Fluvox 100mgamine Maleate Tablets -tablettien teho vahvistettiin neljässä tutkimuksessa avohoitopotilailla, joilla on OCD: kaksi 10 viikon tutkimusta aikuisilla, yksi 10 viikon tutkimus lapsipotilailla (8-17-vuotiaat) ja yksi ylläpitotutkimus aikuisilla [ks. Kliiniset tutkimukset ].
ANNOSTELU JA HALLINNOINTI
Aikuiset
Fluvox 50mgamine Maleate -tablettien suositeltu aloitusannos aikuisille potilaille on 50 mg kerta-annoksena vuorokaudessa nukkumaan mennessä. Kontrolloiduissa kliinisissä tutkimuksissa, joissa vahvistettiin fluvoksamiinimaleaattitablettien tehoa OCD:ssä, potilaiden annos titrattiin 100-300 mg/vrk. Sen vuoksi annosta tulee suurentaa 50 mg:n välein 4–7 päivän välein siedettävyyden mukaan, kunnes saavutetaan suurin terapeuttinen hyöty, ei kuitenkaan yli 300 mg päivässä. On suositeltavaa, että yli 100 mg:n vuorokausiannos jaetaan kahteen annokseen. Jos annokset eivät ole samat, suurempi annos tulee antaa nukkumaan mennessä.
Pediatriset väestöryhmät (lapset ja nuoret)
Fluvoxamine Maleate -tablettien suositeltu aloitusannos lapsipotilaille (8–17-vuotiaat) on 25 mg kerta-annoksena vuorokaudessa nukkumaan mennessä. Kontrolloidussa kliinisessä tutkimuksessa, jossa vahvistettiin fluvoksamiinimaleaattitablettien tehoa OCD:ssä, lapsipotilaiden (8–17-vuotiaat) annos titrattiin 50–200 mg/vrk. Lääkäreiden tulee ottaa huomioon ikä- ja sukupuolierot antaessaan annostusta lapsipotilaille. Enimmäisannos alle 11-vuotiaille lapsille ei saa ylittää 200 mg/vrk. Naislapsilla terapeuttinen vaikutus voidaan saavuttaa pienemmillä annoksilla. Annoksen muuttaminen nuorilla (aikuisen enimmäisannokseen 300 mg asti) voi olla aiheellista terapeuttisen hyödyn saavuttamiseksi. Annosta tulee suurentaa 25 mg:n välein 4–7 päivän välein siedetyn hoidon mukaan, kunnes suurin terapeuttinen hyöty saavutetaan. On suositeltavaa, että yli 50 mg:n vuorokausiannos jaetaan kahteen annokseen. Jos jaetut annokset eivät ole samat, suurempi annos tulee antaa nukkumaan mennessä.
Iäkkäät tai maksan vajaatoimintapotilaat
Iäkkäillä potilailla ja potilailla, joilla on maksan vajaatoiminta, fluvoksamiinimaleaatin puhdistuman on havaittu vähentyneen. Tästä syystä voi olla tarkoituksenmukaista muuttaa näiden potilasryhmien aloitusannosta ja sitä seuraavaa annostitrausta.
Potilaan vaihtaminen psykiatristen häiriöiden hoitoon tarkoitettuun monoamiinioksidaasin estäjään (MAOI)
Psykiatristen häiriöiden hoitoon tarkoitetun MAO-estäjän käytön lopettamisen ja Fluvox 50mgamine Maleate -tabletilla hoidon aloittamisen välillä tulee kulua vähintään 14 päivää. Toisaalta Fluvox 100mgamine Maleate -tablettien lopettamisen jälkeen tulisi varata vähintään 14 päivää ennen MAO-estäjän aloittamista psykiatristen häiriöiden hoitoon [ks. VASTA-AIHEET ].
Fluvoksamiinimaleaattitablettien käyttö muiden MAO-estäjien, kuten linetsolidin tai metyleenisinisen kanssa
Älä aloita Fluvoxamine Maleate -tablettien käyttöä potilaalla, jota hoidetaan linetsolidilla tai suonensisäisellä metyleenisinisellä, koska serotoniinioireyhtymän riski on lisääntynyt. Potilaalla, joka tarvitsee psykiatrisen tilan kiireellistä hoitoa, tulee harkita muita toimenpiteitä, mukaan lukien sairaalahoitoa [ks. VASTA-AIHEET ].
Joissakin tapauksissa potilas, joka jo saa Fluvox 50mgamine Maleate -tabletteja, saattaa vaatia kiireellistä hoitoa linetsolidilla tai suonensisäisellä metyleenisinisellä. Jos hyväksyttäviä vaihtoehtoja linetsolidi- tai suonensisäiselle metyleenisinihoidolle ei ole saatavilla ja linetsolidi- tai suonensisäisen metyleenisinihoidon mahdollisten hyötyjen katsotaan olevan suurempia kuin serotoniinioireyhtymän riskit tietyllä potilaalla, fluvoksamiinimaleaattitablettien käyttö on lopetettava välittömästi ja linetsolidi- tai suonensisäinen annostelu metyleenisinistä voidaan antaa. Potilasta tulee tarkkailla serotoniinioireyhtymän oireiden varalta kahden viikon ajan tai 24 tunnin ajan viimeisen linetsolidin tai suonensisäisen metyleenisinisen annoksen jälkeen sen mukaan, kumpi tulee ensin. Hoitoa Fluvox 100mgamine Maleate -tableteilla voidaan jatkaa 24 tuntia viimeisen linetsolidin tai suonensisäisen metyleenisinisen annoksen jälkeen [ks. VAROITUKSET JA VAROTOIMET ].
Riski metyleenisinisen antamisesta ei-intravenoosisesti (kuten suun kautta otettavien tablettien tai paikallisten injektioiden kautta) tai suonensisäisinä annoksina, jotka ovat paljon pienempiä kuin 1 mg/kg Fluvox 100mgamine Maleate -tablettien kanssa, on epäselvä. Kliinikon tulee kuitenkin olla tietoinen serotoniinioireyhtymän oireiden mahdollisuudesta tällaisen käytön yhteydessä [ks. VAROITUKSET JA VAROTOIMET ].
Huolto/jatko-pidennetty hoito
Yleisesti ollaan samaa mieltä siitä, että pakko-oireinen häiriö vaatii useita kuukausia tai pidempään jatkuvaa farmakologista hoitoa. Hyöty OCD-potilaiden ylläpitämisestä fluvoksamiinimaleaattitableteilla sen jälkeen, kun vaste oli saavutettu keskimäärin noin 4 viikon ajan 10 viikon kertasokkovaiheessa, jonka aikana potilaita titrattiin vaikutuksen saavuttamiseksi, osoitettiin kontrolloidussa tutkimuksessa [ks. Kliiniset tutkimukset ].
Lääkärin, joka päättää käyttää Fluvoxamine Maleate -tabletteja pitkiä aikoja, tulee säännöllisesti arvioida uudelleen lääkkeen pitkän aikavälin hyödyllisyys yksittäiselle potilaalle.
Fluvoksamiinimaleaattitableteilla hoidon lopettaminen
Muiden SSRI- tai SNRI-lääkkeiden käytön lopettamiseen liittyviä oireita on raportoitu [katso VAROITUKSET JA VAROTOIMET ]. Potilaita tulee seurata näiden oireiden varalta, kun hoito lopetetaan. Annoksen asteittaista pienentämistä äkillisen lopettamisen sijaan suositellaan aina kun mahdollista. Jos sietämättömiä oireita ilmaantuu annoksen pienentämisen tai hoidon lopettamisen jälkeen, voidaan harkita jatkamista aiemmin määrätyllä annoksella. Tämän jälkeen lääkäri voi jatkaa annoksen pienentämistä, mutta asteittain.
MITEN TOIMITETAAN
Annostusmuodot ja vahvuudet
Fluvoxamine Maleate -tabletit USP ovat saatavilla seuraavasti:
Tabletit 25 mg: jakouurteet, valkoiset, elliptiset, kalvopäällysteiset (toisella puolella kaiverrus "1222")
50 mg tabletit: jakouurteinen, keltainen, elliptinen, kalvopäällysteinen (toisella puolella merkintä "1225" ja toisella uurrettu)
100 mg tabletit: jakouurteinen, beige, elliptinen, kalvopäällysteinen (toisella puolella merkintä "1221" ja toisella uurrettu)
Varastointi ja käsittely
Fluvox 50mgamine Maleate Tablets USP on saatavana seuraavina vahvuuksina, väreinä, painatuksina ja esitysmuodoissa:
uurteeton, valkoinen, elliptinen, kalvopäällysteinen (toisella puolella merkintä "1222")
Pullot 100 .............. NDC 62559-158-01
uurrettu, keltainen, elliptinen, kalvopäällysteinen (toisella puolella kaiverrus "1225" ja toisella uurrettu)
Pullot 100 .............. NDC 62559-159-01
uurrettu, beige, elliptinen, kalvopäällysteinen (toisella puolella kaiverrus "1221" ja toisella uurrettu)
Pullot 100 .............. NDC 62559-160-01
Pitää poissa lasten ulottuvilta.
Fluvoksamiinimaleaattitabletit tulee suojata korkealta kosteudelta ja säilyttää 20–25 °C:ssa (68–77 °F); retket sallitaan 15° - 30°C (59° - 86°F) [katso USP-ohjattu huonelämpötila ].
Annostele tiiviisiin astioihin.
Valmistaja: ANI Pharmaceuticals, Inc., Baudette, MN 56623. Tarkistettu: heinäkuu 2021
SIVUVAIKUTUKSET
Koska kliiniset tutkimukset suoritetaan hyvin vaihtelevissa olosuhteissa, lääkkeen kliinisissä tutkimuksissa havaittuja haittavaikutuksia ei voida suoraan verrata toisen lääkkeen kliinisissä tutkimuksissa havaittuihin nopeuksiin, eivätkä ne välttämättä kuvasta käytännössä havaittuja nopeuksia.
Haittavaikutukset, jotka johtavat hoidon lopettamiseen
Pohjois-Amerikassa kontrolloiduissa kliinisissä tutkimuksissa fluvoksamiinimaleaatilla hoidetuista 1087 potilaasta, jotka sairastavat potilasta ja masennusta, 22 % keskeytti hoidon haittavaikutuksen vuoksi. Haittavaikutukset, jotka johtivat hoidon lopettamiseen vähintään 2 %:lla fluvoksamiinimaleaattia saaneista potilaista näissä tutkimuksissa, olivat: pahoinvointi (9 %), unettomuus (4 %), uneliaisuus (4 %), päänsärky (3 %) ja voimattomuus, oksentelu , hermostuneisuus, kiihtyneisyys ja huimaus (2 % kumpikin).
Ilmaantuvuus kontrolloiduissa kokeissa
Yleisesti havaitut haittavaikutukset kontrolloiduissa kliinisissä tutkimuksissa
Fluvox 100mgamine Maleate -tabletteja on tutkittu 10 viikkoa kestäneissä lyhytaikaisissa kontrolloiduissa OCD:n (N=320) ja masennuksen (N=1350) tutkimuksissa. Yleensä haittavaikutusten määrät olivat samankaltaisia molemmissa tietosarjoissa sekä lasten OCD-tutkimuksessa. Taulukosta 2 saadut yleisimmin havaitut fluvoksamiinimaleaattitablettien käyttöön liittyvät ja todennäköisesti lääkkeeseen liittyvät haittavaikutukset (ilmaantuvuus 5 % tai enemmän ja vähintään kaksinkertainen lumelääkkeeseen verrattuna) olivat: pahoinvointi, uneliaisuus, unettomuus, voimattomuus, hermostuneisuus, dyspepsia, epänormaali siemensyöksy, hikoilu, anoreksia, vapina ja oksentelu. Kahdessa tutkimuksessa, joihin osallistui vain OCD-potilaita, tunnistettiin seuraavat lisäreaktiot käyttämällä yllä olevaa sääntöä: anorgasmia, heikentynyt libido, suun kuivuminen, nuha, makuaistin vääristyminen ja virtsaamistiheys. OCD-potilailla tehdyssä tutkimuksessa havaittiin seuraavat lisäreaktiot käyttämällä yllä olevaa sääntöä: kiihtymys, masennus, kuukautishäiriöt, ilmavaivat, hyperkinesia ja ihottuma.
Haittavaikutukset, joita esiintyy 1 %:lla
Taulukossa 2 luetellaan haittavaikutukset, joita esiintyi aikuisilla vähintään 1 %:lla ja jotka olivat yleisempiä kuin lumeryhmässä potilailla, joita hoidettiin fluvoksamiinimaleaattitableteilla kahdessa lyhytaikaisessa lumelääkekontrolloidussa OCD-tutkimuksessa (10 viikkoa) ja masennus. tutkimuksissa (6 viikkoa), joissa potilaille annosteltiin yleensä 100-300 mg/vrk. Tämä taulukko näyttää niiden potilaiden prosenttiosuuden kussakin ryhmässä, joilla oli vähintään yksi reaktio jossain vaiheessa hoidon aikana. Raportoidut haittavaikutukset luokiteltiin käyttämällä standardia COSTART-pohjaista sanakirjaterminologiaa.
Lääkärin tulee olla tietoinen siitä, että näitä lukuja ei voida käyttää sivuvaikutusten ilmaantuvuuden ennustamiseen tavanomaisessa lääketieteellisessä käytännössä, jossa potilaan ominaisuudet ja muut tekijät voivat poiketa kliinisissä tutkimuksissa vallinneista. Samoin mainittuja esiintymistiheyksiä ei voida verrata lukuihin, jotka on saatu muista kliinisistä tutkimuksista, joissa on mukana erilaisia hoitoja, käyttöjä ja tutkijoita. Mainitut luvut antavat kuitenkin lääkkeen määräävälle lääkärille jonkinlaisen perustan arvioida lääkkeiden ja muiden tekijöiden suhteellista osuutta sivuvaikutusten ilmaantuvuusasteessa tutkitussa populaatiossa.
TAULUKKO 2: HOITOJEN ILMOITTAJIEN HAITTAVAIKUTUSTEN TAPAHTUMISET KEMIOITTAIN AIKUISTEN OCD- JA masennuspopulaatioissa YHDISTETTY1
Haittavaikutukset OCD:n plasebokontrolloiduissa tutkimuksissa, jotka eroavat huomattavasti (määritelty vähintään kaksinkertaiseksi eroksi) OCD:n ja masennuksen yhdistetyistä reaktioista plasebokontrolloiduissa tutkimuksissa
OCD-tutkimuksissa reaktiot, joiden nopeus oli kaksinkertainen verrattuna OCD- ja masennustutkimuksiin, olivat dysfagia ja amblyopia (useimmiten näön hämärtyminen). Lisäksi pahoinvointi väheni noin 25 %.
OCD-tutkimuksissa reaktiot, joiden nopeus oli kaksinkertainen verrattuna OCD- ja masennustutkimuksiin, olivat: voimattomuus, epänormaali siemensyöksy (useimmiten viivästynyt siemensyöksy), ahdistuneisuus, nuha, anorgasmia (miehillä), masennus, libidon heikkeneminen, nielutulehdus , kiihtyneisyys, impotenssi, myoklonus/nykiminen, jano, laihtuminen, jalkakrampit, lihaskipu ja virtsan kertymä. Nämä reaktiot on lueteltu OCD-tutkimuksissa laskunopeuden mukaan.
Muut haittavaikutukset OCD-lasten väestössä
Lapsipotilailla (N=57), joita hoidettiin Fluvox 100mgamine Maleate -tableteilla, haittavaikutusten kokonaisprofiili oli yleensä samanlainen kuin aikuistutkimuksissa havaittu, kuten taulukosta 2 käy ilmi. Seuraavat haittavaikutukset eivät kuitenkaan esiinny taulukossa 2, kahdella tai useammalla lapsipotilaalla, ja niitä esiintyi useammin fluvoksamiinimaleaattitabletteja kuin lumelääkettä saaneilla: yskän lisääntyminen, kuukautishäiriöt, mustelma, tunne-labiliteetti, nenäverenvuoto, hyperkinesia, maaninen reaktio, ihottuma, poskiontelotulehdus ja painon lasku.
Miesten ja naisten seksuaalinen toimintahäiriö SSRI-lääkkeiden kanssa
Vaikka muutokset seksuaalisessa halussa, seksuaalisessa suorituskyvyssä ja seksuaalisessa tyytyväisyydessä esiintyvät usein psykiatrisen häiriön ilmenemismuotoina ja ikääntymisen myötä, ne voivat olla myös seurausta lääkehoidosta. Erityisesti jotkut todisteet viittaavat siihen, että selektiiviset serotoniinin takaisinoton estäjät (SSRI:t) voivat aiheuttaa tällaisia epämiellyttäviä seksuaalisia kokemuksia.
Luotettavia arvioita seksuaaliseen haluun, suorituskykyyn ja tyytyväisyyteen liittyvien ei-toivottujen kokemusten esiintyvyydestä ja vakavuudesta on kuitenkin vaikea saada osittain siksi, että potilaat ja lääkärit saattavat olla haluttomia keskustelemaan niistä. Näin ollen tuotemerkinnöissä mainitut arviot epämiellyttävien seksuaalisten kokemusten ja suoritusten esiintyvyydestä aliarvioivat todennäköisesti niiden todellisen esiintyvyyden.
Taulukossa 3 on esitetty seksuaalisten sivuvaikutusten ilmaantuvuus, jonka ilmoitti vähintään 2 % potilaista, jotka käyttivät Fluvox 100mgamine Maleate -tabletteja lumekontrolloiduissa masennuksen ja OCD:n tutkimuksissa.
TAULUKKO 3: OCD:N JA Masennuksen SEKSUAALISISTA HAITTAVAIKUTUKSISTA ILMOITTAJIEN POTILASTEN prosenttiosuus AIKUISTEN PLACEBO-OHJELMATTOISSA KOKEISSA
Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia, joissa tutkittaisiin seksuaalista toimintahäiriötä fluvoksamiinihoidolla.
Fluvox 50mgamine -hoitoon on liittynyt useita priapismitapauksia. Niissä tapauksissa, joiden lopputulos oli tunnettu, potilaat toipuivat ilman jälkiseurauksia ja fluvox 50mgamine -hoidon lopettamisen jälkeen.
Vaikka SSRI-lääkkeiden käyttöön liittyvän seksuaalisen toimintahäiriön tarkkaa riskiä on vaikea tietää, lääkäreiden tulee rutiininomaisesti tiedustella tällaisia mahdollisia sivuvaikutuksia.
Elintoimintojen muutokset
Fluvoksamiinimaleaatti- ja plaseboryhmien vertailut erillisissä lyhytaikaisten OCD- ja masennustutkimusten pooleissa (1) eri elintoimintojen muuttujien mediaanimuutoksesta lähtötilanteesta ja (2) sellaisten potilaiden esiintyvyydestä, jotka täyttävät kriteerit mahdollisesti merkittäville muutoksille lähtötasosta useissa elintärkeissä tutkimuksissa. merkkimuuttujat eivät paljastaneet merkittäviä eroja fluvoksamiinimaleaatin ja lumelääkkeen välillä.
Laboratoriomuutokset
Fluvoksamiinimaleaatti- ja plaseboryhmien vertailut erillisissä lyhytaikaisten OCD- ja masennustutkimusten pooleissa, joissa tarkastellaan (1) mediaanimuutosta lähtötilanteesta eri seerumin kemian, hematologian ja virtsan analyysimuuttujien osalta ja (2) potilaiden ilmaantuvuutta, jotka täyttävät mahdollisesti tärkeiden muutosten kriteerit. eri seerumikemian, hematologian ja virtsan analyysimuuttujien lähtötasosta ei ilmennyt merkittäviä eroja fluvox 100mgamine -maleaatin ja lumelääkkeen välillä.
EKG:n muutokset
Fluvox 50mgamine maleaatti ja lumelääke ryhmien vertailut erillisissä lyhytaikaisten OCD- ja masennustutkimusten pooleissa, joissa (1) keskimääräinen muutos lähtötasosta eri EKG-muuttujissa ja (2) potilaiden ilmaantuvuus, jotka täyttävät kriteerit mahdollisesti merkittäville muutoksille lähtötasosta eri EKG:ssä muuttujat eivät paljastaneet merkittäviä eroja fluvoksamiinimaleaatin ja lumelääkkeen välillä.
Muut Fluvox 100mgamine Maleate -tablettien markkinointia edeltävän arvioinnin aikana havaitut reaktiot
Markkinointia edeltävissä kliinisissä tutkimuksissa, jotka suoritettiin Pohjois-Amerikassa ja Euroopassa, fluvoksamiinimaleaattia annettiin useita annoksia yhteensä 2 737:lle potilaalle, jotka kärsivät OCD:stä tai vakavasta masennushäiriöstä. Kliiniset tutkijat kirjasivat tähän altistumiseen liittyvät epäsuotuisat reaktiot käyttämällä valitsemaansa kuvaavaa terminologiaa. Näin ollen ei ole mahdollista antaa merkityksellistä arviota haittavaikutuksia kokeneiden henkilöiden osuudesta ryhmittelemättä ensin samantyyppisiä ei-toivottuja reaktioita rajoitettuun (eli vähennettyyn) määrään vakioreaktiokategorioita.
Seuraavissa taulukoissa raportoitujen haittavaikutusten luokittelussa on käytetty standardia COSTART-pohjaista sanakirjaterminologiaa. Jos reaktion COSTART-termi oli niin yleinen, ettei se ollut informatiivinen, se korvattiin informatiivisemmalla termillä. Esitetyt esiintymistiheydet edustavat sen vuoksi niiden 2737 potilaan osuutta, jotka olivat altistuneet useille fluvox 100mgamine -maleaatin annoksille ja jotka kokivat mainitun tyyppisen reaktion vähintään kerran saaessaan fluvoksamiinimaleaattia. Kaikki raportoidut reaktiot sisältyvät alla olevaan luetteloon seuraavin poikkeuksin: 1) ne reaktiot, jotka on jo lueteltu taulukossa 2, jossa esitetään yleisten haittavaikutusten ilmaantuvuus lumelääkekontrolloiduissa OCD- ja masennuksen kliinisissä tutkimuksissa, on jätetty pois; 2) ne reaktiot, joiden aiheuttajaa ei pidetty todennäköisenä, jätetään pois; 3) reaktiot, joille COSTART-termi oli liian epämääräinen ollakseen kliinisesti merkityksellinen ja joita ei voitu korvata informatiivisemmalla termillä; ja 4) reaktioita, jotka on raportoitu vain yhdellä potilaalla ja joiden katsottiin olevan mahdollisesti vakavia, ei sisällytetä. On tärkeää korostaa, että vaikka raportoidut reaktiot ilmenivät fluvoksamiinimaleaattihoidon aikana, syy-yhteyttä fluvoksamiinimaleaattiin ei ole osoitettu.
Reaktiot luokitellaan edelleen kehon järjestelmäluokkiin ja luetellaan esiintymistiheyden mukaan alenevassa järjestyksessä seuraavilla määritelmillä: toistuvat haittavaikutukset määritellään sellaisiksi, joita esiintyy yhden tai useamman kerran vähintään 1/100 potilaalla; Harvinaiset haittavaikutukset ovat niitä, joita esiintyy 1/100 - 1/1000 potilaalla; ja harvinaisia haittavaikutuksia ovat ne, joita esiintyy alle 1/1000 potilaalla.
Keho kokonaisuutena - Usein: huonovointisuus; Harvinainen: valoherkkyysreaktio ja itsemurhayritys.
Sydän- ja verisuonijärjestelmä - Usein: pyörtyminen.
Ruoansulatuselimistö - Harvinainen: maha-suolikanavan verenvuoto ja melena; Harvinainen: hematemesis.
Hemic ja lymfaattiset järjestelmät - Harvinainen: anemia ja mustelma; Harvinainen: purppura.
Aineenvaihdunta- ja ravitsemusjärjestelmät - Usein: painon nousu ja laihtuminen.
Hermosto - Usein: hyperkinesia, maaninen reaktio ja myoklonus; Harvinaiset: epänormaalit unet, akatisia, kouristukset, dyskinesia, dystonia, euforia, ekstrapyramidaalinen oireyhtymä ja nykiminen; Harvinainen: vieroitusoireyhtymä.
Hengityselimet - Harvinainen: nenäverenvuoto. Harvinaiset: hemoptysis ja kurkunpäänsärky.
Iho - Harvinainen: urtikaria.
Urogenitaalijärjestelmä* - Harvinainen: hematuria, menorragia ja emättimen verenvuoto; Harvinainen: hematospermia.
* Perustuu urosten tai naaraiden lukumäärään tapauksen mukaan.
Markkinoinnin jälkeiset raportit
Seuraavat haittavaikutukset on tunnistettu Fluvox 100mgamine Maleate -tablettien käytön jälkeen hyväksynnän jälkeen. Koska nämä reaktiot on raportoitu vapaaehtoisesti epävarman kokoisesta populaatiosta, ei ole aina mahdollista luotettavasti arvioida niiden esiintymistiheyttä tai määrittää syy-yhteyttä lääkkeelle altistumiseen.
Vapaaehtoiset raportit haittavaikutuksista Fluvox 50mgamine Maleate -tabletteja käyttävillä potilailla, joita on saatu markkinoille tulon jälkeen ja joiden syy-yhteyttä Fluvoxamine Maleate -tablettien käyttöön ei tunneta, ovat: akuutti munuaisten vajaatoiminta, agranulosytoosi, amenorrea, anafylaktinen reaktio, angioedeema, bulloottinen aplastinen ja ruptio , Henoch-Schoenleinin purppura, hepatiitti, ileus, haimatulehdus, porfyria, Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi, vaskuliitti ja kammiotakykardia (mukaan lukien torsades de pointes).
HUUMEIDEN VUOROVAIKUTUKSET
Mahdolliset vuorovaikutukset lääkkeiden kanssa, jotka estävät sytokromi P450 -isoentsyymejä tai metaboloivat niitä
Useat maksan sytokromi P450 isoentsyymit osallistuvat useiden rakenteellisesti erilaisten lääkkeiden ja endogeenisten yhdisteiden oksidatiiviseen biotransformaatioon. Saatavilla oleva tieto fluvoksamiinin ja sytokromi P450 isoentsyymijärjestelmän suhteesta on saatu pääosin terveillä vapaaehtoisilla tehdyistä farmakokineettisistä yhteisvaikutustutkimuksista, mutta myös alustavia in vitro -tietoja on saatavilla. Perustuu havaintoon, jossa fluvox 50mgamine -valmisteella on merkittäviä yhteisvaikutuksia tiettyjen näistä lääkkeistä [katso tämän osan myöhemmät osat ja myös VAROITUKSET JA VAROTOIMET ] ja rajalliset in vitro -tiedot CYP3A4:stä, näyttää siltä, että fluvox 100mgamine estää useita sytokromi P450 isoentsyymejä, joiden tiedetään osallistuvan muiden lääkkeiden metaboliaan, kuten: CYP1A2 (esim. varfariini, teofylliini, propranololi, titsanidiini), CYP2C9 (esim. varfariini), CYP3A4 (esim. alpratsolaami) ja CYP2C19 (esim. omepratsoli).
In vitro -tiedot viittaavat siihen, että fluvoksamiini on suhteellisen heikko CYP2D6:n estäjä.
Noin 7 %:lla normaaliväestöstä on geneettinen koodi, joka johtaa CYP2D6:n aktiivisuuden vähenemiseen. Tällaisia henkilöitä on kutsuttu lääkkeiden, kuten debrisokiinin, dekstrometorfaanin ja trisyklisten masennuslääkkeiden "huonoksi metaboloijaksi" (PM). Vaikka mikään lääkeaineiden yhteisvaikutuksia tutkituista lääkkeistä ei vaikuttanut merkittävästi fluvoksiini 50 mg:n farmakokinetiikkaan, in vivo -tutkimus fluvoksamiinin kerta-annoksen farmakokinetiikkasta 13 PM:n koehenkilöillä osoitti muuttuneita farmakokineettisiä ominaisuuksia verrattuna 16 "laajuiseen metaboloijaan" (EM): keskimääräinen Cmax, AUC , ja puoliintumisaika pidentyi 52 %, 200 % ja 62 % PM:ssä verrattuna EM-ryhmään. Tämä viittaa siihen, että fluvox 100mgamine metaboloituu ainakin osittain CYP2D6:n välityksellä. Varovaisuutta on noudatettava potilailla, joilla tiedetään olevan alentuneet CYP2D6-aktiivisuuden tasot ja jotka saavat samanaikaisesti lääkkeitä, joiden tiedetään estävän tätä sytokromi P450-isoentsyymiä (esim. kinidiini).
Fluvoksamiinin metaboliaa ei ole täysin karakterisoitu, eikä voimakkaan sytokromi P450:n isoentsyymin eston, kuten CYP3A4:n ketokonatsolin eston, vaikutuksia fluvoksin 100 mg amiinin metaboliaan ole tutkittu.
Kliinisesti merkittävä fluvoksamiiniinteraktio on mahdollinen lääkkeiden kanssa, joilla on kapea terapeuttinen suhde, kuten pimotsidi, varfariini, teofylliini, tietyt bentsodiatsepiinit, omepratsoli ja fenytoiini. Jos Fluvox 100mgamine Maleate -tabletteja annetaan yhdessä sellaisen lääkkeen kanssa, joka eliminoituu oksidatiivisen aineenvaihdunnan kautta ja jolla on kapea terapeuttinen ikkuna, jälkimmäisen lääkkeen plasmapitoisuutta ja/tai farmakodynaamisia vaikutuksia on seurattava tarkasti, ainakin kunnes vakaan tilan olosuhteet ovat saavutettu. saavutettu [katso VASTA-AIHEET , VAROITUKSET JA VAROTOIMET ].
CNS-aktiiviset lääkkeet
Psykoosilääkkeet: Katso VAROITUKSET JA VAROTOIMET .
Bentsodiatsepiinit: Katso VAROITUKSET JA VAROTOIMET .
Alpratsolaami: Katso VAROITUKSET JA VAROTOIMET .
Diatsepaami: Katso VAROITUKSET JA VAROTOIMET .
Loratsepaami: Fluvoksamiinimaleaatin toistuvia annoksia (50 mg 2 kertaa) koskeva tutkimus terveillä vapaaehtoisilla miehillä (N=12) ja kerta-annoksella loratsepaamia (4 mg:n kerta-annos) ei osoittanut merkittäviä farmakokineettisiä yhteisvaikutuksia. Keskimäärin sekä loratsepaami yksinään että loratsepaami yhdessä fluvoksamiinin kanssa aiheuttivat huomattavia heikkenemiä kognitiivisissa toiminnassa; Fluvoksamiinin ja loratsepaamin samanaikainen anto ei kuitenkaan tuottanut suurempia keskimääräisiä vähennyksiä kuin pelkkä loratsepaami.
Alkoholi: Tutkimukset, joissa käytettiin kerta-annoksia 40 g etanolia (oraalinen anto yhdessä tutkimuksessa ja suonensisäinen toisessa tutkimuksessa) ja toistuva fluvox 100 mg gamiinimaleaatin annostelu (50 mg kahdesti päivässä), eivät paljastaneet kummankaan lääkkeen vaikutusta toisen lääkkeen farmakokinetiikkaan tai farmakodynamiikkaan. Kuten muitakin psykotrooppisia lääkkeitä käytettäessä, potilaita tulee neuvoa välttämään alkoholin käyttöä Fluvoxamine Maleate -tablettien käytön aikana.
Karbamatsepiini: Kohonneita karbamatsepiinipitoisuuksia ja toksisuusoireita on raportoitu, kun fluvoksi 100 mg amiinimaleaattia ja karbamatsepiinia on annettu samanaikaisesti.
Klotsapiini: Katso VAROITUKSET JA VAROTOIMET .
Litium: Kuten muutkin serotonergiset lääkkeet, litium saattaa voimistaa fluvoksamiinin serotonergisiä vaikutuksia, ja siksi yhdistelmää tulee käyttää varoen. Kouristuskohtauksia on raportoitu, kun fluvox 50mgamine maleaattia ja litiumia on annettu samanaikaisesti.
Metadoni: Katso VAROITUKSET JA VAROTOIMET .
Monoamiinioksidaasin estäjät: Katso ANNOSTELU JA HALLINNOINTI , VASTA-AIHEET , VAROITUKSET JA VAROTOIMET .
Pimotsidi: Katso VASTA-AIHEET , VAROITUKSET JA VAROTOIMET .
Ramelteon: Katso VAROITUKSET JA VAROTOIMET .
Serotonergiset lääkkeet: Katso ANNOSTELU JA HALLINNOINTI , VASTA-AIHEET , VAROITUKSET JA VAROTOIMET .
Takriini: Tutkimuksessa, johon osallistui 13 tervettä miespuolista vapaaehtoista, kerta-annos 40 mg takriinia lisättynä fluvox 50mgamine 100 mg/vrk vakaassa tilassa annettiin viisinkertaiseksi ja kahdeksankertaiseksi takriinin Cmax- ja AUC-arvoissa verrattuna takriinin anto yksinään. Viisi koehenkilöä koki pahoinvointia, oksentelua, hikoilua ja ripulia samanaikaisen annon jälkeen, mikä vastaa takriinin kolinergisiä vaikutuksia.
Tioridatsiini: Katso VASTA-AIHEET , VAROITUKSET JA VAROTOIMET .
Titsanidiini: Katso VASTA-AIHEET , VAROITUKSET JA VAROTOIMET .
Trisykliset masennuslääkkeet (TCA:t): Merkittävästi kohonneita plasman TCA-pitoisuuksia on raportoitu, kun fluvoksamiinimaleaattia ja amitriptyliiniä, klomipramiinia tai imipramiinia on annettu samanaikaisesti. Fluvoksamiinimaleaattitablettien ja TCA:iden yhteiskäytössä on noudatettava varovaisuutta. plasman TCA-pitoisuuksia on ehkä seurattava ja TCA-annosta on ehkä pienennettävä.
Triptaanit: Markkinoille tulon jälkeen on raportoitu harvoin serotoniinioireyhtymää SSRI:n ja triptaanin käytön yhteydessä. Jos fluvox 50mgamine -valmisteen samanaikainen hoito triptaanin kanssa on kliinisesti perusteltua, potilaan huolellinen seuranta on suositeltavaa, erityisesti hoidon aloittamisen ja annosta suurennettaessa [ks. VAROITUKSET JA VAROTOIMET ].
Sumatriptaani: Markkinoille tulon jälkeen on raportoitu harvoin potilaita, joilla on heikkoutta, hyperrefleksiaa ja koordinaatiohäiriöitä selektiivisen serotoniinin takaisinoton estäjän (SSRI) ja sumatriptaanin käytön jälkeen. Jos samanaikainen hoito sumatriptaanilla ja SSRI:llä (esim. fluoksetiini, fluvoksamiini, paroksetiini, sertraliini) on kliinisesti perusteltua, potilaan asianmukainen seuranta on suositeltavaa.
Tryptofaani: Tryptofaani saattaa voimistaa fluvoksamiinin serotonergisiä vaikutuksia, ja siksi yhdistelmää tulee käyttää varoen. Vaikeaa oksentelua on raportoitu fluvoksamiinimaleaatin ja tryptofaanin samanaikaisen käytön yhteydessä [ks. VAROITUKSET JA VAROTOIMET ].
Muut huumeet
Alosetroni: Katso VASTA-AIHEET , VAROITUKSET JA VAROTOIMET ja Lotronex™ (alosetron) pakkausseloste.
Digoksiini: Fluvox 100 mg amiinimaleaatti 100 mg vuorokaudessa 18 päivän ajan (N = 8) ei vaikuttanut merkitsevästi 1,25 mg:n digoksiinin suonensisäisen kerta-annoksen farmakokinetiikkaan.
Diltiatseemi: Bradykardiaa on raportoitu fluvoksamiinimaleaatin ja diltiatseemin samanaikaisen käytön yhteydessä.
Meksiletiini: Katso VAROITUKSET JA VAROTOIMET .
Propranololi ja muut beetasalpaajat: Fluvoksamiinimaleaatin 100 mg/vrk ja propranololin 160 mg/vrk samanaikainen antaminen normaaleille vapaaehtoisille johti keskimäärin viisinkertaiseen nousuun (vaihteluväli 2-17) plasman propranololin vähimmäispitoisuuksissa. Tässä tutkimuksessa propranololiinin aiheuttama sykkeen lasku ja rasituksen diastolinen paine voimistui hieman.
Yksi bradykardia- ja hypotensiotapaus ja toinen ortostaattinen hypotensiotapaus on raportoitu fluvoksamiinimaleaatin ja metoprololin samanaikaisen käytön yhteydessä.
Jos propranololia tai metoprololia annetaan samanaikaisesti Fluvox 50mgamine Maleate -tablettien kanssa, beetasalpaajan aloitusannoksen pienentämistä ja varovaisempaa annoksen titrausta suositellaan. Fluvoksamiinimaleaattitablettien annosta ei tarvitse muuttaa.
Fluvoksamiinimaleaatin (100 mg/vrk) ja atenololin 100 mg/vrk (N=6) samanaikainen anto ei vaikuttanut atenololin pitoisuuksiin plasmassa. Toisin kuin propranololi ja metoprololi, jotka metaboloituvat maksassa, atenololi eliminoituu pääasiassa munuaisten kautta.
Teofylliini: Katso VAROITUKSET JA VAROTOIMET .
Varfariini ja muut hemostaasia häiritsevät lääkkeet (NSAID, aspiriini jne.): Katso VAROITUKSET JA VAROTOIMET .
Tupakoinnin vaikutukset fluvoksamiinin aineenvaihduntaan
Tupakoitsijoilla fluvox 100mgamine -aineenvaihdunta lisääntyi 25 % tupakoimattomiin verrattuna.
Sähkökonvulsiivinen hoito (ECT)
Ei ole olemassa kliinisiä tutkimuksia, jotka osoittaisivat ECT:n ja fluvox 100mgamine maleaatin yhteiskäytön hyödyt tai riskit.
Huumeiden väärinkäyttö ja riippuvuus
Valvottu aine
Fluvoksamiinimaleaattitabletit eivät ole valvottuja aineita.
Riippuvuus
Fluvox 100mgamine maleaatin väärinkäytön, toleranssin ja fyysisen riippuvuuden mahdollisuutta on tutkittu ei-ihmiskädellisissä mallissa. Todisteita riippuvuusilmiöistä ei löytynyt. Fluvoksamiinimaleaattitablettien lopetusvaikutuksia ei arvioitu systemaattisesti kontrolloiduissa kliinisissä tutkimuksissa. Fluvoksamiinimaleaattitabletteja ei tutkittu systemaattisesti kliinisissä tutkimuksissa mahdollisten väärinkäytösten varalta, mutta kliinisissä tutkimuksissa ei havaittu merkkejä huumeiden etsimisestä. On kuitenkin huomattava, että potilaat, joilla oli riski saada lääkeriippuvuus, suljettiin järjestelmällisesti pois fluvox 100mgamine -maleaatin tutkimustutkimuksista. Yleisesti ei ole mahdollista ennustaa prekliinisen tai markkinointia edeltävän kliinisen kokemuksen perusteella, missä määrin keskushermostoon vaikuttavaa lääkettä käytetään väärin, ohjataan muualle ja/tai väärinkäyttöön sen jälkeen, kun se on markkinoille tullut. Tästä syystä lääkäreiden tulee arvioida huolellisesti potilaiden anamneesi huumeiden väärinkäytön varalta ja seurata tällaisia potilaita tarkasti ja tarkkailla heitä fluvoksamiinimaleaatin väärinkäytön tai väärinkäytön merkkien varalta (eli toleranssin kehittyminen, annoksen lisääminen, huumeiden etsintäkäyttäytyminen).
VAROITUKSET
Mukana osana VAROTOIMENPITEET osio.
VAROTOIMENPITEET
Kliininen paheneminen ja itsemurhariski
Potilaat, joilla on vaikea masennushäiriö (MDD), sekä aikuisilla että lapsilla, voivat kokea masennuksensa pahenemista ja/tai itsemurha-ajatuksia ja -käyttäytymisen ilmaantumista (itsemurha-ajatuksia) tai epätavallisia muutoksia käyttäytymisessä riippumatta siitä, käyttävätkö he masennuslääkkeitä vai eivät, ja tämä riski voi jatkua, kunnes merkittävä remissio tapahtuu. Itsemurha on tunnettu masennuksen ja tiettyjen muiden psykiatristen häiriöiden riski, ja nämä häiriöt itsessään ovat vahvimpia itsemurhan ennustajia. Pitkään on kuitenkin ollut huolta siitä, että masennuslääkkeillä voi olla rooli masennuksen pahenemisessa ja itsetuhoisuuden syntymisessä tietyillä potilailla hoidon alkuvaiheessa. Lyhytaikaisten lumekontrolloitujen masennuslääkkeiden (SSRI-lääkkeiden ja muiden) kokeiden yhdistetyt analyysit osoittivat, että nämä lääkkeet lisäävät itsemurha-ajattelun ja -käyttäytymisen (itsemurha-ajattelun) riskiä lapsilla, nuorilla ja nuorilla aikuisilla (18–24-vuotiaat), joilla on vakava masennushäiriö ( MDD) ja muut psykiatriset häiriöt. Lyhytaikaiset tutkimukset eivät osoittaneet lisääntynyttä itsemurhariskiä masennuslääkkeillä lumelääkkeeseen verrattuna yli 24-vuotiailla aikuisilla; 65-vuotiailla ja sitä vanhemmilla aikuisilla masennuslääkkeet vähenivät lumelääkkeeseen verrattuna.
Plasebokontrolloitujen tutkimusten yhdistetyt analyysit lapsilla ja nuorilla, joilla oli MDD, pakko-oireinen häiriö (OCD) tai muut psykiatriset häiriöt, sisälsivät yhteensä 24 lyhytaikaista tutkimusta 9 masennuslääkkeellä yli 4400 potilaalla. Plasebokontrolloitujen tutkimusten yhdistetyt analyysit aikuisilla, joilla oli MDD tai muita psykiatrisia häiriöitä, sisälsivät yhteensä 295 lyhytaikaista tutkimusta (mediaanikesto 2 kuukautta), joissa oli 11 masennuslääkettä yli 77 000 potilaalla. Itsemurhariskissä oli huomattavaa vaihtelua lääkkeiden välillä, mutta taipumus nuorempien potilaiden lisääntymiseen lähes kaikkien tutkittujen lääkkeiden kohdalla. Absoluuttisessa itsemurhariskissä oli eroja eri indikaatioiden välillä, ja suurin ilmaantuvuus MDD:ssä. Riskierot (lääke vs. lumelääke) olivat kuitenkin suhteellisen vakaita ikäryhmien sisällä ja eri käyttöaiheissa. Nämä riskierot (lääkkeen ja lumelääkkeen ero itsemurhatapausten määrässä 1000 hoidettua potilasta kohti) on esitetty taulukossa 1.
TAULUKKO 1: LÄÄKE-PLACEBO EROT ITSITURMATAPAUSTEN MÄÄRÄSSÄ 1 000 HOIDOTUA POTILASTA kohti
Yhtään itsemurhaa ei tapahtunut missään lapsitutkimuksessa. Aikuisten kokeissa oli itsemurhia, mutta määrä ei riittänyt päättämään lääkkeen vaikutuksesta itsemurhaan.
Ei tiedetä, ulottuuko itsemurhariski pitkäaikaiseen käyttöön eli useiden kuukausien jälkeiseen käyttöön. Lumekontrolloiduista ylläpitotutkimuksista aikuisilla, joilla on masennus, on kuitenkin huomattavaa näyttöä siitä, että masennuslääkkeiden käyttö voi viivyttää masennuksen uusiutumista.
Kaikkia potilaita, joita hoidetaan masennuslääkkeillä missä tahansa indikaatiossa, on seurattava asianmukaisesti ja tarkkailtava tarkasti kliinisen pahenemisen, itsemurha-ajattelun ja epätavallisten käyttäytymismuutosten varalta, erityisesti lääkehoidon ensimmäisten kuukausien aikana tai annosta muutettaessa, joko annosta suurennetaan. tai pienenee.
Seuraavia oireita, ahdistusta, kiihtyneisyyttä, paniikkikohtauksia, unettomuutta, ärtyneisyyttä, vihamielisyyttä, aggressiivisuutta, impulsiivisuutta, akatisiaa (psykomotorista levottomuutta), hypomaniaa ja maniaa on raportoitu myös aikuisilla ja lapsipotilailla, joita on hoidettu masennuslääkkeillä vakavan masennuksen vuoksi. kuten muissakin indikaatioissa, sekä psykiatrisissa että ei-psykiatrisissa. Vaikka syy-yhteyttä tällaisten oireiden ilmaantumisen ja joko masennuksen pahenemisen ja/tai itsetuhoisten impulssien ilmaantumisen välillä ei ole osoitettu, on huolestuttavaa, että tällaiset oireet voivat olla syntyvän itsetuhoisuuden esiaste.
Hoito-ohjelman muuttamista, mukaan lukien lääkityksen mahdollista lopettamista, tulee harkita potilailla, joiden masennus pahenee jatkuvasti tai joilla on ilmennyt itsemurha tai oireita, jotka saattavat olla masennuksen tai itsemurha-ajatuksen pahenemisen edeltäjä, varsinkin jos nämä oireet ovat vakavia, äkillisiä. oireiden alkaessa tai eivät olleet osa potilaan oireita.
Jos hoito on päätetty keskeyttää, lääkitystä tulee pienentää niin nopeasti kuin mahdollista, mutta huomioiden, että äkillinen lopettaminen voi liittyä tiettyihin oireisiin ja riskeihin [ks. ANNOSTELU JA HALLINNOINTI ].
Masennuslääkkeillä vakavan masennushäiriön tai muiden, sekä psykiatristen että ei-psykiatristen oireiden vuoksi hoidettavien potilaiden perheitä ja hoitajia tulee varoittaa tarpeesta seurata potilaita kiihtyneisyyden, ärtyneisyyden, epätavallisten käyttäytymismuutosten ja muiden edellä kuvattujen oireiden ilmaantumisen varalta. , sekä itsemurha-ajatuksen ilmaantumista, ja ilmoittamaan tällaisista oireista välittömästi terveydenhuollon tarjoajille. Tällaiseen seurantaan tulisi sisältyä perheiden ja omaishoitajien päivittäinen tarkkailu. Fluvoxamine Maleate -tabletteja koskevat reseptit tulee kirjoittaa pienintä tablettimäärää varten, mikä on potilaan hyvän hoidon mukaista, jotta voidaan vähentää yliannostusriskiä.
Potilaiden seulonta kaksisuuntaisen mielialahäiriön varalta
Vakava masennusjakso voi olla kaksisuuntaisen mielialahäiriön ensimmäinen ilmentymä. Yleisesti uskotaan (vaikkakaan sitä ei ole vahvistettu kontrolloiduissa tutkimuksissa), että tällaisen episodin hoito pelkällä masennuslääkkeellä voi lisätä seka-/maanisen vaiheen esiintymisen todennäköisyyttä potilailla, joilla on kaksisuuntaisen mielialahäiriön riski. Ei tiedetä, edustavatko mikään yllä kuvatuista oireista tällaista muutosta. Ennen masennuslääkehoidon aloittamista masennusoireista kärsivät potilaat tulee kuitenkin seuloa riittävästi sen määrittämiseksi, onko heillä kaksisuuntaisen mielialahäiriön riski; Tällaiseen seulontaan tulee sisältyä yksityiskohtainen psykiatrinen historia, mukaan lukien suvussa itsemurhaa, kaksisuuntaista mielialahäiriötä ja masennusta esiintynyt historia. On huomattava, että Fluvox 50mgamine Maleate -tabletteja ei ole hyväksytty käytettäväksi kaksisuuntaisen mielialahäiriön masennuksen hoidossa.
Serotoniinin oireyhtymä
Mahdollisesti hengenvaarallisen serotoniinioireyhtymän kehittymistä on raportoitu käytettäessä SNRI-lääkkeitä ja SSRI-lääkkeitä, mukaan lukien fluvoksamiinimaleaattitabletit, yksinään, mutta erityisesti käytettäessä samanaikaisesti serotonergisiä lääkkeitä (mukaan lukien triptaanit, trisykliset masennuslääkkeet, fentanyyli, litium, tramadoli, tryptofaani, busipironi, ja mäkikuisma) sekä lääkkeillä, jotka heikentävät serotoniinin aineenvaihduntaa (erityisesti MAO-estäjät, sekä psykiatristen häiriöiden hoitoon tarkoitetut että myös muut, kuten linetsolidi ja suonensisäinen metyleenisininen).
Serotoniinioireyhtymän oireita voivat olla mielentilan muutokset (esim. kiihtyneisyys, hallusinaatiot, delirium ja kooma), autonominen epävakaus (esim. takykardia, labiili verenpaine, huimaus, hikoilu, punoitus, hypertermia), hermo-lihaspoikkeavuuksia (esim. vapina, jäykkyys, myoklonus, hyperrefleksia, koordinaatiohäiriöt), kohtaukset ja/tai maha-suolikanavan oireet (esim. pahoinvointi, oksentelu, ripuli). Potilaita tulee seurata serotoniinioireyhtymän ilmaantumisen varalta.
Fluvoksamiinimaleaattitablettien samanaikainen käyttö psykiatristen häiriöiden hoitoon tarkoitettujen MAO-estäjien kanssa on vasta-aiheista. Fluvoksamiinimaleaattitabletteja ei myöskään saa aloittaa potilaalla, jota hoidetaan MAO-estäjillä, kuten linetsolidilla tai suonensisäisellä metyleenisinisellä. Kaikki metyleenisinistä koskevat raportit, jotka antoivat tietoa antoreitistä, koskivat suonensisäistä antoa annosalueella 1 mg/kg - 8 mg/kg. Ei raportoitu metyleenisinisen antamista muilla reiteillä (kuten oraalisilla tableteilla tai paikallisilla kudosinjektioilla) tai pienempinä annoksina. Fluvox 50mgamine Maleate -tabletteja käyttävällä potilaalla saattaa olla tilanteita, joissa MAO-estäjän, kuten linetsolidin tai suonensisäisen metyleenisinisen, hoito on aloitettava. Fluvox 50mgamine Maleate -tablettien käyttö tulee lopettaa ennen MAO:n estäjähoidon aloittamista [ks. VASTA-AIHEET , ANNOSTELU JA HALLINNOINTI ].
Jos fluvoksamiinimaleaattitablettien samanaikainen käyttö muiden serotonergisten lääkkeiden, mukaan lukien triptaanien, trisyklisten masennuslääkkeiden, fentanyylin, litiumin, tramadolin, buspironin, tryptofaanin, amfetamiinien ja mäkikuisman kanssa on kliinisesti perusteltua, potilaiden tulee olla tietoisia mahdollinen lisääntynyt serotoniinioireyhtymän riski, erityisesti hoidon aloittamisen ja annosta suurennettaessa.
Fluvoxamine Maleate -tablettien ja muiden samanaikaisten serotonergisten aineiden käyttö on lopetettava välittömästi, jos yllä mainitut tapahtumat ilmenevät, ja oireenmukaista tukihoitoa on aloitettava.
Kulman sulkeutuva glaukooma
Pupillien laajentuminen, joka ilmenee monien masennuslääkkeiden, mukaan lukien fluvoksamiinimaleaattitablettien, käytön jälkeen voi laukaista kulman sulkemiskohtauksen potilaalla, jolla on anatomisesti kapeat kulmat ja jolle ei ole tehty iridektomiaa.
Mahdollinen tioridatsiinivuorovaikutus
Fluvoksamiinin (25 mg kahdesti viikon ajan) vaikutusta tioridatsiinin vakaan tilan pitoisuuksiin arvioitiin 10 skitsofreniaa sairastavalla miespotilaalla. Tioridatsiinin ja sen kahden aktiivisen metaboliitin, mesoridatsiinin ja sulforidatsiinin, pitoisuudet kolminkertaistuivat fluvox 100 mg -valmisteen samanaikaisen annon jälkeen.
Tioridatsiinin antaminen saa aikaan annoksesta riippuvan QTc-ajan pidentymisen, mikä liittyy vakaviin kammiorytmioihin, kuten torsades de pointes -tyyppisiin rytmihäiriöihin ja äkilliseen kuolemaan. On todennäköistä, että tämä kokemus aliarvioi suurempien tioridatsiiniannosten aiheuttaman riskin. Lisäksi fluvox 100mgamine -valmisteen vaikutus voi olla vieläkin selvempi, kun sitä annetaan suurempina annoksina. Siksi fluvoksamiinia ja tioridatsiinia ei pitäisi antaa samanaikaisesti [katso VASTA-AIHEET ].
Mahdollinen titsanidiinivuorovaikutus
Fluvoksamiini on voimakas CYP1A2:n estäjä ja titsanidiini on CYP1A2:n substraatti. Fluvox 50mgamine (100 mg päivässä 4 päivän ajan) vaikutusta 4 mg:n titsanidiinin kerta-annoksen farmakokinetiikkaan ja farmakodynamiikkaan on tutkittu 10 terveellä miespuolisella koehenkilöllä. Titsanidiinin Cmax suureni noin 12-kertaiseksi (vaihteluväli 5-32-kertaiseksi), eliminaation puoliintumisaika piteni lähes 3-kertaiseksi ja AUC suureni 33-kertaiseksi (vaihteluväli 14-103-kertaiseksi). Keskimääräinen maksimaalinen vaikutus verenpaineeseen oli systolisen verenpaineen lasku 35 mm Hg, diastolisen verenpaineen lasku 20 mm Hg ja sydämen sykkeen lasku 4 lyöntiä/min. Uneliaisuus lisääntyi merkittävästi ja suorituskyky psykomotorisessa tehtävässä heikkeni merkittävästi. Fluvoksamiinia ja titsanidiinia ei tule käyttää yhdessä [katso VASTA-AIHEET ].
Mahdollinen pimotsidivuorovaikutus
Pimotsidi metaboloituu sytokromi P4503A4-isoentsyymin vaikutuksesta, ja on osoitettu, että ketokonatsoli, voimakas CYP3A4:n estäjä, estää tämän lääkkeen metaboliaa, mikä johtaa emolääkkeen plasmapitoisuuksien suurenemiseen. Pimotsidin suurentunut pitoisuus plasmassa aiheuttaa QT-ajan pidentymistä ja siihen on liittynyt torsades de pointes -tyyppistä kammiotakykardiaa, joka on joskus kuolemaan johtanut. Kuten alla on todettu, merkittävä farmakokineettinen yhteisvaikutus on havaittu fluvoksilla 100 mg yhdistelmässä alpratsolaamin kanssa. Lääke, jonka tiedetään metaboloituvan CYP3A4:n välityksellä. Vaikka ei olekaan lopullisesti osoitettu, että fluvox 100mgamine on voimakas CYP3A4:n estäjä, se todennäköisesti on, koska fluvox 50mgamine -valmisteella on merkittävä yhteisvaikutus alpratsolaamin kanssa. Tästä syystä on suositeltavaa, että fluvoksamiinia ei käytetä yhdessä pimotsidin kanssa [katso VASTA-AIHEET ].
Mahdollinen Alosetroni-vuorovaikutus
Koska alosetroni metaboloituu useiden maksan CYP-lääkkeitä metaboloivien entsyymien toimesta, näiden entsyymien induktorit tai estäjät voivat muuttaa alosetronin puhdistumaa. Fluvox 50mgamine on tunnettu voimakas CYP1A2:n estäjä ja myös CYP3A4, CYP2C9 ja CYP2C19. Farmakokineettisessä tutkimuksessa 40 tervettä naishenkilöä sai fluvoksi 100 mg fluvox 100 mg vuorokaudessa kasvavina annoksina 50 mg:sta 200 mg:aan vuorokaudessa 16 päivän ajan, ja alosetronia annettiin 1 mg viimeisenä päivänä. Fluvox 50mgamine nosti keskimääräistä alosetronin plasmapitoisuutta (AUC) noin 6-kertaiseksi ja pidensi puoliintumisaikaa noin 3-kertaiseksi. [Katso VASTA-AIHEET ja Lotronex™ (alosetroni) pakkausseloste].
Muut potentiaalisesti tärkeät huumeiden yhteisvaikutukset
Bentsodiatsepiinit
Maksan hapettumisen kautta metaboloituvia bentsodiatsepiineja (esim. alpratsolaami, midatsolaami, triatsolaami jne.) tulee käyttää varoen, koska fluvoksamiini todennäköisesti vähentää näiden lääkkeiden puhdistumaa. Fluvox 100mgamine ei todennäköisesti vaikuta glukuronidaation kautta metaboloituvien bentsodiatsepiinien (esim. loratsepaami, oksatsepaami, tematsepaami) puhdistumaan.
alpratsolaami
Kun fluvoksamiinimaleaattia (100 mg qd) ja alpratsolaamia (1 mg qid) annettiin samanaikaisesti vakaaseen tilaan, alpratsolaamin pitoisuudet plasmassa ja muut farmakokineettiset parametrit (AUC, Cmax, T½) olivat noin kaksi kertaa suuremmat kuin alpratsolaamia yksinään annettaessa; oraalinen puhdistuma pieneni noin 50 %. Kohonneet plasman alpratsolaamipitoisuudet heikensivät psykomotorista suorituskykyä ja muistia. Tämä yhteisvaikutus, jota ei ole tutkittu käyttämällä suurempia fluvoksamiiniannoksia, voi olla selvempi, jos 300 mg:n vuorokausiannos annetaan samanaikaisesti, varsinkin kun fluvox 50 mg:n farmakokinetiikka on epälineaarinen annosalueella 100-300 mg. Jos alpratsolaamia annetaan samanaikaisesti Fluvox 50mgamine Maleate -tablettien kanssa, alpratsolaamin aloitusannos tulee puolittaa ja titraamista pienimpään tehokkaaseen annokseen suositellaan. Fluvox 100mgamine Maleate -tablettien annosta ei tarvitse muuttaa.
Diatsepaami
Fluvoxamine Maleate -tablettien ja diatsepaamin samanaikainen anto ei yleensä ole suositeltavaa. Koska fluvoksamiini vähentää sekä diatsepaamin että sen aktiivisen metaboliitin, Ndesmetyylidiatsepaamin, puhdistumaa, on olemassa suuri todennäköisyys molempien lajien huomattavalle kertymiselle pitkäaikaisen yhteiskäytön aikana.
Todisteet, jotka tukevat sitä johtopäätöstä, että fluvoksamiinin ja diatsepaamin yhteiskäyttöä ei suositella, on saatu tutkimuksesta, jossa terveille vapaaehtoisille, jotka ottivat 150 mg/vrk fluvox 50mgamine -valmistetta, annettiin kerta-annos suun kautta 10 mg diatsepaamia. Näillä koehenkilöillä (N=8) diatsepaamin puhdistuma pieneni 65 % ja N-desmetyylidiatsepaamin puhdistuma tasolle, joka oli liian alhainen mitattavaksi 2 viikkoa kestäneen tutkimuksen aikana.
On todennäköistä, että tämä kokemus aliarvioi merkittävästi kertymisen astetta, jota voi esiintyä toistuvan diatsepaamin antamisen yhteydessä. Lisäksi, kuten alpratsolaamin kohdalla todettiin, fluvox 50mgamine -valmisteen vaikutus voi olla jopa selvempi, kun sitä annetaan suurempina annoksina.
Näin ollen diatsepaamia ja fluvoksamiinia ei tulisi tavallisesti antaa samanaikaisesti.
Klotsapiini
Klotsapiinin seerumipitoisuuksien nousua on raportoitu potilailla, jotka ottavat fluvox 100 mg amiinimaleaattia ja klotsapiinia. Koska klotsapiiniin liittyvät kohtaukset ja ortostaattinen hypotensio näyttävät olevan annosriippuvaisia, näiden haittavaikutusten riski voi olla suurempi, kun fluvoksamiinia ja klotsapiinia annetaan samanaikaisesti. Potilaita tulee seurata tarkasti, kun fluvoksamiinimaleaattia ja klotsapiinia käytetään samanaikaisesti.

Metadoni
Merkittävästi kohonneita metadonin (plasmataso:annos) -suhteita on raportoitu, kun fluvox 50mgamine maleaattia annettiin metadonin ylläpitohoitoa saaville potilaille, joilla oli opioidimyrkytysoireita yhdellä potilaalla. Opioidien vieroitusoireita raportoitiin toisen potilaan fluvoksamiinimaleaattihoidon lopettamisen jälkeen.
Meksiletiini
Vakaan tilan fluvoksamiinin (50 mg kahdesti 7 päivän ajan) vaikutusta meksiletiinin (200 mg) kerta-annoksen farmakokinetiikkaan arvioitiin 6 terveellä japanilaismiehellä. Meksiletiinin puhdistuma pieneni 38 % fluvox 100mgamine -valmisteen samanaikaisen annon jälkeen verrattuna pelkkään meksiletiiniin. Jos fluvoksamiinia ja meksiletiiniä annetaan samanaikaisesti, seerumin meksiletiinipitoisuutta on seurattava.
Ramelteon
Kun fluvoksia 50 mg 100 mg kahdesti vuorokaudessa annettiin 3 päivän ajan ennen kerta-annoksen antamista ramelteonin 16 mg ja fluvoksamiinin kanssa, ramelteonin AUC suureni noin 190-kertaiseksi ja Cmax noin 70-kertaiseksi verrattuna pelkkään ramelteoniin. Ramelteonia ei saa käyttää yhdessä fluvoksamiinin kanssa.
Teofylliini
Vakaan tilan fluvoksi 50 mg (50 mg bid) vaikutus teofylliinin kerta-annoksen (375 mg 442 mg aminofylliininä) farmakokinetiikkaan arvioitiin 12 terveellä tupakoimattomalla, miespuolisella vapaaehtoisella. Teofylliinin puhdistuma pieneni noin 3-kertaiseksi. Siksi, jos teofylliiniä annetaan samanaikaisesti fluvoksamiinimaleaatin kanssa, sen annosta tulee pienentää kolmasosaan tavanomaisesta päivittäisestä ylläpitoannoksesta ja teofylliinin pitoisuutta plasmassa on seurattava. Fluvox 100mgamine Maleate -tablettien annosta ei tarvitse muuttaa.
Varfariini ja muut lääkkeet, jotka häiritsevät hemostaasia (NSAID, aspiriini jne.)
Verihiutaleiden vapauttamalla serotoniinia on tärkeä rooli hemostaasissa. Epidemiologiset tutkimukset tapauskontrollista ja kohorttisuunnittelusta ovat osoittaneet yhteyden serotoniinin takaisinottoa häiritsevien psykotrooppisten lääkkeiden käytön ja ylemmän maha-suolikanavan verenvuodon esiintymisen välillä. Nämä tutkimukset ovat myös osoittaneet, että tulehduskipulääkkeiden tai aspiriinin samanaikainen käyttö voi lisätä tätä verenvuotoriskiä. Siksi potilaita tulee varoittaa tällaisten lääkkeiden käytöstä samanaikaisesti fluvoksamiinin kanssa [ks. VAROITUKSET JA VAROTOIMET ].
Varfariini
Kun fluvoksi 50mgamiinimaleaattia (50 mg tid) annettiin samanaikaisesti varfariinin kanssa kahden viikon ajan, varfariinin plasmapitoisuudet nousivat 98 % ja protrombiiniajat pitkivät. Siksi oraalisia antikoagulantteja ja fluvoksamiinimaleaattitabletteja saavien potilaiden protrombiiniaikaa tulee seurata ja antikoagulanttiannosta muuttaa vastaavasti. Fluvoksamiinimaleaattitablettien annosta ei tarvitse muuttaa.
Fluvox 100mgamine Maleate -tableteilla hoidon lopettaminen
Fluvoksamiinimaleaattitablettien ja muiden SSRI- ja SNRI-lääkkeiden (serotoniinin ja norepinefriinin takaisinoton estäjät) markkinoinnin aikana on raportoitu spontaaneja haittavaikutuksia, jotka ilmenevät näiden lääkkeiden käytön lopettamisen jälkeen, erityisesti äkillisesti, mukaan lukien seuraavat: dysforinen mieliala, ärtyneisyys, kiihtyneisyys, huimaus , aistihäiriöt (esim. parestesiat, kuten sähköiskun tuntemukset), ahdistuneisuus, sekavuus, päänsärky, letargia, emotionaalinen labilisuus, unettomuus ja hypomania. Vaikka nämä tapahtumat ovat yleensä itsestään ohimeneviä, on raportoitu vakavia keskeytysoireita.
Potilaita tulee tarkkailla näiden oireiden varalta, kun he lopettavat Fluvox 50 mg -tablettien käytön. Annoksen asteittaista pienentämistä äkillisen lopettamisen sijaan suositellaan aina kun mahdollista. Jos sietämättömiä oireita ilmaantuu annoksen pienentämisen tai hoidon lopettamisen jälkeen, voidaan harkita jatkamista aiemmin määrätyllä annoksella. Myöhemmin lääkäri voi jatkaa annoksen pienentämistä, mutta asteittain [katso ANNOSTELU JA HALLINNOINTI ].
Epänormaali verenvuoto
SSRI:t ja SNRI:t, mukaan lukien fluvoksamiinimaleaattitabletit, voivat lisätä verenvuototapahtumien riskiä. Aspiriinin, ei-steroidisten tulehduskipulääkkeiden, varfariinin ja muiden antikoagulanttien samanaikainen käyttö voi lisätä tätä riskiä. Tapausraportit ja epidemiologiset tutkimukset (tapauskontrolli ja kohorttisuunnittelu) ovat osoittaneet yhteyden serotoniinin takaisinottoa häiritsevien lääkkeiden käytön ja maha-suolikanavan verenvuodon välillä. SSRI- ja SNRI-lääkkeisiin liittyvät verenvuototapahtumat ovat vaihdelleet mustelmista, hematoomista, nenäverenvuotoista ja petekioista hengenvaarallisiin verenvuotoon.
Potilaita tulee varoittaa verenvuotoriskistä, joka liittyy Fluvox 100mgamine Maleate -tablettien ja tulehduskipulääkkeiden, aspiriinin tai muiden hyytymiseen vaikuttavien lääkkeiden samanaikaiseen käyttöön [ks. VAROITUKSET JA VAROTOIMET ].
Manian/hypomanian aktivointi
Markkinointia edeltävissä tutkimuksissa, joihin osallistui pääasiassa masentuneita potilaita, hypomaniaa tai maniaa esiintyi noin 1 %:lla fluvoksamiinilla hoidetuista potilaista. Kymmenen viikon lasten OCD-tutkimuksessa kahdella 57 fluvoksamiinilla hoidetusta potilaasta (4 %) esiintyi maanisia reaktioita, kun taas ei yksikään 63 lumepotilasta. Manian/hypomanian aktivaatiota on raportoitu myös pienellä osalla potilaista, joilla oli vakava mielialahäiriö ja joita hoidettiin muilla markkinoilla olevilla masennuslääkkeillä. Kuten kaikkia masennuslääkkeitä, Fluvoxamine Maleate -tabletteja tulee käyttää varoen potilailla, joilla on aiemmin ollut mania.
Kohtaukset
Markkinointia edeltävien tutkimusten aikana kouristuskohtauksia raportoitiin 0,2 %:lla fluvoksamiinilla hoidetuista potilaista. Varovaisuutta suositellaan, kun lääkettä annetaan potilaille, joilla on aiemmin esiintynyt kouristuksia. Fluvox 100mgamine -valmistetta tulee välttää potilailla, joilla on epästabiili epilepsia, ja potilaita, joilla on hallinnassa oleva epilepsia, tulee seurata huolellisesti. Fluvoksamiinihoito tulee lopettaa, jos kouristuskohtauksia ilmenee tai jos kohtausten tiheys lisääntyy.
Hyponatremia
Hyponatremiaa voi esiintyä SSRI- ja SNRI-hoidon seurauksena, mukaan lukien fluvoksamiinimaleaattitabletit. Monissa tapauksissa tämä hyponatremia näyttää olevan seurausta sopimattoman antidiureettisen hormonin (SIADH) oireyhtymästä. Tapauksia, joissa seerumin natrium on alle 110 mmol/l, on raportoitu. Iäkkäillä potilailla voi olla suurempi riski kehittää hyponatremia SSRI- ja SNRI-lääkkeiden kanssa [katso Käyttö tietyissä populaatioissa ]. Myös potilailla, jotka käyttävät diureetteja tai joilla on muuten nestevajaus, voi olla suurempi riski. Fluvox 100mgamine Maleate -tablettien käytön lopettamista tulee harkita potilailla, joilla on oireinen hyponatremia, ja asianmukainen lääketieteellinen toimenpide on aloitettava.
Hyponatremian merkkejä ja oireita ovat päänsärky, keskittymisvaikeudet, muistin heikkeneminen, sekavuus, heikkous ja epävakaus, jotka voivat johtaa kaatumiseen. Vakavampiin ja/tai akuutimpiin tapauksiin liittyviä merkkejä ja oireita ovat olleet hallusinaatiot, pyörtyminen, kouristukset, kooma, hengityspysähdys ja kuolema.
Käyttö potilailla, joilla on samanaikainen sairaus
Tarkkaan seurattu kliininen kokemus Fluvox 50mgamine Maleate -tablettien käytöstä potilailla, joilla on samanaikainen systeeminen sairaus, on rajallinen. Varovaisuutta tulee noudattaa annettaessa Fluvoxamine Maleate -tabletteja potilaille, joilla on sairauksia tai tiloja, jotka voivat vaikuttaa hemodynaamisiin vasteisiin tai aineenvaihduntaan.
Fluvoksamiinimaleaattitabletteja ei ole arvioitu tai käytetty merkittävässä määrin potilailla, joilla on äskettäin ollut sydäninfarkti tai epävakaa sydänsairaus. Potilaat, joilla oli tällaisia diagnooseja, suljettiin järjestelmällisesti pois monista kliinisistä tutkimuksista tuotteen markkinointia edeltävän testauksen aikana. Markkinointia edeltäviin tutkimuksiin osallistuneiden masennus- tai OKD-potilaiden elektrokardiogrammien arvioinnissa ei havaittu eroja fluvox 100 mg -valmisteen ja lumelääkkeen välillä kliinisesti tärkeiden EKG-muutosten ilmaantumisen suhteen.
Potilaat, joilla on maksan vajaatoiminta
Maksan vajaatoimintaa sairastavilla potilailla fluvox 50 mg -amiinin puhdistuma pieneni noin 30 %. Maksan vajaatoimintaa sairastavien potilaiden tulee aloittaa pienellä Fluvoxamine Maleate -tablettien annoksella ja suurentaa sitä hitaasti huolellisesti seuraten.
Laboratoriotestit
Erityisiä laboratoriotutkimuksia ei suositella.
Seksuaalinen toimintahäiriö
SSRI-lääkkeiden käyttö, mukaan lukien fluvoksamiinimaleaattitabletit, voi aiheuttaa seksuaalisen toimintahäiriön oireita [ks. HAITTAVAIKUTUKSET 4)]. Miespotilailla SSRI:n käyttö voi johtaa siemensyöksyssä viivästymiseen tai epäonnistumiseen, libidon heikkenemiseen ja erektiohäiriöihin. Naispotilailla SSRI-lääkkeiden käyttö voi heikentää libidoa ja hidastaa orgasmia tai orgasmin puuttumista.
Lääkkeen määrääjien on tärkeää tiedustella seksuaalista toimintaa ennen Fluvoxamine Maleate Tablet -tablettien aloittamista ja tiedustella erityisesti seksuaalitoiminnassa tapahtuvia muutoksia hoidon aikana, koska seksuaalista toimintaa ei välttämättä raportoida spontaanisti. Seksuaalisen toiminnan muutoksia arvioitaessa yksityiskohtainen historia (mukaan lukien oireiden alkamisajankohta) on tärkeää, koska seksuaalisilla oireilla voi olla muita syitä, mukaan lukien taustalla oleva psykiatrinen häiriö. Keskustele mahdollisista hoitostrategioista potilaiden tukemiseksi tekemään tietoisia hoitopäätöksiä.
Potilasneuvontatiedot
Neuvo potilasta lukemaan FDA:n hyväksymä potilasmerkintä ( Lääkitysopas ).
Lääkäreiden tai muiden terveydenhuollon ammattilaisten tulee kertoa potilaille, heidän perheilleen ja heidän hoitajilleen Fluvoxamine Maleate -tablettien hoidon eduista ja riskeistä ja neuvoa heitä asianmukaisessa käytössä. Fluvox 100mgamine Maleate -tableteille on saatavana potilaan lääkitysopas "masennuslääkkeistä, masennuksesta ja muista vakavista mielenterveyssairauksista sekä itsemurha-ajatuksista tai -toimista". Lääkkeen määrääjän tai terveydenhuollon ammattilaisen tulee neuvoa potilaita, heidän perheitään ja hoitajiaan lukemaan lääkitysopas ja auttaa heitä ymmärtämään sen sisältö. Potilaille tulee antaa mahdollisuus keskustella lääkitysoppaan sisällöstä ja saada vastauksia mahdollisiin kysymyksiinsä. Lääkitysoppaan koko teksti on painettu uudelleen tämän asiakirjan lopussa.
Potilaita tulee kertoa seuraavista ongelmista ja pyytää heitä varoittamaan lääkäriään, jos niitä ilmenee Fluvox 100mgamine Maleate -tablettien käytön aikana.
Kliininen paheneminen ja itsemurhariski
Potilaita, heidän perheitään ja heidän omaisiaan tulee kannustaa olemaan valppaana ahdistuneisuuden, kiihtyneisyyden, paniikkikohtausten, unettomuuden, ärtyneisyyden, vihamielisyyden, aggressiivisuuden, impulsiivisuuden, akatisian (psykomotorinen levottomuus), hypomanian, manian ja muiden epätavallisten käyttäytymismuutosten ilmaantuessa. , masennuksen paheneminen ja itsemurha-ajatukset, erityisesti masennuslääkehoidon alkuvaiheessa ja kun annosta muutetaan ylös tai alas. Potilaiden perheitä ja hoitajia tulee neuvoa etsimään tällaisten oireiden ilmaantumista päivittäin, koska muutokset voivat olla äkillisiä. Tällaisista oireista tulee ilmoittaa potilaan lääkkeen määrääjälle tai terveydenhuollon ammattilaiselle, varsinkin jos ne ovat vakavia, alkavat äkillisesti tai eivät kuuluneet potilaan oireisiin. Tällaiset oireet voivat liittyä lisääntyneeseen itsemurha-ajattelun ja -käyttäytymisen riskiin, ja ne osoittavat erittäin tarkan seurannan ja mahdollisesti lääkityksen muuttamisen tarpeen [ks. LAATIKKO VAROITUS , VAROITUKSET JA VAROTOIMET ]
Serotoniinin oireyhtymä
Potilaita tulee varoittaa serotoniinioireyhtymän riskistä erityisesti käytettäessä fluvoksamiinia samanaikaisesti muiden serotonergisten aineiden kanssa (mukaan lukien triptaanit, trisykliset masennuslääkkeet, fentanyyli, litium, tramadoli, tryptofaani, buspironi, amfetamiinit ja mäkikuisma). [katso VAROITUKSET JA VAROTOIMET ].
Kulman sulkeutuva glaukooma
Potilaita tulee kertoa, että Fluvoxamine Maleate -tablettien ottaminen voi aiheuttaa lievää pupillien laajentumista, joka voi herkillä henkilöillä johtaa sulkeutumiskulmaglaukooman episodiin. Aiempi glaukooma on lähes aina avokulmaglaukooma, koska sulkukulmaglaukooma voidaan diagnosoituna hoitaa lopullisesti iridektomialla. Avokulmaglaukooma ei ole kulmaglaukooman riskitekijä. Potilaat saattavat haluta tulla tutkituksi sen määrittämiseksi, ovatko he alttiita kulman sulkemiselle, ja heille voidaan tehdä profylaktinen toimenpide (esim. iridektomia), jos he ovat alttiita [ks. VAROITUKSET JA VAROTOIMET ].
Häiriö kognitiiviseen tai moottorin suorituskykyyn
Koska kaikki psykoaktiiviset lääkkeet voivat heikentää harkintakykyä, ajattelua tai motorisia taitoja, potilaita tulee varoittaa käyttämästä vaarallisia koneita, mukaan lukien autot, kunnes he ovat varmoja siitä, että Fluvox 100mgamine Maleate -tabletit eivät vaikuta haitallisesti heidän kykyynsä osallistua sellaiseen toimintaan.
Raskaus
- Kehota raskaana olevia naisia ilmoittamaan terveydenhuollon tarjoajalleen, jos he tulevat raskaaksi tai aikovat tulla raskaaksi Fluvoxamine Maleate Tablets -hoidon aikana.
- Kerro potilaille, että Fluvoxamine Maleate -tablettien käyttö raskauden loppuvaiheessa saattaa lisätä vastasyntyneiden komplikaatioiden riskiä, jotka vaativat pitkäaikaista sairaalahoitoa, hengitystukea, letkuruokintaa ja/tai vastasyntyneen jatkuvaa keuhkoverenpainetautia (PPHN).
- Kerro naisille, että masennuslääkkeiden käytön lopettamisen yhteydessä on olemassa uusiutumisen riski.
- Kerro naisille, että on olemassa raskausaltistusrekisteri, joka seuraa raskauden tuloksia naisilla, jotka ovat altistuneet fluvoksamiinimaleaattitableteille raskauden aikana [ks. Käyttö tietyissä populaatioissa ].
Imetys
Neuvo imettäville naisille, jotka käyttävät Fluvox 100mgamine Maleate -tabletteja seuraamaan vauvoja ripulin, oksentelun, vähentyneen unen ja kiihtyneisyyden varalta ja hakeutumaan lääkärin hoitoon, jos he huomaavat näitä merkkejä [ks. Käyttö tietyissä populaatioissa ].
Samanaikainen lääkitys
Potilaita tulee neuvoa ilmoittamaan lääkärilleen, jos he käyttävät tai aikovat ottaa resepti- tai käsikauppalääkkeitä, koska Fluvox 50mgamine Maleate -tablettien kanssa on mahdollista kliinisesti merkittäviä yhteisvaikutuksia.
Potilaita tulee varoittaa fluvoksamiinin ja tulehduskipulääkkeiden, aspiriinin tai muiden hyytymiseen vaikuttavien lääkkeiden samanaikaisesta käytöstä, koska serotoniinin takaisinottoa häiritsevien psykotrooppisten lääkkeiden yhteiskäyttö on yhdistetty lisääntyneeseen verenvuotoriskiin [ks. VAROITUKSET JA VAROTOIMET ].
Koska fluvoksamiinia ja titsanidiinia käytetään yhdessä, vakavien haittavaikutusten riski, mukaan lukien vakava verenpaineen lasku ja sedaatio, voi lisääntyä, fluvox 50mgamine -valmistetta ei tule käyttää titsanidiinin kanssa [ks. VAROITUKSET JA VAROTOIMET ].
Koska fluvoksamiinia ja alosetronia käytetään yhdessä, vakavien haittavaikutusten riski voi lisääntyä, fluvox 50mgamine -valmistetta ei tule käyttää LotronexTM:n (alosetroni) kanssa [ks. VAROITUKSET JA VAROTOIMET ].
Seksuaalinen toimintahäiriö
Kerro potilaille, että Fluvox 50mgamine Maleate -tablettien käyttö voi aiheuttaa seksuaalisen toimintahäiriön oireita sekä mies- että naispotilailla. Kerro potilaille, että heidän tulee keskustella kaikista seksuaalisen toiminnan muutoksista ja mahdollisista hoitostrategioista terveydenhuollon tarjoajan kanssa [katso VAROITUKSET JA VAROTOIMET ].
Alkoholi
Kuten muitakin psykotrooppisia lääkkeitä käytettäessä, potilaita tulee neuvoa välttämään alkoholin käyttöä Fluvox 50mgamine Maleate -tablettien käytön aikana.
Allergiset reaktiot
Potilaita tulee neuvoa ilmoittamaan lääkärilleen, jos heille ilmaantuu ihottumaa, nokkosihottumaa tai siihen liittyvää allergista ilmiötä Fluvoxamine Maleate Tablets -hoidon aikana.
Kaikki luetellut tuotenimet ovat omistajiensa rekisteröityjä tavaramerkkejä, eivätkä ne ole ANI Pharmaceuticals, Inc:n tavaramerkkejä.
Ei-kliininen toksikologia
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Karsinogeneesi
Syöpää aiheuttavia vaikutuksia ei havaittu rotilla, joita hoidettiin suun kautta fluvoksamiinimaleaatilla 30 kuukauden ajan, tai hamstereissa, joita hoidettiin suun kautta fluvoksi 50 mg amiinimaleaatilla 20 (naaraat) tai 26 (urokset) kuukauden ajan. Näissä tutkimuksissa suuria annoksia saaneiden ryhmien päivittäisiä annoksia nostettiin tutkimuksen aikana vähintään 160 mg/kg:sta maksimiarvoon 240 mg/kg rotilla ja vähintään 135 mg/kg:sta maksimiarvoon. 240 mg/kg hamstereissa. Enimmäisannos 240 mg/kg on noin 5-kertainen (hamstereille ja rotille) kuusi kertaa lapsille annettu MRHD mg/m²:n perusteella.
Mutageneesi
Genotoksisesta mahdollisuudesta ei havaittu näyttöä hiiren mikrotumatestissä, in vitro kromosomipoikkeavuustestissä tai Amesin mikrobimutageenitestissä metabolisen aktivaation kanssa tai ilman sitä.
Hedelmällisyyden heikkeneminen
Tutkimuksessa, jossa uros- ja naarasrotille annettiin fluvox 100 mg/kg (60, 120 tai 240 mg/kg) ennen parittelua ja raskauden aikana sekä niiden aikana, hedelmällisyys heikkeni oraalisilla 120 mg/kg:n annoksilla (3 kertaa MRHD:lle annettu). nuorilla mg/m²) tai enemmän, mikä on osoituksena lisääntyneestä parittelulatenssista, vähentyneestä siittiöiden määrästä, vähentyneestä lisäkiveksen painosta ja vähentyneestä raskauden määrästä. Lisäksi implantaatioiden ja alkioiden määrä väheni suurimmalla annoksella (6 kertaa nuorten MRHD mg/m² perusteella). Vaikuton annos hedelmällisyyden heikkenemiseen oli 60 mg/kg (1,6 kertaa nuorille annettu MRHD mg/m²-perusteisesti).
Käyttö tietyissä populaatioissa
Raskaus
Raskausaltistusrekisteri
On olemassa raskausaltistusrekisteri, joka seuraa raskauden tuloksia naisilla, jotka ovat altistuneet masennuslääkkeille raskauden aikana. Terveydenhuollon tarjoajia kehotetaan rekisteröimään potilaita soittamalla National Pregnancy Registry for Antidepressants numeroon 1-844-405-6185 tai käymällä verkossa osoitteessa https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/antidepressants/.
Riskien yhteenveto
Pitkäaikainen kokemus fluvox 100mgamine -valmisteesta raskaana oleville naisille vuosikymmeniä, julkaistujen havainnointitutkimusten perusteella, ei ole osoittanut selkeää lääkkeeseen liittyvää vakavien synnynnäisten epämuodostumien tai keskenmenon riskiä (ks. Data ). On olemassa riskejä, jotka liittyvät hoitamattomaan masennukseen raskauden aikana, ja riskejä, jotka liittyvät vastasyntyneen jatkuvaan keuhkoverenpaineeseen (PPHN) ja vastasyntyneen huonoon sopeutumiseen, jos raskauden aikana altistuu selektiivisille serotoniinin takaisinoton estäjille (SSRI), mukaan lukien fluvoksamiini (ks. Kliiniset näkökohdat ).
Kun tiineitä rottia hoidettiin suun kautta fluvoksamiinilla koko organogeneesin ajan, havaittiin lisääntynyttä alkiosikiökuolemaa ja lisääntynyttä sikiön silmäpoikkeavuuksien (laskostunut verkkokalvo) esiintyvyyttä annoksilla, jotka olivat ≥ 3 kertaa ihmisille suositeltujen enimmäisannosten (MRHD) 300 mg/vrk. nuorille mg/m² perusteella. Lisäksi sikiön painon laskua havaittiin annoksella, joka oli 6-kertainen nuorille annettuun MRHD-annokseen verrattuna mg/m²:n perusteella. Ei havaittu haitallisia kehitysvaikutuksia kaneissa, joita hoidettiin fluvoksamiinilla organogeneesin aikana annoksella, joka oli 2 kertaa nuorille annettu MRHD mg/m²:n perusteella. Kun fluvox 50mgamine -valmistetta annettiin rotille suun kautta tiineyden ja imetyksen aikana, lisääntynyt poikaskuolleisuus syntyessään havaittiin annoksella, joka oli 2 kertaa nuorille annettu MRHD mg/m²:n perusteella. Lisäksi pentujen painon ja eloonjäämisen alenemista havaittiin annoksilla, jotka ovat ≥ 0,13 kertaa nuorille annettu MRHD (ks. Data ).
Vakavien synnynnäisten epämuodostumien ja keskenmenon arvioitu taustariski ilmoitetulle väestölle ei ole tiedossa. Kaikilla raskauksilla on taustalla riski synnynnäisistä epämuodostumista, menetyksestä tai muista haitallisista seurauksista. Yhdysvaltain väestössä vakavien synnynnäisten epämuodostumien ja keskenmenon arvioitu taustariski kliinisesti tunnistetuissa raskauksissa on 2-4 % ja 15-20 %.
Kliiniset näkökohdat
Äidin ja/tai alkion/sikiön sairauteen liittyvä riski
Naiset, jotka lopettavat masennuslääkkeiden käytön raskauden aikana, kokevat todennäköisemmin vakavan masennuksen uusiutumisen kuin naiset, jotka jatkavat masennuslääkkeiden käyttöä. Tämä havainto on prospektiivisesta pitkittäistutkimuksesta, jossa seurattiin 201 raskaana olevaa naista, joilla oli aiemmin ollut vakava masennushäiriö ja jotka olivat eutymia ja käyttivät masennuslääkkeitä raskauden alussa. Ota huomioon hoitamattoman masennuksen riski, kun lopetat tai vaihdat masennuslääkehoitoa raskauden ja synnytyksen aikana.
Sikiön/vastasyntyneen haittavaikutukset
Vastasyntyneille, jotka ovat altistuneet fluvoksamiinimaleaattitableteille ja muille SSRI- tai SNRI-lääkkeille kolmannen raskauskolmanneksen lopussa, on kehittynyt komplikaatioita, jotka vaativat pitkäaikaista sairaalahoitoa, hengitystukea ja letkuruokintaa. Tällaiset komplikaatiot voivat ilmaantua heti synnytyksen jälkeen. Raportoituja kliinisiä löydöksiä ovat olleet hengitysvaikeudet, syanoosi, apnea, kohtaukset, lämpötilan epävakaus, ruokintavaikeudet, oksentelu, hypoglykemia, hypotonia, hypertonia, hyperrefleksia, vapina, hermostuneisuus, ärtyneisyys ja jatkuva itku. Nämä ominaisuudet ovat yhdenmukaisia joko SSRI- ja SNRI-lääkkeiden suoran toksisen vaikutuksen kanssa tai mahdollisesti lääkkeen käytön lopetusoireyhtymän kanssa. On huomattava, että joissakin tapauksissa kliininen kuva on yhdenmukainen serotoniinioireyhtymän kanssa [katso VAROITUKSET JA VAROTOIMET ].
Data
Ihmistiedot
Altistuminen SSRI-lääkkeille raskauden loppuvaiheessa saattaa lisätä vastasyntyneen keuhkoverenpainetaudin (PPHN) riskiä. PPHN:tä esiintyy 1-2:lla 1000 elävänä syntynyttä kohden väestössä, ja siihen liittyy huomattava vastasyntyneiden sairastuvuus ja kuolleisuus.
Eläinten tiedot
Kun tiineille rotille annettiin suun kautta 100 mg fluvox-annoksia (60, 120 tai 240 mg/kg) koko organogeneesin ajan, havaittiin kehitystoksisuutta lisääntyneen alkiosikiökuoleman muodossa ja lisääntyneen sikiön silmän poikkeavuuksien (laskostuneet verkkokalvot) ilmaantuvuuden muodossa annokset 120 mg/kg tai suuremmat (3 kertaa MRHD 300 mg/vrk, annettuna nuorille mg/m²-pohjaisesti). Sikiön painon laskua havaittiin suurella annoksella 240 mg/kg/vrk (6 kertaa nuorille annettu MRHD mg/m²:n perusteella). Vaikutukseton annos kehitystoksisuuteen tässä tutkimuksessa oli 60 mg/kg/vrk (1,6 kertaa nuorille annettu MRHD mg/m²:n perusteella).
Tutkimuksessa, jossa tiineille kaneille annettiin jopa 40 mg/kg annoksia (noin 2,1 kertaa nuorille annettu MRHD mg/m²:n perusteella) organogeneesin aikana, ei havaittu haitallisia vaikutuksia alkion ja sikiön kehitykseen.
Muissa lisääntymistutkimuksissa, joissa naarasrotille annettiin suun kautta tiineyden ja imetyksen aikana (5, 20, 80 tai 160 mg/kg), lisääntynyt poikaskuolleisuus syntymähetkellä havaittiin annoksilla 80 mg/kg/vrk (2 kertaa MRHD). annettiin nuorille mg/m²:n perusteella) tai enemmän, ja poikasten painon ja eloonjäämisen alenemista havaittiin kaikilla annoksilla (alhainen vaikutus annos, noin 0,13 kertaa nuorille annettu MRHD mg/m²-pohjalta laskettuna).
Imetys
Julkaistun kirjallisuuden tiedot kertovat, että fluvoksamiinia on äidinmaidossa (ks Data ). Mitään haitallisia vaikutuksia imetettävään lapseen ei ole raportoitu useimmissa tapauksissa, joissa äiti on käyttänyt fluvox 50mgamine -valmistetta imetyksen aikana. On kuitenkin raportoitu ripulia, oksentelua, heikentynyttä unta ja levottomuutta (ks. Kliiniset näkökohdat ). Fluvox 100mgamine -valmisteen vaikutuksesta maidontuotantoon ei ole tietoa. Imetyksen kehitys- ja terveyshyödyt tulee ottaa huomioon äidin kliinisen fluvox 50mgamine -tarpeen ja fluvoksamiinin tai äidin taustalla olevan sairauden mahdollisten haitallisten vaikutusten kanssa imetettävään lapseen.
Kliiniset näkökohdat
Tarkkaile rintamaidon kautta fluvoksamiinille altistuneita imeväisiä ripulin, oksentelun, unen heikkenemisen ja levottomuuden varalta.
Data
Maidon lääkeainepitoisuudet olivat ≤ 425 ng/ml, kun äidille oli annettu fluvox 100mgamine 25 mg/vrk - 300 mg/vrk julkaistuissa tapausraporteissa ja tapaussarjoissa.
Naaraat ja urokset, joilla on lisääntymispotentiaali
Hedelmättömyys
Eläinlöydökset viittaavat siihen, että hedelmällisyys voi heikentyä fluvox 50mgamine -hoidon aikana [ks. Ei-kliininen toksikologia ].
Käyttö lapsille
Fluvox 100mgamine maleaatin teho pakko-oireisen häiriön hoidossa osoitettiin 10 viikkoa kestäneessä plasebokontrolloidussa monikeskustutkimuksessa, johon osallistui 120 8–17-vuotiasta avopotilasta. Lisäksi 99 näistä avopotilaista jatkoi avointa fluvoksamiinimaleaattihoitoa vielä yhdestä kolmeen vuotta, mikä vastaa 94 potilasvuotta. Tässä tutkimuksessa havaittu haittavaikutusprofiili oli yleensä samanlainen kuin aikuisilla fluvoksamiinilla tehdyissä tutkimuksissa [katso HAITTAVAIKUTUKSET , ANNOSTELU JA HALLINNOINTI ].
Fluvoksamiinin ja muiden SSRI-lääkkeiden käytön yhteydessä on havaittu vähentynyttä ruokahalua ja painon laskua. Tästä syystä painon ja kasvun säännöllistä seurantaa suositellaan, jos lapsen SSRI-hoitoa jatketaan pitkään.
Mahdollisia riskejä, jotka voivat liittyä fluvox 50mgamine -valmisteen pitkäaikaiseen käyttöön lapsilla ja nuorilla, joilla on OCD, ei ole arvioitu systemaattisesti. Lääkkeen määrääjän tulee muistaa, että todisteet, joihin vedottiin pääteltäessä, että fluvoksamiini on turvallinen lapsille ja nuorille, perustuvat suhteellisen lyhytaikaisiin kliinisiin tutkimuksiin ja aikuispotilailla saatujen kokemusten ekstrapoloimiseen. Erityisesti ei ole olemassa tutkimuksia, jotka arvioivat suoraan fluvoksamiinin pitkäaikaisen käytön vaikutuksia lasten ja nuorten kasvuun, kognitiiviseen käyttäytymiseen ja kypsymiseen. Vaikka ei ole olemassa myönteistä havaintoa, joka viittaa siihen, että fluvoksamiinilla on kyky vaikuttaa haitallisesti kasvuun, kehitykseen tai kypsymiseen, tällaisten löydösten puuttuminen ei ole vakuuttava todiste siitä, että fluvoksamiinilla ei olisi haitallisia vaikutuksia pitkäaikaisessa käytössä [ks. VAROITUKSET JA VAROTOIMET ].
Turvallisuutta ja tehokkuutta muilla lapsipotilailla kuin OCD-potilailla ei ole varmistettu [katso LAATIKKO VAROITUS ; VAROITUKSET JA VAROTOIMET ]. Jokaisen, joka harkitsee Fluvox 100mgamine Maleate -tablettien käyttöä lapsella tai nuorella, on tasapainotettava mahdolliset riskit kliinisen tarpeen kanssa.
Geriatrinen käyttö
Noin 230 potilasta, jotka osallistuivat kontrolloituihin fluvoksamiinimaleaattitablettien markkinointia edeltäviin tutkimuksiin, oli 65-vuotiaita tai vanhempia. Näiden potilaiden ja nuorempien potilaiden välillä ei havaittu yleisiä eroja turvallisuudessa. Muut raportoidut kliiniset kokemukset eivät ole osoittaneet eroja iäkkäiden ja nuorempien potilaiden vasteessa. SSRI:t ja SNRI:t, mukaan lukien fluvoksamiinimaleaattitabletit, on kuitenkin yhdistetty useisiin kliinisesti merkittävään hyponatremiatapauksiin iäkkäillä potilailla, joilla saattaa olla suurempi riski saada tämä haittatapahtuma [ks. VAROITUKSET JA VAROTOIMET ]. Lisäksi fluvoksamiinin puhdistuma on pienentynyt noin 50 % vanhuksilla verrattuna nuorempiin potilaisiin [ks. KLIININEN FARMAKOLOGIA ], ja joidenkin vanhempien henkilöiden suurempaa herkkyyttä ei myöskään voida sulkea pois. Sen vuoksi pienempää aloitusannosta tulee harkita iäkkäillä potilailla, ja Fluvox 50mgamine Maleate -tabletteja tulee titrata hitaasti hoidon alussa.
YLIANNOSTUS
Seuraavia on raportoitu fluvox 100mgamine -tabletin yliannostuksen yhteydessä:
- Kohtaukset, jotka voivat viivästyä, ja muuttunut henkinen tila mukaan lukien kooma.
- Kardiovaskulaarinen toksisuus, joka voi viivästyä, mukaan lukien QRS- ja QTc-ajan pidentyminen. Hypertensio on yleisimmin havaittu, mutta harvoin hypotensiota voi esiintyä yksinään tai samanaikaisesti alkoholin kanssa.
- Serotoniinioireyhtymä (potilailla, jotka ovat saaneet useita lääkkeitä yliannostuksen muiden pro-serotonergisten lääkkeiden kanssa, voi olla suurempi riski).
Ruoansulatuskanavan dekontaminaatiota aktiivihiilellä tulee harkita potilailla, jotka ilmaantuvat varhain fluvoksamiinin yliannostuksen jälkeen.
Harkitse ottamista yhteyttä myrkytyskeskukseen (1-800-221-2222) tai lääketieteelliseen toksikologiin yliannostuksen hallintasuosituksia varten.
VASTA-AIHEET
Yhteishallinto
Titsanidiinin, tioridatsiinin, alosetronin tai pimotsidin samanaikainen anto Fluvox 50mgamine Maleate -tablettien kanssa on vasta-aiheista [ks. VAROITUKSET JA VAROTOIMET ].
Serotoniinioireyhtymä ja monoamiinioksidaasin estäjät (MAOI)
MAO-estäjien käyttö psykiatristen häiriöiden hoitoon Fluvoxamine Maleate Tablets -tableteilla tai 14 päivän sisällä Fluvoxamine Maleate Tablet -hoidon lopettamisesta on vasta-aiheista, koska se lisää serotoniinioireyhtymän riskiä. Fluvox 50mgamine Maleate -tablettien käyttö 14 päivän sisällä psykiatristen häiriöiden hoitoon tarkoitetun MAO-estäjän käytön lopettamisesta on myös vasta-aiheista [ks. ANNOSTELU JA HALLINNOINTI , VAROITUKSET JA VAROTOIMET ].
Fluvoksamiinimaleaattitablettien aloittaminen potilaalla, jota hoidetaan MAO-estäjillä, kuten linetsolidilla tai suonensisäisellä metyleenisinisellä, on myös vasta-aiheista, koska serotoniinioireyhtymän riski on lisääntynyt [ks. ANNOSTELU JA HALLINNOINTI , VAROITUKSET JA VAROTOIMET ].
KLIININEN FARMAKOLOGIA
Toimintamekanismi
Fluvox 50mgamine maleaatin vaikutusmekanismin pakko-oireisessa häiriössä oletetaan liittyvän sen spesifiseen serotoniinin takaisinoton estoon aivojen hermosoluissa. Fluvox 100mgamine -valmisteen on osoitettu olevan tehokas serotoniinin takaisinoton kuljettajan estäjä prekliinisissä tutkimuksissa sekä in vitro että in vivo.
Farmakodynamiikka
In vitro -tutkimuksissa fluvoksi 100 mg amiinimaleaatilla ei ollut merkittävää affiniteettia histaminergisiin, alfa- tai beeta-adrenergisiin, muskariini- tai dopaminergisiin reseptoreihin. Joidenkin näistä reseptoreista antagonismin uskotaan liittyvän joidenkin psykotrooppisten lääkkeiden erilaisiin rauhoittaviin, kardiovaskulaarisiin, antikolinergisiin ja ekstrapyramidaalisiin vaikutuksiin.
Farmakokinetiikka
Imeytyminen
Fluvoksamiinimaleaatin absoluuttinen hyötyosuus on 53 %. Ruoka ei vaikuta merkittävästi oraaliseen biologiseen hyötyosuuteen.
Annossuhteellisuustutkimuksessa, jossa fluvoksamiinimaleaattia annettiin 100, 200 ja 300 mg/vrk 10 peräkkäisenä päivänä 30 normaalilla vapaaehtoisella, vakaa tila saavutettiin noin viikon annostelun jälkeen. Vakaan tilan huippupitoisuudet plasmassa saavutettiin 3–8 tunnin kuluessa annostelusta ja saavuttivat pitoisuudet, jotka olivat keskimäärin 88, 283 ja 546 ng/ml. Siten fluvoksamiinilla oli epälineaarinen farmakokinetiikka tällä annosalueella, eli suuremmat fluvox 100mgamine -maleaattiannokset tuottivat suhteettoman korkeampia pitoisuuksia kuin pienemmällä annoksella ennustettiin.
Jakelu
Fluvoksamiinin keskimääräinen näennäinen jakautumistilavuus on noin 25 l/kg, mikä viittaa laajaan kudosten jakautumiseen.
Noin 80 % fluvox 100mgamiinista sitoutuu plasman proteiineihin, enimmäkseen albumiiniin, pitoisuusalueella 20-2000 ng/ml.
Aineenvaihdunta
Fluvox 100mgamine maleaatti metaboloituu laajalti maksassa; pääasialliset aineenvaihduntareitit ovat oksidatiivinen demetylaatio ja deaminaatio. Yhdeksän metaboliittia tunnistettiin radioaktiivisesti leimatun fluvox 100 mg -maleaatin 5 mg:n annoksen jälkeen, ja ne muodostivat noin 85 % fluvox 100 mg -amiinin virtsaan erittyneistä tuotteista. Ihmisen päämetaboliitti oli fluvoksin 100 mg amiinihappo, joka yhdessä N-asetyloidun analoginsa kanssa vastasi noin 60 % virtsaan erittyneistä tuotteista. Kolmannen metaboliitin, fluvoksetanolin, muodostui oksidatiivisella deaminaatiolla, osuus oli noin 10 %. Fluvox 100 mg amiinihappoa ja fluvox 100 mg etanolia testattiin serotoniinin ja norepinefriinin takaisinoton eston in vitro -määrityksessä rotilla; ne olivat inaktiivisia lukuun ottamatta entisen metaboliitin heikkoa vaikutusta serotoniinin oton estoon (1-2 suuruusluokkaa vähemmän tehokasta kuin lähtöaine). Noin 2 % fluvox 100mgamiinista erittyi virtsaan muuttumattomana [ks. HUUMEIDEN VUOROVAIKUTUKSET ].
Eliminointi
14C-leimatun oraalisen fluvox 50mgamine -maleaatin (5 mg) annoksen jälkeen keskimäärin 94 % lääkkeeseen liittyvistä tuotteista löytyi virtsasta 71 tunnin kuluessa.
Fluvox 100 mg:n keskimääräinen puoliintumisaika plasmassa vakaassa tilassa toistuvien 100 mg:n vuorokausiannosten suun kautta terveillä nuorilla vapaaehtoisilla oli 15,6 tuntia.
Vanhukset
Fluvoksamiinimaleaattitablettien 50 ja 100 mg:n tutkimuksessa, jossa verrattiin iäkkäitä (66–73-vuotiaita) ja nuoria (19–35-vuotiaita) potilaita, keskimääräiset huippupitoisuudet plasmassa olivat vanhuksilla 40 % korkeammat. Fluvoksi 50 mg:n toistuvan annoksen eliminaation puoliintumisaika oli 17,4 ja 25,9 tuntia vanhuksilla verrattuna 13,6 ja 15,6 tuntiin nuorilla vakaassa tilassa 50 ja 100 mg:n annoksilla. Iäkkäillä potilailla fluvox 100mgamine -valmisteen puhdistuma pieneni noin 50 %, ja siksi Fluvox 100mgamine Maleate -tabletteja tulee titrata hitaasti hoidon aloittamisen aikana [ks. ANNOSTELU JA HALLINNOINTI ].
Pediatriset aiheet
Fluvox 50 mg -valmisteen toistuvan annoksen farmakokinetiikka määritettiin mies- ja naislapsilla (6-11-vuotiaat) ja nuorilla (12-17-vuotiaat). Vakaan tilan plasman fluvox 100mgamine -pitoisuudet olivat 2-3 kertaa korkeammat lapsilla kuin nuorilla. Lapsilla AUC ja Cmax olivat 1,5–2,7 kertaa suuremmat kuin nuorilla. (Katso taulukko 4.) Kuten aikuisilla, sekä lapsilla että nuorilla esiintyi epälineaarista toistuvan annoksen farmakokinetiikkaa. Naislasten AUC (0-12) ja Cmax oli merkittävästi korkeampi kuin mieslapsilla, ja siksi pienemmät fluvoksamiinimaleaattitablettien annokset voivat tuottaa terapeuttista hyötyä. (Katso taulukko 5.) Sukupuolten välisiä eroja ei havaittu nuorilla. Vakaan tilan plasman fluvoksamiinipitoisuudet olivat samankaltaisia aikuisilla ja nuorilla annoksella 300 mg/vrk, mikä osoittaa, että fluvoksiini 100 mg amiinialtistus oli samanlainen näissä kahdessa populaatiossa. (Katso taulukko 4.) Annoksen muuttaminen nuorilla (aikuisen enimmäisannokseen 300 mg asti) voi olla aiheellista terapeuttisen hyödyn saavuttamiseksi [ks. ANNOSTELU JA HALLINNOINTI ].
TAULUKKO 4: FLUVOX 50mgAMINE FARMAKOKINEETTISTEN KESKIMÄÄRIEN (SD) VERTAILU LASTEN, NUORTEN JA AIKUISTEN VÄLILLÄ
TAULUKKO 5: FLUVOX 50mgAMINE FARMAKOKINEETTISTEN PARAMETTERIEN VERTAILU MIES- JA NAISLASTEN (6-11 VUOTIA) VÄLILLÄ
Maksa- ja munuaissairaudet
Ristiintutkimusten vertailu (terveet koehenkilöt vs. potilaat, joilla on maksan vajaatoiminta) viittasi fluvox 50mgamine -puhdistuman vähenemiseen 30 % maksan toimintahäiriön yhteydessä. Keskimääräiset vähimmäispitoisuudet plasmassa munuaisten vajaatoimintapotilailla (kreatiniinipuhdistuma 5-45 ml/min) 4 ja 6 viikon hoidon jälkeen (50 mg kahdesti, N = 13) olivat keskenään vertailukelpoisia, mikä viittaa siihen, ettei fluvoksamiinia kertynyt näille potilaille. [katso VAROITUKSET JA VAROTOIMET ].
Kliiniset tutkimukset
Aikuisten OCD-tutkimukset
Fluvoksamiinimaleaattitablettien tehokkuus pakko-oireisen häiriön (OCD) hoidossa osoitettiin kahdessa 10 viikkoa kestäneessä monikeskustutkimuksessa, rinnakkaisryhmätutkimuksessa aikuispotilailla. Näissä tutkimuksissa potilaat titrattiin fluvoxin 50 mg maleaatin päivittäiseen kokonaisannokseen 150 mg/vrk tutkimuksen kahden ensimmäisen viikon aikana, minkä jälkeen annosta säädettiin 100-300 mg/vrk (hintatarjousaikataulun mukaan) , vasteen ja suvaitsevaisuuden perusteella. Näissä tutkimuksissa potilailla oli kohtalainen tai vaikea OCD (DSM-III-R), joiden keskimääräinen lähtötaso oli Yale-Brown Obsessive Compulsive -asteikolla (Y-BOCS), kokonaispistemäärä 23. Fluvox 50 mg amiinimaleaattia saaneiden potilaiden keskimääräinen väheneminen oli noin 4-5 yksikköä Y-BOCS-kokonaispisteissä verrattuna 2 yksikön vähennykseen lumepotilailla.
Taulukossa 6 on tulosluokittelu hoitoryhmittäin CGI (Clinical Global Impressions) -asteikon Global Improvement -kohdassa molemmille tutkimuksille yhdistettynä.
TAULUKKO 6: TULOSLUOKITTELU (%) CGI-GLOBAALISTA PARANNUSKOHTEESTA KAHDEN AIKUISTEN OCD-TUTKIMUKSEN SUORITTAJILLE
Tutkimusanalyysit iän ja sukupuolen vaikutuksista tuloksiin eivät osoittaneet iän tai sukupuolen perusteella eroavaa vastetta.
Aikuisten OCD-ylläpitotutkimus
Ylläpitotutkimuksessa aikuisilla avohoitopotilailla, joilla oli OKD, 114 potilasta, jotka täyttivät OCD:n DSM-IV-kriteerit ja joiden Yale-Brown Obsessive Compulsive Scale (Y-BOCS) -pistemäärä oli ≥18, titrattiin tehokkaaksi annokseksi fluvoksamiinimaleaattitabletteja 100–300 mg. /vrk osana ensimmäistä 10 viikon yksisokkohoitovaihetta. Hoitovaste tässä yksisokkovaiheessa määriteltiin Y-BOCS-pisteiksi, jotka olivat vähintään 30 % lähtötasoa alhaisemmat viikkojen 8 ja 10 lopussa. Potilaista, jotka vastasivat, heidän vasteen kesto oli keskimäärin 4 viikkoa. Potilaat, jotka reagoivat tämän alkuvaiheen aikana, satunnaistettiin joko jatkamaan Fluvox 50mgamine Maleate -tablettien käyttöä (N = 56) tai saamaan lumelääkettä (N = 58) kaksoissokkoutetussa vaiheessa uusiutumisen havainnointia varten. Relapsi kaksoissokkovaiheen aikana määriteltiin vähintään 30 %:n nousuksi Y-BOCS-pisteissä yli kyseisen vaiheen lähtötilanteen tai potilaan kieltäytymisenä jatkaa hoitoa OCD-oireiden huomattavan lisääntymisen vuoksi. Kaksoissokkovaiheessa potilailla, jotka saivat jatkuvaa fluvoksamiinimaleaattitablettihoitoa, todettiin keskimäärin merkittävästi pienempi uusiutumisaste kuin lumelääkettä saaneilla.
Tämän tutkimuksen väestöalaryhmien tarkastelu ei paljastanut mitään selkeitä todisteita iän tai sukupuolen perusteella erilaisesta ylläpitovaikutuksesta.
Lasten OCD-tutkimus
Fluvoxamine Maleate -tablettien tehokkuus OCD:n hoidossa osoitettiin myös 10 viikkoa kestäneessä monikeskustutkimuksessa, rinnakkaisryhmätutkimuksessa lasten avohoidossa (8–17-vuotiaat lapset ja nuoret). Tämän tutkimuksen potilaat titrattiin päivittäiseen fluvox 100 mg -amiinin kokonaisannokseen, joka oli noin 100 mg/vrk tutkimuksen kahden ensimmäisen viikon aikana, minkä jälkeen annosta säädettiin välillä 50-200 mg/vrk (hintatarjouksen mukaan). reagoinnin ja suvaitsevaisuuden perusteella. Kaikilla potilailla oli keskivaikea tai vaikea OKD (DSM-III-R), joiden keskimääräinen lähtötaso oli lasten Yale-Brown Obsessive Compulsive Scale (CY-BOCS) -kokonaispistemäärällä 24. Fluvox 100 mg gamiinimaleaattia saaneiden potilaiden keskimääräinen lasku aleni. noin kuusi yksikköä CY-BOCS-kokonaispisteissä verrattuna kolmen yksikön vähennykseen lumelääkepotilailla.
Taulukossa 7 on tulosluokittelu hoitoryhmittäin CGI (Clinical Global Impression) -asteikon Global Improvement -kohdassa lapsitutkimuksessa.
TAULUKKO 7: TULOSLUOKITTELU (%) CGI-GLOBAALISTA PARANNUSKOHTEESTA PEDIATRIAN TUTKIMUKSEN SUORITTAJILLE
Post hoc -tutkimukset sukupuolen vaikutuksista tuloksiin eivät osoittaneet erilaista reagointikykyä sukupuolen perusteella. Lisätutkimukset osoittivat huomattavan hoitovaikutuksen 8–11-vuotiaiden ikäryhmässä ja käytännössä ei vaikutusta 12–17-vuotiaiden ikäryhmässä. Vaikka näiden tulosten merkitys ei ole selvä, 2-3 kertaa korkeammat vakaan tilan plasman fluvoksamiinipitoisuudet lapsilla verrattuna nuoriin [ks. KLIININEN FARMAKOLOGIA ] viittaa siihen, että pienentynyt altistus nuorilla on saattanut olla tekijä, ja annoksen muuttaminen nuorilla (aikuisen enimmäisannokseen 300 mg asti) saattaa olla aiheellista terapeuttisen hyödyn saavuttamiseksi.
POTILASTIEDOT
Fluvox 100mgamiini (Flu VOX ah meen) Maleaattitabletit
Lue Fluvox 100mgamine Maleate -tablettien mukana tuleva lääkitysopas ennen kuin aloitat sen käytön ja aina, kun saat täyttöä. Saattaa tulla uutta tietoa. Tämä lääkitysopas ei korvaa terveydenhuollon tarjoajan kanssa puhumista terveydentilastasi tai hoidostasi. Keskustele terveydenhuollon tarjoajan kanssa, jos et ymmärrä jotain tai haluat oppia lisää.
Mikä on tärkein tieto, joka minun pitäisi tietää Fluvox 50mgamine Maleate -tableteista?
Fluvoksamiini on samanlainen lääke kuin masennuksen hoitoon käytettävä lääke, ja se voi aiheuttaa vakavia sivuvaikutuksia, kuten:
1. Itsetuhoiset ajatukset tai teot:
- Fluvoxamine Maleate -tabletit ja masennuslääkkeet voivat lisätä itsemurha-ajatuksia tai -toimia joillakin lapsilla, nuorilla tai nuorilla aikuisilla hoidon ensimmäisten kuukausien aikana tai annosta muuttaessa.
- Masennus tai muut vakavat mielenterveysongelmat ovat tärkeimmät syyt itsemurha-ajatuksiin tai -toimiin.
- Tarkkaile näitä muutoksia ja soita heti terveydenhuollon tarjoajallesi, jos huomaat:
- Uudet tai äkilliset muutokset mielialassa, käyttäytymisessä, toimissa, ajatuksissa tai tunteissa, varsinkin jos ne ovat vakavia.
- Kiinnitä erityistä huomiota tällaisiin muutoksiin, kun Fluvox 100mgamine Maleate -tabletteja aloitetaan tai annosta muutetaan.
Pidä kaikki seurantakäynnit terveydenhuollon tarjoajan kanssa ja soita käyntien välillä, jos olet huolissasi oireista.
Soita välittömästi terveydenhuollon tarjoajallesi, jos sinulla on jokin seuraavista oireista, tai soita hätänumeroon, varsinkin jos ne ovat uusia, pahempia tai huolestuttavia:
- yrittää itsemurhaa
- vaarallisten impulssien vaikutuksesta
- käyttäytyy aggressiivisesti tai väkivaltaisesti
- ajatuksia itsemurhasta tai kuolemasta
- uusi tai pahempi masennus
- uusia tai pahempia ahdistuneisuus- tai paniikkikohtauksia
- kiihtyneisyys, levottomuus, vihaisuus tai ärtyneisyys
- nukahtamisvaikeuksia
- aktiivisuuden lisääntyminen tai puhuminen enemmän kuin sinulle on normaalia
- muita epätavallisia muutoksia käyttäytymisessä tai mielialassa
Kerro heti terveydenhuollon tarjoajallesi, jos sinulla on jokin seuraavista oireista, tai soita hätänumeroon. Fluvoksamiinimaleaattitablettien käyttöön saattaa liittyä näitä vakavia sivuvaikutuksia:
2. Serotoniinioireyhtymä: Tämä tila voi olla hengenvaarallinen ja voi sisältää:
- kiihtyneisyys, hallusinaatiot, kooma tai muut mielentilan muutokset
- koordinaatiohäiriöt tai lihasnykitykset (yliaktiiviset refleksit)
- syke, korkea tai matala verenpaine
- hikoilu tai kuume
- pahoinvointia, oksentelua tai ripulia
- lihasten jäykkyys
3. Visuaaliset ongelmat
- silmän kipu
- muutoksia näkökyvyssä
- turvotus tai punoitus silmässä tai sen ympärillä
Vain jotkut ihmiset ovat vaarassa saada nämä ongelmat. Haluat ehkä käydä silmätutkimuksessa nähdäksesi, oletko vaarassa, ja saada ehkäisevää hoitoa, jos olet.
4. Vakavat allergiset reaktiot:
- vaikeuksia hengittää
- kasvojen, kielen, silmien tai suun turvotus
- ihottuma, kutisevat nokkosihottumat tai rakkulat yksinään tai kuumeen tai nivelkipujen kanssa
5. Epänormaali verenvuoto: Fluvox 100mgamine Maleate -tabletit ja masennuslääkkeet voivat lisätä verenvuodon tai mustelmien riskiä, varsinkin jos käytät verta ohentavaa varfariinia (Coumadin®, Jantoven®) tai ei-steroidista tulehduskipulääkettä (NSAID:t, kuten ibuprofeeni, naprokseeni tai aspiriini).
6. Kohtaukset tai kouristukset
7. Maaniset jaksot:
- lisääntynyt huomattavasti energiaa
- vakavia unihäiriöitä
- kilpailevia ajatuksia
- huolimaton käytös
- epätavallisen mahtavia ideoita
- liiallinen onnellisuus tai ärtyneisyys
- puhua enemmän tai nopeammin kuin tavallisesti
8. Muutokset ruokahalussa tai painossa. Lasten ja nuorten pituutta ja painoa tulee seurata hoidon aikana.
9. Alhaiset suola- (natrium-) tasot veressä. Iäkkäät ihmiset voivat olla alttiimpia tälle. Oireita voivat olla:
- päänsärky
- heikkous tai epävakaus
- sekavuus, keskittymis- tai ajattelu- tai muistiongelmat
10. Seksuaaliset ongelmat (häiriöt). Selektiivisten serotoniinin takaisinoton estäjien (SSRI) käyttö, mukaan lukien Fluvox 50mgamine Maleate -tabletit, voi aiheuttaa seksuaalisia ongelmia.
- Miehillä oireita voivat olla:
- Viivästynyt siemensyöksy tai kyvyttömyys saada siemensyöksyä
- Vähentynyt seksihalu
- Ongelmia saada tai säilyttää erektio
- Naisilla oireita voivat olla:
- Vähentynyt seksihalu
- Viivästynyt orgasmi tai kyvyttömyys saada orgasmi
Keskustele terveydenhuollon tarjoajan kanssa, jos sinulla on muutoksia seksuaalisessa toiminnassasi tai jos sinulla on kysyttävää tai huolenaiheita seksuaalisista ongelmista Fluvox 50mgamine Maleate Tablets -hoidon aikana. Terveydenhuollon tarjoajasi voi ehdottaa hoitoja.
Älä lopeta Fluvoxamine Maleate -tabletteja keskustelematta ensin terveydenhuollon tarjoajan kanssa.
Fluvoxamine Maleate -tablettien lopettaminen liian nopeasti voi aiheuttaa vakavia oireita, kuten:
- ahdistuneisuus, ärtyneisyys, korkea tai huono mieliala, levottomuus tai muutokset nukkumistottumuksissa
- päänsärky, hikoilu, pahoinvointi, huimaus
- sähköiskun kaltaiset tuntemukset, vapina, sekavuus
Mitä Fluvoxamine Maleate -tabletit ovat?
Fluvoksamiinimaleaattitabletit ovat reseptilääke, jota käytetään pakko-oireisen häiriön (OCD) hoitoon. On tärkeää keskustella terveydenhuollon tarjoajan kanssa OCD:n hoidon riskeistä ja myös riskeistä, jos sitä ei hoideta. Sinun tulee keskustella kaikista hoitovaihtoehdoista terveydenhuollon tarjoajan kanssa.
Keskustele terveydenhuollon tarjoajan kanssa, jos et usko, että tilasi paranee Fluvox 100mgamine Maleate Tablets -hoidon myötä.
Kuka ei saa ottaa Fluvox 100mgamine Maleate -tabletteja?
Älä ota Fluvoxamine Maleate -tabletteja, jos:
- olet allerginen fluvox 50mgamine -maleaatille tai jollekin Fluvoxamine Maleate -tablettien aineosalle. Katso tämän lääkitysoppaan lopusta täydellinen luettelo Fluvox 50mgamine Maleate -tablettien ainesosista.
- ota monoamiinioksidaasin estäjää (MAOI). Kysy terveydenhuollon tarjoajalta tai apteekista, jos et ole varma, käytätkö MAO-estäjää, mukaan lukien antibiootti linetsolidi.
- Älä ota MAO:n estäjää 2 viikon sisällä Fluvoxamine Maleate Tablet -tablettien lopettamisesta, ellei lääkärisi kehota tekemään niin.
- Älä aloita Fluvox 50mgamine Maleate -tablettien käyttöä, jos olet lopettanut MAO:n estäjän käytön viimeisen 2 viikon aikana, ellei lääkärisi ole niin määrännyt.
Ihmisillä, jotka ottavat Fluvoxamine Maleate Tablets -tabletteja lähellä MAO-estäjän käyttöä, voi olla vakavia tai jopa hengenvaarallisia sivuvaikutuksia. Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin näistä oireista:
-
- korkea kuume
- hallitsemattomat lihasspasmit
- jäykät lihakset
- nopeat sydämen sykkeen tai verenpaineen muutokset
- hämmennystä
- tajunnan menetys (pyörtyminen)
- ota Mellaril® (tioridatsiini). Älä ota Mellaril®-valmistetta 2 viikon kuluessa Fluvox 50mgamine Maleate -tablettien käytön lopettamisesta, koska se voi aiheuttaa vakavia sydämen rytmihäiriöitä tai äkillisen kuoleman.
- ota Orap® (pimotsidi), koska tämän lääkkeen ottaminen Fluvox 50mgamine Maleate -tablettien kanssa voi aiheuttaa vakavia sydämen rytmihäiriöitä tai äkillisen kuoleman.
- ota Zanaflex® (tisanidiini). Fluvoxamine Maleate -tabletit voivat lisätä Zanaflexin määrää kehossasi, mikä voi lisätä sen vaikutuksia ja sivuvaikutuksia. Tämä voi sisältää uneliaisuutta ja verenpaineen laskua ja vaikuttaa siihen, kuinka hyvin teet asioita, jotka vaativat valppautta.
- Ota Lotronex® (alosetroni). Fluvox 50mgamine maleaattitabletit voivat lisätä Lotronexin määrää kehossasi, mikä voi lisätä sen vaikutuksia ja sivuvaikutuksia.
Mitä minun pitäisi kertoa terveydenhuollon tarjoajalleni ennen Fluvox 50mgamine Maleate -tablettien ottamista? Kysy, jos et ole varma.
Ennen kuin aloitat Fluvoxamine Maleate -tablettien käytön, kerro terveydenhuollon tarjoajallesi, jos:
- Käytätkö tiettyjä lääkkeitä, kuten:
- Monoamiinioksidaasin estäjät (MAO:t), kuten Emsam® (selegiliini), Nardil® (feneltsiini) tai Parnate® (tranyylisypromiini)
- Mellaril® (tioridatsiini): käytetään mielenterveyden tai mielialaongelmien hoitoon
- Zanaflex® (tizanidiini): käytetään spastisuuden (tila, jossa lihakset kiristyvät ja kouristuvat) hoitoon
- Orap® (pimotsidi): käytetään Touretten oireyhtymän (aivosairaus, joka aiheuttaa tics) hoitoon
- Lotronex® (alosetroni): käytetään ripulin, jatkuvan vatsakivun, kouristuksen ja turvotuksen hoitoon
- Triptaanit: käytetään migreenipäänsäryn hoitoon
- Lääkkeet, joita käytetään mielialan, ahdistuneisuuden, psykoottisten tai ajatushäiriöiden hoitoon, mukaan lukien trisykliset lääkkeet, litium, SSRI:t, SNRI:t tai psykoosilääkkeet
- Tramadoli: käytetään vähentämään kipua
- Bentsodiatsepiinit: käytetään vähentämään ahdistusta, stressiä, emotionaalisia häiriöitä tai kohtauksia; auttaa nukahtamaan; auttaa alkoholin vieroitushoidossa; vähentää levottomuutta; ja rentouttaa lihaksia
- Metadoni: käytetään lievittämään kipua tai auttamaan riippuvuudessa
- Klotsapiini: käytetään mielenterveyshäiriöiden hoitoon
- Meksiletiini: käytetään sydämen rytmihäiriöiden hoitoon
- Teofylliini: käytetään keuhkojen turvonneiden ilmakanavien hoitoon, rintakehän lihasten rentouttamiseen hengenahdistuksen lievittämiseksi, usein astman hoitoon
- Varfariini ja muut lääkkeet, jotka vaikuttavat veren hyytymiseen
- Diureetit korkean verenpaineen, sydämen vajaatoiminnan tai turvotuksen hoitoon
- Reseptivapaat lisäravinteet, kuten tryptofaani tai mäkikuisma
- sinulla on maksaongelmia
- on munuaisongelmia
- on sydänongelmia
- sinulla on tai on ollut kohtauksia tai kouristuksia
- sinulla on kaksisuuntainen mielialahäiriö tai mania
- sinulla on alhainen natriumpitoisuus veressäsi
- sinulla on ollut aivohalvaus
- on korkea verenpaine
- sinulla on tai on ollut verenvuotoongelmia
- olet raskaana tai suunnittelet raskautta. Keskustele terveydenhuollon tarjoajan kanssa sikiölle aiheutuvista riskeistä, jos otat Fluvox 50mgamine Maleate -tabletteja.
- Keskustele terveydenhuollon tarjoajan kanssa OCD: n hoidon hyödyistä ja riskeistä raskauden aikana.
- Jos tulet raskaaksi Fluvox 50mgamine Maleate Tablets -hoidon aikana, keskustele terveydenhuollon tarjoajasi kanssa rekisteröitymisestä National Pregnancy Registry for masennuslääkkeisiin. Voit ilmoittautua soittamalla numeroon 1-844-405-6185.
- imetät tai aiot imettää. Fluvoxamine Maleate -tabletit erittyvät äidinmaitoon. Keskustele terveydenhuollon tarjoajan kanssa parhaasta tavasta ruokkia vauva, kun käytät Fluvox 50mgamine Maleate -tabletteja.
Kerro terveydenhuollon tarjoajallesi kaikista käyttämistäsi lääkkeistä, mukaan lukien reseptilääkkeet ja ilman reseptiä saatavat lääkkeet, vitamiinit ja yrttilisät. Fluvoxamine Maleate -tabletit ja jotkin lääkkeet voivat olla vuorovaikutuksessa keskenään, ne eivät ehkä toimi yhtä hyvin tai voivat aiheuttaa vakavia sivuvaikutuksia.
Terveydenhuollon tarjoaja tai apteekkihenkilökunta voi kertoa sinulle, onko Fluvoxamine Maleate -tablettien ottaminen muiden lääkkeiden kanssa turvallista. Älä aloita tai lopeta mitään lääkettä Fluvoxamine Maleate -tablettien käytön aikana keskustelematta ensin terveydenhuollon tarjoajan kanssa.
Jos käytät Fluvox 100mgamine Maleate -tabletteja, älä käytä muita fluvoksamiinia sisältäviä lääkkeitä, mukaan lukien: LUVOX 50mg CR®
Kuinka minun pitäisi ottaa Fluvoxamine Maleate -tabletteja?
- Ota Fluvoxamine Maleate -tabletit juuri niin kuin on määrätty. Terveydenhuollon tarjoajasi saattaa joutua muuttamaan Fluvox 100mgamine Maleate -tablettien annosta, kunnes se on oikea annos sinulle.
- Fluvox 100mgamine Maleate -tabletit voidaan ottaa ruoan kanssa tai ilman ruokaa.
- Jos unohdat ottaa Fluvoxamine Maleate -tabletteja, ota unohtunut annos heti kun muistat. Jos on melkein seuraavan annoksen aika, jätä unohtunut annos väliin ja ota seuraava annos tavalliseen aikaan. Älä ota kahta annosta Fluvox 100mgamine Maleate -tabletteja samanaikaisesti.
- Jos otat liikaa Fluvox 50mgamine Maleate -tabletteja, soita välittömästi terveydenhuollon tarjoajalle tai myrkytystietokeskukseen tai hakeudu ensiapuun.
Mitä minun tulisi välttää käyttäessäni Fluvox 50mgamine Maleate -tabletteja?
Fluvox 100mgamine Maleate -tabletit voivat aiheuttaa uneliaisuutta tai vaikuttaa kykyysi tehdä päätöksiä, ajatella selkeästi tai reagoida nopeasti. Älä aja, käytä raskaita koneita tai tee muuta vaarallista toimintaa, ennen kuin tiedät, kuinka Fluvoxamine Maleate Tablets vaikuttaa sinuun. Älä juo alkoholia käyttäessäsi Fluvoxamine Maleate -tabletteja.
Mitkä ovat Fluvox 100mgamine Maleate -tablettien mahdolliset sivuvaikutukset?
- Fluvoksamiinimaleaattitabletit voivat aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- Katso "Mikä on tärkein tieto, joka minun pitäisi tietää Fluvox 100mgamine Maleate -tableteista?"
Ahdistusta tai unihäiriöitä
Yleisiä mahdollisia sivuvaikutuksia ihmisillä, jotka käyttävät Fluvox 100mgamine Maleate -tabletteja, ovat:
- pahoinvointi
- uneliaisuus
- heikkous
- ruoansulatushäiriöt
- hikoilu
- ruokahalun menetys
- vapina
- oksentelua
- viivästynyt siemensyöksy
- kyvyttömyys saada orgasmia
- vähentynyt seksihalu
- kuiva suu
- tukkoinen nenä
- epätavallinen maku
- toistuva virtsaaminen
Muita sivuvaikutuksia lapsille ja nuorille ovat:
- levottomuutta tai epänormaalia aktiivisuuden lisääntymistä
- masentunut tai surullinen olo
- liikaa kaasua
- raskaat kuukautiset
- ihottuma
- mahdollinen hidastunut kasvunopeus ja painonmuutos.
Kerro terveydenhuollon tarjoajallesi, jos sinulla on jokin haittavaikutus, joka häiritsee sinua tai joka ei katoa. Nämä eivät ole kaikkia Fluvox 50mgamine Maleate -tablettien mahdollisia sivuvaikutuksia. Lisätietoja saat terveydenhuollon tarjoajalta tai apteekista.
Soita Lääkärillesi HAITTAVAIKUTUKSIIN LIITTYVÄN LÄÄKETIETEELLISEN NEUVON saamiseksi. VOI ILMOITTAA HAITTAVAIKUTUKSISTA numerossa 1-800-308-6755 tai FDA:ssa numerossa 1-800-FDA-1088
Kuinka minun pitäisi säilyttää Fluvox 50mgamine Maleate -tabletteja?
Säilytä fluvoksamiinimaleaattitabletit huoneenlämmössä 59 ° F - 86 ° F (15 ° C - 30 ° C).
- Pidä Fluvoxamine Maleate -tabletit poissa korkeasta kosteudesta.
- Pidä Fluvoxamine Maleate Tablets -pullo tiiviisti suljettuna.
Pidä Fluvoxamine Maleate -tabletit ja kaikki lääkkeet poissa lasten ulottuvilta.
Yleistä tietoa Fluvox 100mgamine Maleate -tableteista
Lääkkeitä määrätään joskus muihin kuin lääkitysoppaassa lueteltuihin tarkoituksiin. Älä käytä Fluvoxamine Maleate -tabletteja sairauteen, johon sitä ei ole määrätty. Älä anna Fluvox 100mgamine Maleate -tabletteja muille ihmisille, vaikka heillä olisi sama sairaus. Se voi vahingoittaa heitä.
Tämä lääkitysopas sisältää yhteenvedon tärkeimmistä tiedoista fluvoksamiinimaleaattitableteista. Jos haluat lisätietoja, keskustele terveydenhuollon tarjoajasi kanssa. Voit pyytää terveydenhuollon tarjoajalta tai apteekista tietoja Fluvoxamine Maleate -tableteista, jotka on kirjoitettu terveydenhuollon ammattilaisille.
Lisätietoja Fluvox 50mgamine Maleate -tableteista saat soittamalla maksuttomaan numeroon 1-800-308-6755 tai siirtymällä osoitteeseen www.anipharmaceuticals.com.
Mitkä ovat Fluvoxamine Maleate -tablettien ainesosat?
Vaikuttava aine: Fluvoksamiinimaleaatti
Inaktiiviset ainesosat:
25 mg:n tabletit: karnaubavaha, hypromelloosi, mannitoli, polyetyleeniglykoli, polysorbaatti 80, esigelatinoitu tärkkelys (peruna), piidioksidi, natriumstearyylifumaraatti, tärkkelys (maissi) ja titaanidioksidi.
50 mg ja 100 mg tabletit: sisältävät edellä mainittujen inaktiivisten aineosien lisäksi synteettisiä rautaoksideja.
Tämän lääkitysoppaan on hyväksynyt Yhdysvaltain elintarvike- ja lääkevirasto.
