Ventolin Inhaler 100mcg Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Ventolin on ja miten sitä käytetään?
Ventolin HFA on reseptilääke, jota käytetään akuutin tai vaikean tai rasituksen aiheuttaman astman (bronkospasmin) oireiden hoitoon. Ventolin HFA:ta voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Ventolin HFA kuuluu lääkeluokkaan, jota kutsutaan beta2-agonisteiksi.
Ei tiedetä, onko Ventolin HFA turvallinen ja tehokas alle 4-vuotiaille lapsille.
Mitkä ovat Ventolinin mahdolliset sivuvaikutukset?
Ventolin voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- hengityksen vinkuminen,
- tukehtuminen,
- hengitysongelmia,
- rintakipu,
- nopea syke,
- sykkivät sydämenlyönnit,
- lepattaa rinnassasi,
- kova päänsärky,
- hakkaa niskassasi tai korvissasi,
- kipua tai polttamista virtsatessa,
- lisääntynyt jano,
- lisääntynyt virtsaaminen,
- kuiva suu,
- hedelmäinen hengityksen tuoksu,
- jalkakrampit,
- ummetus
- epäsäännölliset sydämenlyönnit,
- tunnottomuus tai pistely,
- lihasheikkous ja
- veltto tunne
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Ventolinin yleisimpiä sivuvaikutuksia ovat:
- rintakipu,
- nopeat tai jyskyttävät sydämenlyönnit,
- huimaus,
- tärisevä olo,
- hermostuneisuus,
- päänsärky,
- selkäkipu,
- kehon kivut,
- ärtynyt vatsa,
- kipeä kurkku,
- poskiontelokipu ja
- vuotava tai tukkoinen nenä
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Ventolinin mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
VENTOLIN HFA:n aktiivinen komponentti on albuterolisulfaatti, USP, albuterolin raseeminen muoto ja suhteellisen selektiivinen beeta-adrenerginen keuhkoputkia laajentava aine. Albuterolisulfaatin kemiallinen nimi on α1 - [(tert-butyyliamino)metyyli]-4-hydroksi-m-ksyleeni-α, α'-diolisulfaatti (2:1) (suola) ja seuraava kemiallinen rakenne:
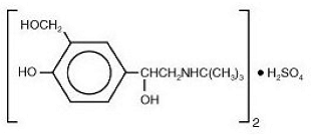
Albuterolisulfaatti on valkoinen kiteinen jauhe, jonka molekyylipaino on 576,7, ja empiirinen kaava on (C13H21NO3)2•H2SO4. Se liukenee veteen ja liukenee hieman etanoliin.
Maailman terveysjärjestön suosittelema nimi albuteroliemäkselle on salbutamoli.
VENTOLIN HFA on sininen muovinen inhalaattori, jossa on sininen nauhakorkki, joka sisältää paineistetun mitatun aerosolisäiliön, jossa on laskuri. Jokainen säiliö sisältää albuterolisulfaatin mikrokiteisen suspension ponneaineessa HFA-134a (1,1,1,2-tetrafluorietaani). Se ei sisällä muita apuaineita.
Esikäsittelyn jälkeen jokainen inhalaattorin käyttö antaa venttiilistä 120 mikrogrammaa albuterolisulfaattia USP 75 mg:ssa suspensiota ja 108 mikrogrammaa albuterolisulfaattia, USP suukappaleesta (vastaa 90 mikrogrammaa albuteroliemästä suukappaleesta).
Valmistele VENTOLIN HFA ennen ensimmäistä käyttöä, kun inhalaattoria ei ole käytetty yli 2 viikkoon tai kun inhalaattori on pudonnut. Pohjustaaksesi VENTOLIN HFA:ta, päästä 4 suihketta ilmaan pois kasvoilta ja ravista hyvin ennen jokaista suihketta.
INDIKAATIOT
Bronkospasmi
VENTOLIN® HFA -inhalaatioaerosoli on tarkoitettu bronkospasmin hoitoon tai ehkäisyyn vähintään 4-vuotiailla potilailla, joilla on palautuva obstruktiivinen hengitystiesairaus.
Harjoituksen aiheuttama bronkospasmi
VENTOLIN HFA on tarkoitettu rasituksen aiheuttaman bronkospasmin ehkäisyyn 4-vuotiaille ja sitä vanhemmille potilaille.
ANNOSTELU JA HALLINNOINTI
Bronkospasmi
Akuuttien bronkospasmin hoitoon tai bronkospasmiin liittyvien oireiden ehkäisyyn tavallinen annos aikuisille ja lapsille on 2 inhalaatiota 4–6 tunnin välein. Joillekin potilaille 1 inhalaatio 4 tunnin välein voi olla riittävä. Useampaa antoa tai useampaa inhalaatiomäärää ei suositella.
Harjoituksen aiheuttama bronkospasmi
Rasituksen aiheuttaman bronkospasmin ehkäisyssä tavallinen annos aikuisille ja 4-vuotiaille ja sitä vanhemmille lapsille on 2 inhalaatiota 15-30 minuuttia ennen harjoittelua.
Hallintotiedot
VENTOLIN HFA tulee antaa vain suun kautta hengitettynä.
Pohjustus
VENTOLIN HFA:n esitäyttö on välttämätöntä, jotta varmistetaan sopiva albuterolipitoisuus jokaisessa painalluksessa. Valmistele VENTOLIN HFA ennen ensimmäistä käyttöä, kun inhalaattoria ei ole käytetty yli 2 viikkoon tai kun inhalaattori on pudonnut. VENTOLIN HFA:n pohjustamiseksi levitä 4 suihketta ilmaan pois kasvoilta ja ravista hyvin ennen jokaista suihketta.
Puhdistus
Oikean annostelun varmistamiseksi ja toimilaitteen aukkojen tukkeutumisen estämiseksi pese toimilaite lämpimällä vedellä ja anna sen ilmakuivua kokonaan vähintään kerran viikossa.
MITEN TOIMITETAAN
Annostusmuodot ja vahvuudet
Hengitys Aerosoli. Sininen muovinen inhalaattori, jossa on sininen nauhakorkki, joka sisältää paineistetun mitatun annoksen aerosolisäiliön, joka sisältää 60 tai 200 mitattua inhalaatiota ja jossa on laskuri. Jokainen painallus vapauttaa 108 mikrogrammaa albuterolisulfaattia (90 mikrogrammaa albuteroliemästä) suukappaleesta.
Varastointi ja käsittely
VENTOLIN HFA Inhalaatioaerosoli toimitetaan seuraavissa laatikoissa 1 paineistetussa alumiinikapselissa, jossa on laskuri ja jossa on sininen muovinen toimilaite, jossa on sininen hihna:
NDC 0173-0682-20 18 g:n kanisteri, joka sisältää 200 painallusta NDC 0173-0682-21 8 g kanisteri, joka sisältää 60 painallusta NDC 0173-0682-24 8 g:n laitospakkaus, joka sisältää 60 toimintoa
Jokainen inhalaattori on suljettu kosteudelta suojaavaan foliopussiin, jossa on kuivausaine, joka tulee hävittää, kun pussi avataan. Jokaiseen inhalaattoriin on pakattu potilastietolehtinen.
VENTOLIN HFA:n mukana toimitettua sinistä toimilaitetta ei saa käyttää muiden tuotesäiliöiden kanssa, eikä muiden tuotteiden toimilaitteita saa käyttää VENTOLIN HFA -kapselin kanssa.
VENTOLIN HFA:ssa on kanisteriin kiinnitetty laskuri. Laskuri alkaa 204:stä tai 64:stä ja laskee alas aina, kun suihke vapautetaan. Oikeaa lääkemäärää jokaisella painalluksella ei voida taata sen jälkeen, kun laskuri on lukenut 000, vaikka säiliö ei ole täysin tyhjä ja jatkaa toimintaansa. Inhalaattori tulee hävittää, kun laskuri on 000 tai 12 kuukautta kosteutta suojaavasta kalvopussista poistamisen jälkeen sen mukaan, kumpi tulee ensin.
Pitää poissa lasten ulottuvilta. Vältä roiskumista silmiin.
Sisältö paineen alaisena: Älä puhkaise. Älä käytä tai säilytä lämmön tai avotulen lähellä. Altistuminen yli 120 °F:n lämpötiloille voi aiheuttaa halkeamia. Älä koskaan heitä kanisteria tuleen tai polttouuniin.
Säilytä huoneenlämmössä 68°F - 77°F (20°C - 25°C); retket sallitaan 59°F - 86°F (15°C - 30°C) [Katso USP-ohjattu huonelämpötila ]. Säilytä inhalaattoria suukappale alaspäin. Parhaan tuloksen saavuttamiseksi inhalaattorin tulee olla huoneenlämpöinen ennen käyttöä. RAVISTA HYVIN ENNEN JOKAISTA SUUTETTA.
GlaxoSmithKline, Research Triangle Park, NC 27709. Tarkistettu: joulukuu 2014
SIVUVAIKUTUKSET
VENTOLIN HFA:n käyttö voi liittyä seuraaviin:
- Paradoksaalinen bronkospasmi [katso VAROITUKSET JA VAROTOIMET ]
- Sydän- ja verisuonivaikutukset [katso VAROITUKSET JA VAROTOIMET ]
- Välittömät yliherkkyysreaktiot [ks VAROITUKSET JA VAROTOIMET ]
- Hypokalemia [katso VAROITUKSET JA VAROTOIMET ]
Kokemus kliinisistä kokeista
Koska kliiniset tutkimukset suoritetaan hyvin vaihtelevissa olosuhteissa, lääkkeen kliinisissä tutkimuksissa havaittuja haittavaikutuksia ei voida suoraan verrata toisen lääkkeen kliinisissä tutkimuksissa havaittuihin nopeuksiin, eivätkä ne välttämättä kuvasta käytännössä havaittuja nopeuksia.
Alla kuvatut turvallisuustiedot heijastavat altistusta VENTOLIN HFA:lle 248 VENTOLIN HFA:lla hoidetussa potilaassa kolmessa lumekontrolloidussa kliinisessä tutkimuksessa, jotka kestivät 2–12 viikkoa. Aikuisten ja nuorten tiedot perustuvat kahteen kliiniseen tutkimukseen, joissa 202 astmaa sairastavaa 12-vuotiasta ja sitä vanhempia saivat VENTOLIN HFA:ta 2 inhalaatiolla 4 kertaa päivässä 12 viikon ajan. Aikuisten/nuorten väestöstä oli 92 naista, 110 miestä ja 163 valkoista, 19 mustaa, 18 latinalaisamerikkalaista ja 2 muuta. Lapsipotilaiden tiedot perustuvat yhteen kliiniseen tutkimukseen, jossa 46 astmapotilasta iältään 4–11 vuotta hoidettiin VENTOLIN HFA:lla 2 inhalaatiolla 4 kertaa päivässä 2 viikon ajan. Väestö oli 21 naista, 25 miestä ja 25 valkoista, 17 mustaa, 3 latinalaisamerikkalaista ja 1 muu.
12-vuotiaat ja sitä vanhemmat aikuiset ja nuoret: Kahdessa 12 viikon satunnaistetussa kaksoissokkotutkimuksessa 610 astmaa sairastavalla aikuisella ja nuorella koehenkilöllä verrattiin VENTOLIN HFA:ta, CFC 11/12 -moottorilla toimivaa albuteroliinhalaattoria ja HFA-134a lumelääkeinhalaattoria. Kaiken kaikkiaan VENTOLIN HFA:n ja CFC 11/12 -käyttöisen albuteroli-inhalaattorin haittavaikutusten ilmaantuvuus ja luonne olivat vertailukelpoisia. Taulukossa 1 on lueteltu kaikkien näiden tutkimusten haittavaikutusten ilmaantuvuus (riippumatta siitä, onko tutkija katsonut lääkkeeseen liittyviksi tai ei-liittymättömiksi), joita esiintyi vähintään 3 % VENTOLIN HFA:lla hoidetussa ryhmässä ja useammin hoidetussa ryhmässä. VENTOLIN HFA:lla kuin HFA-134a lumelääkeinhalaattoriryhmässä.
Alle 3 %:lla VENTOLIN HFA:ta saaneista aikuisista ja nuorista potilaista ja suuremmasta osasta VENTOLIN HFA:ta saaneista henkilöistä kuin HFA-134a lumelääkeinhalaattoria saaneista raportoituja haittavaikutuksia, jotka voivat liittyä VENTOLIN HFA:han, ovat ripuli, kurkunpäätulehdus, suun ja nielun turvotus, yskä, keuhkosairaudet, takykardia ja ekstrasystolat. Sydämentykytys ja huimaus on havaittu myös VENTOLIN HFA:n käytön yhteydessä.
4–11-vuotiaat lapsipotilaat: Kaksi viikkoa kestäneen kliinisen tutkimuksen tulokset 4–11-vuotiailla astmaa sairastavilla lapsilla osoittivat, että tällä lapsiryhmällä oli samanlainen haittavaikutusprofiili kuin aikuisilla ja nuorilla.
VENTOLIN HFA:n turvallisuuden ja tehon arvioimiseksi on suoritettu kolme tutkimusta syntymä- ja 4-vuotiailla koehenkilöillä. Näiden tutkimusten tulokset eivät vahvistaneet VENTOLIN HFA:n tehoa tässä ikäryhmässä [ks. Käyttö tietyissä populaatioissa ]. Koska VENTOLIN HFA:n tehoa ei ole osoitettu syntymän ja 48 kuukauden ikäisten lasten hoidossa, VENTOLIN HFA:n turvallisuutta tässä ikäryhmässä ei voida vahvistaa. Alle 4-vuotiailla lapsipotilailla havaittu turvallisuusprofiili oli kuitenkin verrattavissa vanhemmilla lapsipotilailla sekä aikuisilla ja nuorilla havaittuun turvallisuusprofiiliin. Kun haittavaikutusten ilmaantuvuus oli suurempi alle 4-vuotiailla koehenkilöillä verrattuna vanhempiin, suurempi ilmaantuvuus havaittiin kaikissa hoitoryhmissä, lumelääke mukaan lukien. Näitä haittavaikutuksia olivat ylempien hengitysteiden infektio, nenänielutulehdus, kuume ja takykardia.
Markkinoinnin jälkeinen kokemus
Kliinisissä tutkimuksissa raportoitujen haittavaikutusten lisäksi seuraavat haittavaikutukset on tunnistettu albuterolisulfaatin hyväksymisen jälkeisen käytön aikana. Koska nämä reaktiot on raportoitu vapaaehtoisesti epävarman kokoisesta populaatiosta, ei ole aina mahdollista luotettavasti arvioida niiden esiintymistiheyttä tai määrittää syy-yhteyttä lääkkeelle altistumiseen. Nämä tapahtumat on valittu sisällytettäviksi joko niiden vakavuuden, ilmoitustiheyden tai syy-yhteyden albuteroliin tai näiden tekijöiden yhdistelmän vuoksi.
VENTOLIN HFA:n käytön jälkeen on raportoitu paradoksaalisia bronkospasmia, käheyttä, rytmihäiriöitä (mukaan lukien eteisvärinä, supraventrikulaarinen takykardia) ja yliherkkyysreaktioita (mukaan lukien nokkosihottuma, angioödeema, ihottuma).
Lisäksi albuteroli, kuten muut sympatomimeettiset aineet, voi aiheuttaa haittavaikutuksia, kuten hypokalemiaa, kohonnutta verenpainetta, perifeeristä vasodilataatiota, angina pectoria, vapinaa, keskushermoston stimulaatiota, hyperaktiivisuutta, unettomuutta, päänsärkyä, lihaskrampit, suun nielun kuivumista tai ärsytystä ja aineenvaihduntaa. asidoosi.
HUUMEIDEN VUOROVAIKUTUKSET
Muita lyhytvaikutteisia sympatomimeettisiä aerosolikeuhkoputkia laajentavia aineita ei tule käyttää samanaikaisesti albuterolin kanssa. Jos muita adrenergisiä lääkkeitä annetaan jollakin tavalla, niitä tulee käyttää varoen, jotta vältetään haitalliset sydän- ja verisuonivaikutukset.
Beeta-adrenergisiä reseptoreja salpaavat aineet
Beetasalpaajat eivät ainoastaan estä beeta-agonistien, kuten VENTOLIN HFA:n, keuhkovaikutusta, vaan ne voivat myös aiheuttaa vaikeaa bronkospasmia astmapotilailla. Siksi astmapotilaita ei normaalisti tule hoitaa beetasalpaajilla. Tietyissä olosuhteissa näille potilaille ei kuitenkaan välttämättä ole hyväksyttäviä vaihtoehtoja beetasalpaajien käytölle. kardioselektiivisiä beetasalpaajia voidaan harkita, vaikka niitä tuleekin antaa varoen.
Kaliumia säästämättömät diureetit
Beeta-agonistit voivat pahentaa äkillisesti EKG-muutoksia ja/tai hypokalemiaa, jotka voivat johtua kaliumia säästämättömien diureettien (kuten loop- tai tiatsididiureettien) antamisesta, etenkin jos beeta-agonistin suositeltu annos ylittyy. Vaikka näiden vaikutusten kliinistä merkitystä ei tunneta, varovaisuutta tulee noudattaa käytettäessä VENTOLIN HFA:ta samanaikaisesti kaliumia säästämättömien diureettien kanssa.
Digoksiini
Seerumin digoksiinipitoisuudet laskivat keskimäärin 16–22 %, kun albuterolia annettiin kerta-annoksena laskimoon ja suun kautta normaaleille vapaaehtoisille, jotka olivat saaneet digoksiinia 10 päivän ajan. Näiden löydösten kliininen merkitys potilaille, joilla on obstruktiivinen hengitystiesairaus ja jotka saavat kroonisesti inhaloitavaa albuterolia ja digoksiinia, on epäselvä. Siitä huolimatta olisi järkevää arvioida huolellisesti seerumin digoksiinitasot potilailla, jotka saavat parhaillaan digoksiinia ja albuterolia.
Monoamiinioksidaasin estäjät ja trisykliset masennuslääkkeet
VENTOLIN HFA:ta tulee antaa äärimmäisen varoen potilaille, joita hoidetaan monoamiinioksidaasin estäjillä tai trisyklisillä masennuslääkkeillä, tai 2 viikon kuluessa tällaisten lääkkeiden käytön lopettamisesta, koska albuterolin vaikutus verisuonijärjestelmään saattaa voimistua.
VAROITUKSET
Mukana osana VAROTOIMENPITEET osio.
VAROTOIMENPITEET
Paradoksaalinen Bronkospasmi
VENTOLIN HFA voi aiheuttaa paradoksaalisen bronkospasmin, joka voi olla hengenvaarallinen. Jos paradoksaalinen bronkospasmi ilmaantuu VENTOLIN HFA:n annon jälkeen, se on lopetettava välittömästi ja aloitettava vaihtoehtoinen hoito. On huomattava, että paradoksaalista bronkospasmia, kun se liittyy inhaloitaviin formulaatioihin, esiintyy usein uuden kapselin ensimmäisen käytön yhteydessä.
Astman paheneminen
Astma voi pahentua akuutisti muutaman tunnin aikana tai kroonisesti useiden päivien tai pidempään. Jos potilas tarvitsee tavallista enemmän VENTOLIN HFA -annoksia, tämä voi olla merkki astman epävakaudesta ja edellyttää potilaan ja hoito-ohjelman uudelleenarviointia kiinnittäen erityistä huomiota mahdolliseen anti-inflammatoriseen hoitoon, esim. kortikosteroideihin.
Anti-inflammatoristen aineiden käyttö
Beeta-adrenergisten agonistien keuhkoputkia laajentavien lääkkeiden käyttö ei välttämättä riitä astman hallintaan monilla potilailla. Tulehduskipulääkkeiden, esim. kortikosteroidien, lisäämistä hoito-ohjelmaan tulee harkita ajoissa.
Sydän- ja verisuonivaikutukset
VENTOLIN HFA, kuten kaikki muutkin beeta2-adrenergiset agonistit, voi aiheuttaa kliinisesti merkittäviä kardiovaskulaarisia vaikutuksia joillakin potilailla, kuten muutoksia pulssissa tai verenpaineessa. Jos tällaisia vaikutuksia ilmenee, VENTOLIN HFA:n käyttö on ehkä lopetettava. Lisäksi beeta-agonistien on raportoitu aiheuttavan EKG-muutoksia, kuten T-aallon tasoittumista, QTc-ajan pidentymistä ja ST-segmentin laskua. Näiden löydösten kliinistä merkitystä ei tunneta. Siksi VENTOLIN HFA:ta, kuten kaikkia muita sympatomimeettisiä amiineja, tulee käyttää varoen potilailla, joilla on taustalla olevia sydän- ja verisuonisairauksia, erityisesti sepelvaltimon vajaatoimintaa, sydämen rytmihäiriöitä ja verenpainetautia.
Älä ylitä suositeltua annosta
Inhaloitavien sympatomimeettisten lääkkeiden liiallisen käytön yhteydessä on raportoitu kuolemantapauksia astmapotilailla. Tarkkaa kuolinsyytä ei tunneta, mutta sydämenpysähdystä epäillään odottamattoman vakavan akuutin astmaattisen kriisin ja sitä seuranneen hypoksian seurauksena.
Välittömät yliherkkyysreaktiot
Välittömiä yliherkkyysreaktioita (esim. nokkosihottuma, angioedeema, ihottuma, bronkospasmi, hypotensio), mukaan lukien anafylaksia, saattaa ilmetä VENTOLIN HFA:n annon jälkeen [ks. VASTA-AIHEET ].
Rinnakkaiset olosuhteet
VENTOLIN HFA:ta, kuten muita sympatomimeettisiä amiineja, tulee käyttää varoen potilailla, joilla on kouristuksia, kilpirauhasen liikatoimintaa tai diabetes mellitus, ja potilaille, jotka reagoivat epätavallisen sympatomimeettisille amiineille. Suonensisäisen albuterolin suurten annosten on raportoitu pahentavan jo olemassa olevaa diabetes mellitusta ja ketoasidoosia.
Hypokalemia
Beeta-adrenergiset agonistilääkkeet voivat aiheuttaa joillakin potilailla merkittävää hypokalemiaa, mahdollisesti solunsisäisen shuntingin kautta, mikä voi aiheuttaa haitallisia kardiovaskulaarisia vaikutuksia [ks. KLIININEN FARMAKOLOGIA ]. Seerumin kaliumpitoisuuden lasku on yleensä ohimenevää, eikä se vaadi lisäravinteita.
Potilasneuvontatiedot
Neuvo potilasta lukemaan FDA:n hyväksymä potilasmerkintä ( POTILASTIEDOT ja käyttöohjeet ).
Käyttötiheys
Kerro potilaille, että VENTOLIN HFA:n vaikutuksen tulisi kestää jopa 4–6 tuntia. Älä käytä VENTOLIN HFA:ta suositeltua useammin. Neuvo potilaita olemaan suurentamatta VENTOLIN HFA:n annosta tai antotiheyttä neuvottelematta lääkärin kanssa. Neuvo potilaita hakeutumaan välittömästi lääkärin hoitoon, jos VENTOLIN HFA -hoidon teho heikkenee oireiden lievittämisessä, oireet pahenevat ja/tai heidän on käytettävä tuotetta tavallista useammin.
Pohjustus
Neuvo potilaita valmistamaan VENTOLIN HFA ennen ensimmäistä käyttökertaa, kun inhalaattoria ei ole käytetty yli 2 viikkoon tai kun inhalaattori on pudonnut. Pohjustaaksesi VENTOLIN HFA:ta, päästä 4 suihketta ilmaan pois kasvoilta ja ravista hyvin ennen jokaista suihketta.
Puhdistus
Oikean annostelun varmistamiseksi ja toimilaitteen aukon tukkeutumisen estämiseksi neuvo potilaita pesemään toimilaite lämpimällä vedellä ja antamaan sen kuivua täysin ilmassa vähintään kerran viikossa. Kerro potilaille, että potilastiedotteessa on yksityiskohtaiset puhdistusohjeet.
Paradoksaalinen Bronkospasmi
Kerro potilaille, että VENTOLIN HFA voi aiheuttaa paradoksaalisen bronkospasmin. Neuvo heitä lopettamaan VENTOLIN HFA:n käyttö, jos paradoksaalista bronkospasmia ilmenee.
Samanaikainen huumeiden käyttö
Kerro potilaille, että kun he käyttävät VENTOLIN HFA:ta, muita inhaloitavia lääkkeitä ja astmalääkkeitä tulee ottaa vain lääkärin ohjeiden mukaan.
Yleiset haittavaikutukset
Inhaloitavan albuterolin hoidon yleisiä haittavaikutuksia ovat sydämentykytys, rintakipu, nopea syke, vapina ja hermostuneisuus.
Raskaus
Neuvo raskaana olevia tai imettäviä potilaita ottamaan yhteyttä lääkäriinsä VENTOLIN HFA:n käytöstä.
VENTOLIN on GSK-konsernin rekisteröity tavaramerkki. Muut luetellut tuotemerkit ovat omistajiensa tavaramerkkejä, eivätkä ne ole GSK-yritysryhmän tavaramerkkejä. Näiden merkkien valmistajat eivät ole sidoksissa GSK-yritysryhmään tai sen tuotteisiin eivätkä tue sitä.
Ei-kliininen toksikologia
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Sprague-Dawley-rotilla tehdyssä 2-vuotisessa tutkimuksessa albuterolisulfaatti aiheutti annoksesta riippuvan mesovariumin hyvänlaatuisten leiomyoomien ilmaantuvuuden lisäyksen ravinnon annoksilla 2,0 mg/kg (noin 14 ja 6 kertaa MRHDID aikuisilla ja sitä suuremmilla) lapsilla (mg/m). Toisessa tutkimuksessa tämä vaikutus estettiin antamalla samanaikaisesti propranololia, joka on ei-selektiivinen beeta-adrenerginen antagonisti. 18 kuukautta kestäneessä CD-1-hiirillä tehdyssä tutkimuksessa albuterolisulfaatti ei osoittanut tuumorigeenisyyttä ravinnon annoksilla, jotka olivat enintään 500 mg/kg (noin 1 700 ja 800 kertaa MRHDID aikuisilla ja 800 kertaa MRHDID:iin verrattuna, mg/m²:n perusteella). ). Kultahamstereilla tehdyssä 22 kuukautta kestäneessä tutkimuksessa albuterolisulfaatti ei osoittanut tuumorigeenisyyttä ravinnon annoksilla, jotka olivat enintään 50 mg/kg (noin 225 ja 110 kertaa MRHDID aikuisilla ja 110 kertaa MRHDID:iin verrattuna, mg/m²:n perusteella).
Albuterolisulfaatti ei ollut mutageeninen Ames-testissä tai hiivan mutaatiotestissä. Albuterolisulfaatti ei ollut klastogeeninen ihmisen perifeeristen lymfosyyttien määrityksessä tai AH1-kannan hiiren mikrotumamäärityksessä.
Rotilla tehdyt lisääntymistutkimukset eivät osoittaneet heikentynyttä hedelmällisyyttä oraalisilla albuterolisulfaatin annoksilla aina 50 mg/kg asti (noin 340 kertaa aikuisten MRHDID mg/m:n perusteella).
Käyttö tietyissä populaatioissa
Raskaus
Teratogeeniset vaikutukset
Raskausluokka C. Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia VENTOLIN HFA:lla tai albuterolisulfaatilla raskaana oleville naisille. Maailmanlaajuisen markkinointikokemuksen aikana albuterolilla hoidettujen potilaiden jälkeläisillä on raportoitu erilaisia synnynnäisiä epämuodostumia, mukaan lukien suulakihalkeama ja raajavikoja. Jotkut äideistä käyttivät useita lääkkeitä raskauden aikana. Mitään johdonmukaista vikamallia ei voida havaita, eikä yhteyttä albuterolin käytön ja synnynnäisten epämuodostumien välillä ole osoitettu. Eläinten lisääntymistutkimukset hiirillä ja kaniineilla paljastivat todisteita teratogeenisuudesta. VENTOLIN HFA:ta tulee käyttää raskauden aikana vain, jos mahdollinen hyöty oikeuttaa sikiölle mahdollisesti aiheutuvan riskin. Naisia tulee neuvoa ottamaan yhteyttä lääkäriin, jos he tulevat raskaaksi VENTOLIN HFA:n käytön aikana.
Hiirillä tehdyssä lisääntymistutkimuksessa ihonalaisesti annettu albuterolisulfaatti aiheutti suulakihalkeamia 5:ssä 111:stä (4,5 %) sikiöstä altistuksilla, jotka olivat pienempiä kuin aikuisille suurin suositeltu päivittäinen inhalaatioannos (MRHDID) mg/m²:stä ja 10:ssä 108:sta. (9,3 %) sikiöt noin 8-kertaisella MRHDID:llä. Samanlaisia vaikutuksia ei havaittu noin yhdestoista MRHDID:n kohdalla. Suulakihalkeama esiintyi myös 22:lla 72:sta (30,5 %) naaraiden sikiöstä, joita hoidettiin ihonalaisesti isoproterenolilla (positiivinen kontrolli).
Kaniinin lisääntymistutkimuksessa suun kautta annettu albuterolisulfaatti aiheutti kranioskoosia 7:ssä 19 sikiöstä (37 %) noin 680-kertaisella MRHDID:llä.
Toisessa kanitutkimuksessa albuterolisulfaatti/HFA-134a-formulaatio, joka annettiin inhalaationa, suurensi sikiön fontanellien etuosaa noin kolmanneksella MRHDID:stä.
Ei-teratogeeniset vaikutukset
Tutkimus, jossa raskaana oleville rotille annettiin radioaktiivisesti leimattua albuterolisulfaattia, osoitti, että lääkkeeseen liittyvää materiaalia siirtyy äidin verenkierrosta sikiöön.
Työ ja toimitus
Ei ole olemassa hyvin kontrolloituja ihmiskokeita, jotka olisivat tutkineet VENTOLIN HFA:n vaikutuksia ennenaikaiseen synnytykseen tai synnytykseen. Koska beeta-agonisti saattaa vaikuttaa kohdun supistumiskykyyn, VENTOLIN HFA:n käyttö synnytyksen aikana tulee rajoittaa potilaisiin, joiden hyödyt ovat selvästi suuremmat kuin riskit.
Imettävät äidit
Plasman albuterolisulfaatin ja HFA-134a:n pitoisuudet inhaloitavien terapeuttisten annosten jälkeen ovat ihmisillä erittäin alhaiset, mutta ei tiedetä, erittyvätkö VENTOLIN HFA:n komponentit äidinmaitoon. Koska albuterolilla on eläinkokeissa todettu tuumorigeenisyyttä ja koska VENTOLIN HFA:n käytöstä imettävillä äideillä ei ole kokemusta, on tehtävä päätös, lopetetaanko imetys vai lopetetaanko lääke, ottaen huomioon lääkkeen merkitys äiti. Varovaisuutta tulee noudattaa, kun VENTOLIN HFA:ta annetaan imettäville naisille.
Käyttö lapsille
VENTOLIN HFA:n turvallisuus ja tehokkuus 4-vuotiailla ja sitä vanhemmilla lapsilla on osoitettu perustuen kahteen 12 viikkoa kestäneeseen kliiniseen tutkimukseen yli 12-vuotiailla astmapotilailla ja yhden 2 viikon kliinisen tutkimuksen perusteella 4–11-vuotiailla astmapotilailla. [katso HAITTAVAIKUTUKSET , Kliiniset tutkimukset ]. VENTOLIN HFA:n turvallisuutta ja tehokkuutta alle 4-vuotiailla lapsilla ei ole varmistettu. VENTOLIN HFA:n turvallisuuden ja tehon arvioimiseksi alle 4-vuotiailla koehenkilöillä on suoritettu kolme tutkimusta, ja tulokset on kuvattu alla.
Kaksi 4 viikon satunnaistettua, kaksoissokkoutettua, lumekontrolloitua tutkimusta suoritettiin 163 lapsella, jotka olivat iältään syntymästä 48 kuukauden ikään ja joilla oli obstruktiiviseen hengitystiesairauksiin liittyviä bronkospasmin oireita (oireita olivat mm. hengityksen vinkuminen, yskä, hengenahdistus tai puristava tunne rinnassa). . VENTOLIN HFA tai lumelääke HFA toimitettiin joko AeroChamber Plus® Valved Holding Chamber tai Optichamber® Valved Holding Chamber ja maski kanssa 3 kertaa päivässä. Yhdessä tutkimuksessa VENTOLIN HFA:ta 90 mikrog (n = 26), VENTOLIN HFA:ta 180 mikrogrammaa (n = 25) ja lumelääkettä HFA:ta (n = 26) annettiin 24–48 kuukauden ikäisille lapsille. Toisessa tutkimuksessa VENTOLIN HFA 90 mikrogrammaa (n = 29), VENTOLIN HFA 180 mikrogrammaa (n = 29) ja lumelääkettä HFA (n = 28) annettiin syntymästä 24 kuukauden ikäisille lapsille. Neljän viikon hoitojakson aikana astman oireiden pisteytyksissä ei ollut hoitoeroja kummassakaan tutkimuksessa VENTOLIN HFA:ta 90 mikrog, VENTOLIN HFA:ta 180 mikrogrammaa ja lumelääkettä saaneiden ryhmien välillä.
Kolmannessa tutkimuksessa VENTOLIN HFA:ta arvioitiin 87:llä alle 24 kuukauden ikäisellä lapsipotilaalla akuutin hengityksen vinkumisen hoidossa. Tässä kokeessa VENTOLIN HFA toimitettiin AeroChamber Plus -venttiilikammiolla. VENTOLIN HFA 180 mcg ja VENTOLIN HFA 360 mcg välillä ei ollut merkittäviä eroja astman oirepisteissä ja astman oireiden pisteytyksen keskimääräisessä muutoksessa lähtötasosta.
In vitro -annosten karakterisointitutkimuksia suoritettiin VENTOLIN HFA:n kuljetuksen arvioimiseksi säilytyskammioiden kautta, joihin oli kiinnitetty maskeja. Tutkimukset suoritettiin kahdella eri säilytyskammiolla, joissa oli naamarit (pienet ja keskikokoiset). In vitro -tutkimustiedot, kun simuloidaan potilaan hengitystä, viittaavat siihen, että VENTOLIN HFA:n annos, joka on annettu inhaloitavaksi maskilla varustetun venttiilikammion kautta, on verrattavissa aikuisille ilman välikettä ja maskia annettuun annokseen kehon painokiloa kohden (taulukko 2). Edellä kuvatut alle 4-vuotiailla lapsilla tehdyt kliiniset tutkimukset viittaavat kuitenkin siihen, että joko VENTOLIN HFA:n optimaalista annosta ei ole määritelty tässä ikäryhmässä tai VENTOLIN HFA ei ole tehokas tässä ikäryhmässä. VENTOLIN HFA:n turvallisuutta ja tehokkuutta välikappaleen kanssa tai ilman annettuna ei ole osoitettu alle 4-vuotiaille lapsille.
Geriatrinen käyttö
VENTOLIN HFA:n kliinisissä tutkimuksissa ei ollut riittävästi 65-vuotiaita tai vanhempia, jotta voitaisiin määrittää, reagoivatko vanhemmat koehenkilöt eri tavalla kuin nuoremmat. Muut raportoidut kliiniset kokemukset eivät ole osoittaneet eroja iäkkäiden ja nuorempien potilaiden vasteissa. Yleensä iäkkään potilaan annoksen valinnassa tulee olla varovainen, yleensä alkaen annosalueen alimmasta päästä, mikä heijastaa maksan, munuaisten tai sydämen toiminnan heikkenemisen sekä samanaikaisen sairauden tai muun lääkehoidon yleisyyttä.
YLIANNOSTUS
Odotetut merkit ja oireet albuterolin yliannostuksesta ovat liiallinen beeta-adrenerginen stimulaatio ja/tai minkä tahansa beeta-adrenergisen stimulaation merkkien ja oireiden esiintyminen tai voimistuminen (esim. kohtaukset, angina pectoris, kohonnut verenpaine tai hypotensio, takykardia 200 lyöntiä/min, rytmihäiriöt, hermostuneisuus, päänsärky, vapina, lihaskrampit, suun kuivuminen, sydämentykytys, pahoinvointi, huimaus, väsymys, huonovointisuus, unettomuus, hyperglykemia, hypokalemia, metabolinen asidoosi).
Kuten kaikkien inhaloitavien sympatomimeettisten lääkkeiden kohdalla, sydämenpysähdys ja jopa kuolema voi liittyä VENTOLIN HFA -inhalaatioaerosolin yliannostukseen.
Hoito koostuu VENTOLIN HFA -hoidon lopettamisesta ja asianmukaisesta oireenmukaisesta hoidosta. Kardioselektiivisen beetasalpaajan harkittua käyttöä voidaan harkita pitäen mielessä, että tällainen lääkitys voi aiheuttaa bronkospasmia. Ei ole riittävästi näyttöä sen määrittämiseksi, onko dialyysistä hyötyä VENTOLIN HFA:n yliannostuksesta.
VASTA-AIHEET
VENTOLIN HFA on vasta-aiheinen potilailla, joilla on aiemmin ollut yliherkkyys jollekin ainesosalle [ks. VAROITUKSET JA VAROTOIMET , KUVAUS ].
KLIININEN FARMAKOLOGIA
Toimintamekanismi
In vitro -tutkimukset ja in vivo -farmakologiset tutkimukset ovat osoittaneet, että albuterolilla on parempi vaikutus beeta2-adrenergisiin reseptoreihin verrattuna isoproterenoliin. Vaikka beeta2-adrenoseptorit ovat vallitsevia adrenergisiä reseptoreita keuhkoputkien sileässä lihaksessa ja beeta1-adrenoreseptorit ovat vallitsevia reseptoreita sydämessä, on myös ihmisen sydämessä beeta2-adrenoreseptoreita, jotka muodostavat 10–50 % kaikista beeta-adrenoreseptoreista. Näiden reseptorien tarkkaa toimintaa ei ole varmistettu, mutta niiden läsnäolo lisää mahdollisuutta, että jopa selektiivisillä beeta2-agonisteilla voi olla sydänvaikutuksia.
Beeta2-adrenergisten reseptorien aktivaatio hengitysteiden sileissä lihaksissa johtaa adenyylisyklaasin aktivoitumiseen ja syklisen 3',5'-adenosiinimonofosfaatin (syklisen AMP) solunsisäisen pitoisuuden kasvuun. Tämä syklisen AMP:n lisääntyminen johtaa proteiinikinaasi A:n aktivoitumiseen, mikä estää myosiinin fosforylaatiota ja alentaa solunsisäistä ionista kalsiumpitoisuutta, mikä johtaa rentoutumiseen. Albuteroli rentouttaa kaikkien hengitysteiden sileät lihakset henkitorvesta terminaalisiin keuhkoputkiin. Albuteroli toimii toiminnallisena antagonistina, joka rentouttaa hengitysteitä asiaan liittyvästä kouristusta aiheuttavasta aineesta riippumatta, mikä suojaa kaikilta keuhkoputkia supistavilta haasteilta. Lisääntyneet sykliset AMP-pitoisuudet liittyvät myös välittäjäaineiden vapautumisen estämiseen syöttösoluista hengitysteissä.
Useimmissa kontrolloiduissa kliinisissä tutkimuksissa albuterolin on osoitettu vaikuttavan enemmän hengitysteihin keuhkoputkien sileän lihaksen rentoutumisen muodossa kuin isoproterenolilla vertailukelpoisina annoksina samalla, kun sillä on vähemmän kardiovaskulaarisia vaikutuksia. Kontrolloidut kliiniset tutkimukset ja muut kliiniset kokemukset ovat osoittaneet, että inhaloitava albuteroli, kuten muutkin beeta-adrenergiset agonistilääkkeet, voi aiheuttaa joillakin potilailla merkittävän kardiovaskulaarisen vaikutuksen pulssin nopeudella, verenpaineella, oireilla ja/tai elektrokardiografisilla muutoksilla mitattuna [ks. VAROITUKSET JA VAROTOIMET ].
Farmakokinetiikka
Albuterolin systeemiset tasot ovat alhaiset suositeltujen annosten hengittämisen jälkeen. Tutkimus, joka suoritettiin 12 terveellä mies- ja naishenkilöllä käyttämällä suurempaa annosta (1 080 mikrogrammaa albuteroliemästä), osoitti, että keskimääräiset huippupitoisuudet plasmassa olivat noin 3 ng/ml annostelun jälkeen, kun albuterolia annettiin käyttämällä ponneainetta HFA-134a. Keskimääräinen aika huippupitoisuuksien saavuttamiseen (Tmax) viivästyi VENTOLIN HFA:n annon jälkeen (Tmax = 0,42 tuntia) verrattuna CFC-käyttöiseen albuteroliinhalaattoriin (Tmax = 0,17 tuntia). Albuterolin näennäinen terminaalinen puoliintumisaika plasmassa on noin 4,6 tuntia. Muita farmakokineettisiä tutkimuksia VENTOLIN HFA:lle ei suoritettu vastasyntyneillä, lapsilla tai vanhuksilla.
Eläinten toksikologia ja/tai farmakologia
Prekliininen
Suonensisäiset tutkimukset rotilla albuterolisulfaatilla ovat osoittaneet, että albuteroli läpäisee veri-aivoesteen ja saavuttaa aivopitoisuudet, jotka ovat noin 5,0 % plasman pitoisuuksista. Veri-aivoesteen ulkopuolisissa rakenteissa (käpy- ja aivolisäke) albuterolipitoisuuksien havaittiin olevan 100-kertaisia koko aivoihin verrattuna.
Laboratorio-eläimillä (minisiat, jyrsijät ja koirat) tehdyt tutkimukset ovat osoittaneet sydämen rytmihäiriöiden ja äkillisen kuoleman (jossa on histologisia todisteita sydänlihaksen nekroosista) esiintymistä, kun beeta-agonisteja ja metyyliksantiineja on annettu samanaikaisesti. Näiden löydösten kliinistä merkitystä ei tunneta.
Ponneaine HFA-134a
Ponneaineen HFA-134a havaittiin imeytyvän ja eliminoituvan nopeasti eläimillä ja ihmisillä, ja eliminaation puoliintumisaika oli eläimillä 3-27 minuuttia ja ihmisillä 5-7 minuuttia. Aika plasman maksimipitoisuuteen (Tmax) ja keskimääräinen viipymäaika ovat molemmat erittäin lyhyitä, mikä johtaa ohimenevään HFA-134a:n ilmestymiseen vereen ilman merkkejä kertymisestä.
Ponneaine HFA-134a:lla ei ole farmakologista aktiivisuutta lukuun ottamatta erittäin suuria annoksia eläimissä (eli 380–1 300 kertaa ihmisen maksimialtistus, joka perustuu plasmapitoisuuden ja aikakäyrän [AUC]-arvojen alle jäävän alueen vertailuun), mikä aiheuttaa pääasiassa ataksiaa ja vapinaa. , hengenahdistus tai syljeneritys. Nämä tapahtumat ovat samanlaisia kuin rakenteellisesti samankaltaisten CFC-yhdisteiden aiheuttamat vaikutukset, joita on käytetty laajalti annossumutteissa.
Kliiniset tutkimukset
Astmaan liittyvä bronkospasmi
12-vuotiaat ja sitä vanhemmat aikuiset ja nuoret
VENTOLIN HFA:n tehoa arvioitiin kahdessa 12 viikon satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa 12-vuotiailla ja sitä vanhemmilla potilailla, joilla oli lievä tai kohtalainen astma. Näissä kokeissa oli yhteensä 610 henkilöä (323 miestä, 287 naista). Kussakin tutkimuksessa koehenkilöt saivat 2 inhalaatiota VENTOLIN HFA:ta, CFC 11/12 -propelleed albuterolia tai HFA-134a lumelääkettä 4 kertaa päivässä 12 viikon ajan. Koehenkilöt, jotka käyttivät HFA-134a-plaseboinhalaattoria, käyttivät myös VENTOLIN HFA:ta astman oireiden lievittämiseen tarpeen mukaan. Jotkut näihin kliinisiin tutkimuksiin osallistuneet henkilöt käyttivät samanaikaisesti inhaloitavaa steroidihoitoa. Teho arvioitiin sarja pakotetun uloshengityksen tilavuudella 1 sekunnissa (FEV). Kussakin näistä kokeista 2 VENTOLIN HFA:n inhalaatiota tuotti huomattavasti paremman FEV1:n parantumisen hoitoa edeltävään arvoon verrattuna lumelääkkeeseen. Kahden kliinisen tutkimuksen tulokset kuvataan alla.
12 viikkoa kestäneessä satunnaistetussa kaksoissokkotutkimuksessa VENTOLIN HFA:ta (101 henkilöä) verrattiin CFC 11/12 -albuteroliin (99 potilasta) ja HFA-134a lumelääkeinhalaattoriin (97 potilasta) ikäisillä nuorilla ja aikuisilla. 12–76-vuotiaat, joilla on lievä tai keskivaikea astma. FEV1-sarjamittaukset [näkyy alla prosentuaalisena muutoksena testipäivän lähtötasosta päivänä 1 (n = 297) ja viikolla 12 (n = 249)] osoittivat, että 2 VENTOLIN HFA:n inhalaatiota tuotti huomattavasti paremman FEV1:n parantumisen hoitoa edeltävään arvoon verrattuna. plasebo.
FEV1 prosentuaalisena muutoksena ennakkoannoksesta suuressa, 12 viikon kliinisessä tutkimuksessa, päivä 1 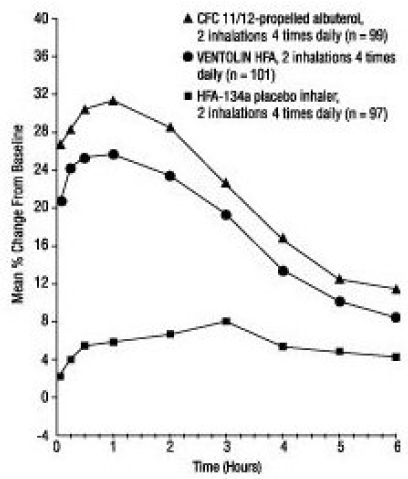
Viikko 12 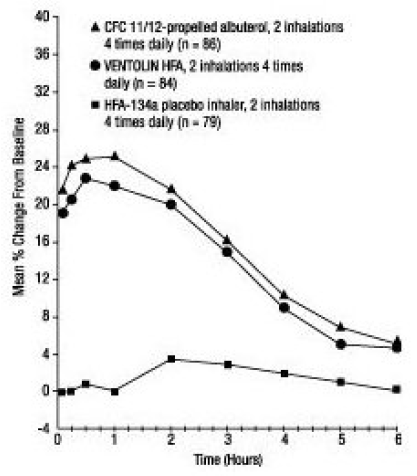
Vastaajapopulaatiossa (suurempi tai yhtä suuri kuin 15 %:n nousu FEV1:ssä 30 minuutin kuluessa annoksen ottamisesta), joita hoidettiin VENTOLIN HFA:lla, FEV1:n 15 %:n nousun alkamiseen hoitoa edeltävään arvoon verrattuna keskimääräinen aika oli 5,4 minuuttia ja keskimääräinen aika huippuvaikutus oli 56 minuuttia. Keskimääräinen vaikutuksen kesto mitattuna FEV1:n 15 %:n nousulla käsittelyä edeltävään arvoon verrattuna oli noin 4 tuntia. Joillakin koehenkilöillä vaikutuksen kesto oli jopa 6 tuntia.
Toinen 12 viikkoa kestänyt satunnaistettu kaksoissokkotutkimus suoritettiin sen tehokkuuden ja turvallisuuden arvioimiseksi, kun koehenkilöt vaihdettiin CFC 11/12 -käyttöisestä albuterolista VENTOLIN HFA:han. Kokeen 3 viikon sisäänajovaiheen aikana kaikki koehenkilöt saivat CFC 11/12 -käyttöistä albuterolia. Kaksoissokkohoitovaiheessa VENTOLIN HFA:ta (91 potilasta) verrattiin CFC 11/12 -moottorilla toimivaan albuteroliin (100 henkilöä) ja HFA-134a lumelääkeinhalaattoriin (95 henkilöä) aikuisilla ja nuorilla, joilla oli lievä tai kohtalainen astma. FEV1-sarjamittaukset osoittivat, että 2 VENTOLIN HFA:n inhalaatiota paransi merkittävästi enemmän keuhkojen toimintaa kuin lumelääke. Siirtyminen CFC 11/12 -käyttöisestä albuteroliinhalaattorista VENTOLIN HFA:han ei paljastanut kliinisesti merkittäviä muutoksia tehoprofiilissa.
Kahdessa aikuistutkimuksessa VENTOLIN HFA:n tehokkuustulokset olivat merkitsevästi parempia kuin lumelääke, ja ne olivat kliinisesti vertailukelpoisia CFC 11/12 -käyttöisellä albuterolilla saavutettuihin tuloksiin, vaikkakin pieniä numeerisia eroja havaittiin keskimääräisessä FEV-vasteessa ja muissa mittareissa. Lääkäreiden tulee huomioida, että yksilölliset vasteet beeta-adrenergisiin agonisteihin, joita annetaan eri ponneaineiden kautta, voivat vaihdella ja että vastaavia vasteita yksittäisillä potilailla ei pitäisi olettaa.
4–11-vuotiaat lapsipotilaat
VENTOLIN HFA:n tehoa arvioitiin yhdessä 2 viikon satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa tutkimuksessa 135:llä 4–11-vuotiaalla lapsipotilaalla, joilla oli lievä tai keskivaikea astma. Tässä tutkimuksessa koehenkilöt saivat VENTOLIN HFA:ta, CFC 11/12 -propelleed albuterolia tai HFA-134a lumelääkettä. Keuhkojen toiminnan sarjamittaukset osoittivat, että 2 VENTOLIN HFA:n inhalaatiota paransi merkittävästi enemmän keuhkojen toimintaa kuin lumelääke ja että VENTOLIN HFA:lla ja CFC 11/12 -käyttöisellä albuterolilla käsiteltyjen ryhmien välillä ei ollut merkittäviä eroja. VENTOLIN HFA:lla hoidetussa vasteen saaneessa populaatiossa keskimääräinen aika, jonka jälkeen uloshengitysvirtauksen huippunopeus (PEFR) lisääntyi 15 % hoitoa edeltävään arvoon verrattuna, oli 7,8 minuuttia, ja keskimääräinen aika huippuvaikutuksen saavuttamiseen oli noin 90 minuuttia. Keskimääräinen vaikutuksen kesto mitattuna PEFR:n 15 %:n nousulla esikäsittelyarvoon verrattuna oli yli 3 tuntia. Joillakin koehenkilöillä vaikutuksen kesto oli jopa 6 tuntia.
Harjoituksen aiheuttama bronkospasmi
Yksi kontrolloitu kliininen tutkimus aikuisilla astmaa sairastavilla koehenkilöillä (N = 24) osoitti, että 2 VENTOLIN HFA:n inhalaatiota noin 30 minuuttia ennen harjoittelua esti merkittävästi rasituksen aiheuttamaa bronkospasmia (mitattu FEV1:n maksimiprosentilla rasituksen jälkeen) verrattuna HFA-134a:han. lumelääke inhalaattori. Lisäksi VENTOLIN HFA:n osoitettiin olevan kliinisesti verrattavissa CFC 11/12 -käyttöiseen albuteroliinhalaattoriin tässä käyttöaiheessa.
POTILASTIEDOT
VENTOLIN® [vent' o-lin] HFA (albuterolisulfaatti) Hengitysaerosoli
Lue VENTOLIN HFA -inhalaatioaerosolin mukana tulevat potilastiedot ennen kuin aloitat sen käytön ja aina, kun saat täyttöä. Saattaa tulla uutta tietoa. Nämä potilastiedot eivät korvaa terveydenhuollon tarjoajan kanssa puhumista terveydentilastasi tai hoidostasi.
Mikä on VENTOLIN HFA?
VENTOLIN HFA on reseptilääke, jota käytetään 4-vuotiaille ja sitä vanhemmille:
- hoitaa tai ehkäistä bronkospasmia ihmisillä, joilla on palautuva obstruktiivinen hengitystiesairaus
- ehkäisee harjoituksen aiheuttamaa bronkospasmia
Ei tiedetä, onko VENTOLIN HFA turvallinen ja tehokas alle 4-vuotiaille lapsille.
Kuka ei saa käyttää VENTOLIN HFA:ta?
Älä käytä VENTOLIN HFA:ta jos olet allerginen albuterolisulfaatille tai jollekin VENTOLIN HFA:n aineosalle. Katso ”Mitä VENTOLIN HFA:n ainesosat ovat?” alla täydellinen luettelo ainesosista.
Mitä minun pitäisi kertoa terveydenhuollon tarjoajalleni ennen VENTOLIN HFA:n käyttöä?
Kerro terveydenhuollon tarjoajallesi kaikista terveydentilastasi, mukaan lukien jos:
- on sydänongelmia.
- on korkea verenpaine.
- saada kohtauksia.
- sinulla on kilpirauhasen ongelmia.
- on diabetes.
- sinulla on alhainen kaliumtaso veressäsi.
- olet allerginen jollekin VENTOLIN HFA:n aineosalle tai muille lääkkeille. Katso ”Mitä VENTOLIN HFA:n ainesosat ovat?” alla täydellinen luettelo ainesosista.
- sinulla on muita sairauksia.
- olet raskaana tai suunnittelet raskautta. Ei tiedetä, voiko VENTOLIN HFA vahingoittaa sikiötäsi.
- imettävät. Ei tiedetä, erittyykö VENTOLIN HFA:n sisältämä lääke maitoon ja voiko se vahingoittaa vauvaasi.
Kerro terveydenhuollon tarjoajallesi kaikista käyttämistäsi lääkkeistä, mukaan lukien resepti- ja käsikauppalääkkeet, vitamiinit ja yrttilisät. VENTOLIN HFA ja tietyt muut lääkkeet voivat olla vuorovaikutuksessa keskenään. Tämä voi aiheuttaa vakavia sivuvaikutuksia.
Kerro erityisesti terveydenhuollon tarjoajallesi, jos otat:
- muita inhaloitavia lääkkeitä tai astmalääkkeitä
- beetasalpaajia
- diureetteja
- digoksiini
- monoamiinioksidaasin estäjät
- trisykliset masennuslääkkeet
Pyydä terveydenhuollon tarjoajaltasi tai apteekista luettelo näistä lääkkeistä, jos et ole varma.
Tunne käyttämäsi lääkkeet. Pidä niistä luetteloa näyttääksesi terveydenhuollon tarjoajalle ja apteekkihenkilökunnalle, kun saat uuden lääkkeen.
Kuinka minun pitäisi käyttää VENTOLIN HFA:ta?
Lue vaiheittaiset ohjeet VENTOLIN HFA:n käytöstä tämän potilastietojen lopussa.
- Älä käytä VENTOLIN HFA:ta, ellei terveydenhuollon tarjoaja ole opettanut sinulle inhalaattorin käyttöä ja ymmärrät, kuinka sitä käytetään oikein.
- Lasten tulee käyttää VENTOLIN HFA:ta aikuisen avustuksella lapsen terveydenhuollon tarjoajan ohjeiden mukaisesti.
- Käytä VENTOLIN HFA:ta juuri niin kuin terveydenhuollon tarjoajasi on neuvonut käyttämään sitä. Älä käytä VENTOLIN HFA:ta useammin kuin on määrätty.
- Älä nosta annostasi tai ota ylimääräisiä VENTOLIN HFA -annoksia keskustelematta ensin terveydenhuollon tarjoajan kanssa.
- Jokaisen VENTOLIN HFA -annoksen tulee kestää 4–6 tuntia.
- Hakeudu välittömästi lääkärin hoitoon, jos VENTOLIN HFA ei enää auta oireitasi.
- Hakeudu välittömästi lääkärin hoitoon, jos oireesi pahenevat tai jos sinun on käytettävä inhalaattoria useammin.
- Kun käytät VENTOLIN HFA:ta, käytä muita inhaloitavia lääkkeitä ja astmalääkkeitä vain terveydenhuollon tarjoajan ohjeiden mukaan.
- Soita terveydenhuollon tarjoajallesi, jos astmaoireesi, kuten hengityksen vinkuminen ja hengitysvaikeudet, pahenevat muutaman tunnin tai päivän kuluessa. Terveydenhuollon tarjoajasi saattaa joutua antamaan sinulle toisen lääkkeen oireidesi hoitoon.
Mitkä ovat VENTOLIN HFA:n mahdolliset sivuvaikutukset?
VENTOLIN HFA voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- pahenevat hengitysvaikeudet, yskä ja hengityksen vinkuminen (paradoksaalinen bronkospasmi). Jos näin tapahtuu, lopeta VENTOLIN HFA:n käyttö ja soita terveydenhuollon tarjoajallesi tai hakeudu välittömästi hätäapuun. Paradoksaalinen bronkospasmi esiintyy todennäköisemmin, kun käytät ensimmäistä kertaa uutta lääkesäiliötä.
- sydänongelmia, mukaan lukien nopeampi syke ja korkea verenpaine
- mahdollinen kuolema astmapotilailla, jotka käyttävät liikaa VENTOLIN HFA:ta
- vakavia allergisia reaktioita. Soita terveydenhuollon tarjoajallesi tai hakeudu ensiapuun, jos saat jonkin seuraavista vakavan allergisen reaktion oireista:
- ihottuma
- nokkosihottuma
- kasvojen, suun ja kielen turvotus
- hengitysongelmia
- muutokset veren laboratorioarvoissa (sokeri, kalium)
VENTOLIN HFA:n yleisiä sivuvaikutuksia ovat:
- kipeä kurkku
- ylempien hengitysteiden infektio, mukaan lukien virusinfektio
- yskä
- lihaskipu
- sydämesi tuntuu hakkaavan tai jyskyttävän (tykytystykytys)
- rintakipu
- nopea syke
- vapina
- hermostuneisuus
- huimaus
Kerro terveydenhuollon tarjoajallesi kaikista sivuvaikutuksista, jotka häiritsevät sinua tai jotka eivät katoa.
Nämä eivät ole kaikki VENTOLIN HFA:n sivuvaikutuksia. Kysy lisätietoja terveydenhuollon tarjoajaltasi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
Kuinka minun pitäisi säilyttää VENTOLIN HFA?
- Säilytä VENTOLIN HFA:ta huoneenlämmössä 20 °C - 25 °C (68 °F - 77 °F) suukappale alaspäin.
- VENTOLIN HFA:n sisältö on paineen alaisena: Älä puhkaise. Älä käytä tai säilytä lämmön tai avotulen lähellä. Yli 120 °F:n lämpötilat voivat aiheuttaa kapselin räjähtämisen.
- Älä heitä tuleen tai jätteenpolttouuniin.
- Säilytä VENTOLIN HFA avaamattomassa foliopussissa ja avaa vasta, kun se on käyttövalmis.
- Pidä VENTOLIN HFA ja kaikki lääkkeet poissa lasten ulottuvilta.
Yleistä tietoa VENTOLIN HFA:n turvallisesta ja tehokkaasta käytöstä
Lääkkeitä määrätään joskus tarkoituksiin, joita ei ole mainittu potilastiedotteessa. Älä käytä VENTOLIN HFA:ta sairauteen, johon sitä ei ole määrätty. Älä anna VENTOLIN HFA:ta muille ihmisille, vaikka heillä olisi sama sairaus kuin sinulla. Se voi vahingoittaa heitä.
Tämä potilastietolehtinen tiivistää tärkeimmät tiedot VENTOLIN HFA:sta. Jos haluat lisätietoja, keskustele terveydenhuollon tarjoajan tai apteekkihenkilökunnan kanssa. Voit kysyä terveydenhuollon tarjoajalta tai apteekista terveydenhuollon ammattilaisille kirjoitettua tietoa VENTOLIN HFA:sta.
Lisätietoja VENTOLIN HFA:sta saat soittamalla numeroon 1-888-825-5249 tai vierailemalla verkkosivuillamme osoitteessa www.ventolin.com.
Mitä ainesosia VENTOLIN HFA sisältää?
Aktiivinen ainesosa: albuterolisulfaatti
Ei-aktiivinen ainesosa: ponneaine HFA-134a
Käyttöohjeet
Vain suun kautta hengitettynä
VENTOLIN HFA -inhalaattorisi
- Metallisäiliö pitää lääkkeen. Katso Kuva A.
Kuva A 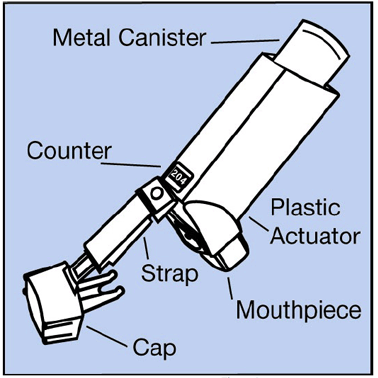
- Säiliössä on laskuri, joka näyttää kuinka monta lääkesuihketta sinulla on jäljellä. Numero näkyy toimilaitteen takana olevan ikkunan läpi. Katso kuva B.
Kuva B 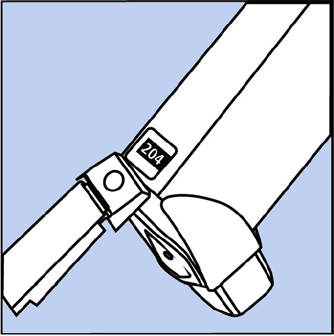
- Laskuri alkaa jommastakummasta 204 tai 064 riippuen siitä, minkä kokoinen inhalaattori sinulla on. Luku laskee 1:llä joka kerta, kun ruiskutat inhalaattoria. Laskuri lopettaa laskemisen 000:aan.
- Älä yritä muuttaa numeroita tai ottaa laskuria pois metallisäiliöstä. Laskuria ei voi nollata, ja se on kiinnitetty pysyvästi kanisteriin.
- Sininen muovinen toimilaite suihkuttaa lääkettä säiliöstä. Toimilaitteessa on suojakorkki, joka peittää suukappaleen. Katso Kuva A . Pidä suojus suukappaleessa, kun säiliö ei ole käytössä. Hihna pitää kannen kiinni toimilaitteessa.
- Älä käytä toimilaitetta minkä tahansa muun inhalaattorin lääkesäiliön kanssa.
- Älä käytä VENTOLIN HFA -säiliötä minkä tahansa muun inhalaattorin toimilaitteen kanssa.
Ennen kuin käytät VENTOLIN HFA -inhalaattoria
- Ota VENTOLIN HFA pois foliopussista juuri ennen kuin käytät sitä ensimmäistä kertaa. Hävitä pussi ja pussin sisällä oleva kuivauspaketti turvallisesti.
- Inhalaattorin tulee olla huoneenlämpöinen ennen käyttöä.
- Jos lapsesi tarvitsee VENTOLIN HFA:ta, tarkkaile lastasi tarkasti varmistaaksesi, että lapsesi käyttää inhalaattoria oikein. Terveydenhuollon tarjoaja näyttää sinulle, kuinka lapsesi tulee käyttää VENTOLIN HFA:ta.
Täytä VENTOLIN HFA -inhalaattorisi
- Ennen kuin käytät VENTOLIN HFA:ta ensimmäistä kertaa, sinun on esivalmistettava inhalaattori, jotta saat oikean määrän lääkettä, kun käytät sitä.
- Valmistele inhalaattori poistamalla suukappaleen korkki ja ravistamalla inhalaattoria hyvin. Suihkuta sitten inhalaattoria kerran ilmaan pois kasvoiltasi. Katso kuva C. Vältä roiskumista silmiin.
Kuva C 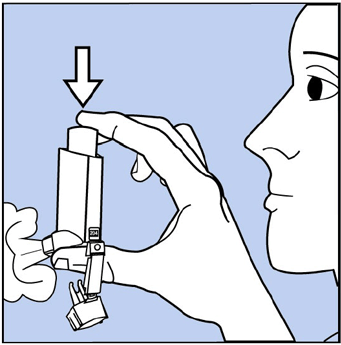
- Ravista ja suihkuta inhalaattoria tällä tavalla vielä 3 kertaa, jotta se viimeistelee sen. Laskurin pitäisi nyt lukea 200 tai 60 , riippuen siitä, minkä kokoinen inhalaattori sinulla on. Katso kuva D.
Kuva D 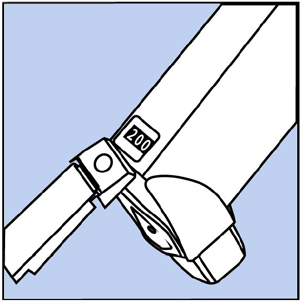
- Sinun on täytettävä inhalaattorisi uudelleen, jos et ole käyttänyt sitä yli 14 päivään tai jos pudotat sen. Ota korkki pois suukappaleesta ja ravista ja suihkuta inhalaattoria 4 kertaa ilmaan pois kasvoiltasi.
Kuinka käyttää VENTOLIN HFA -inhalaattoria
Noudata näitä ohjeita aina, kun käytät VENTOLIN HFA:ta.
Vaihe 1. Varmista, että säiliö sopii tiukasti toimilaitteeseen. Laskurin pitäisi näkyä toimilaitteen ikkunan läpi.
Ravista inhalaattoria hyvin ennen jokaista ruiskutusta.
Ota korkki pois toimilaitteen suukappaleesta. Katso, onko suukappaleen sisällä vieraita esineitä, ja poista kaikki, mitä näet.
Vaihe 2. Pidä inhalaattoria suukappale alaspäin. Katso Kuva E .
Kuva E 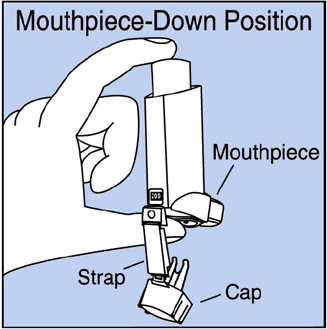
Vaihe 3. Hengitä ulos suun kautta ja työnnä niin paljon ilmaa keuhkoistasi kuin pystyt. Laita suukappale suuhusi ja sulje huulet sen ympärille. Katso kuva F .
Kuva F 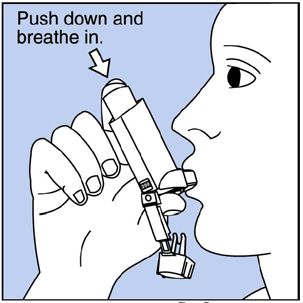
Vaihe 4. Työnnä säiliön yläosa kokonaan alas samalla kun hengität syvään ja hitaasti suun kautta. Katso Kuva F .
Vaihe 5. Kun suihke on tullut ulos, ota sormesi pois säiliöstä. Kun olet hengittänyt kokonaan sisään, ota inhalaattori ulos suustasi ja sulje suusi.
Vaihe 6. Pidätä hengitystäsi noin 10 sekuntia tai niin kauan kuin tuntuu mukavalta. Hengitä ulos niin pitkään kuin pystyt.
Jos terveydenhuollon tarjoaja on kertonut sinulle e more s prays , odota 1 minuutti ja ravista inhalaattoria uudelleen. Toista vaiheet 2–6.
Vaihe 7. Laita korkki takaisin suukappaleeseen jokaisen inhalaattorin käytön jälkeen. Varmista, että se napsahtaa tiukasti paikalleen.
VENTOLIN HFA -inhalaattorin puhdistus
Puhdista inhalaattorisi vähintään kerran viikossa. Et ehkä näe lääkkeen kerääntymistä inhalaattoriin, mutta on tärkeää pitää se puhtaana, jotta lääkkeen kerääntyminen ei estä suihketta. Katso kuva G.
Kuva G 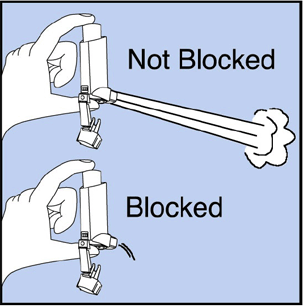
Vaihe 8. Ota säiliö pois toimilaitteesta ja poista suukappaleen korkki. Kannen hihna pysyy kiinni toimilaitteessa.
Vaihe 9. Pidä toimilaitetta hanan alla ja juokse lämmintä vettä sen läpi noin 30 sekunnin ajan. Katso Kuva H.
Kuva H 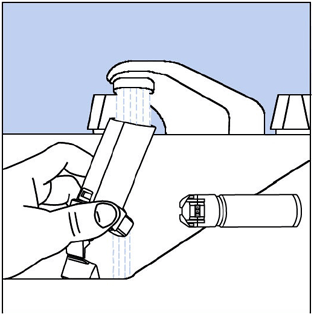
Vaihe 10. Käännä toimilaite ylösalaisin ja valuta lämmintä vettä suukappaleen läpi noin 30 sekunnin ajan. Katso Kuva I .
Kuva I 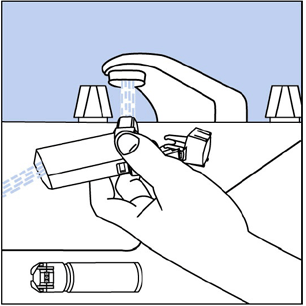
Vaihe 11. Ravista toimilaitteesta niin paljon vettä kuin mahdollista. Katso suukappaleeseen varmistaaksesi, että lääkkeen kerääntyminen on pesty kokonaan pois. Jos siinä on kerääntymiä, toista vaiheet 9 ja 10.
Vaihe 12. Anna toimilaitteen kuivua yön yli. Katso kuva J.
Kuva J 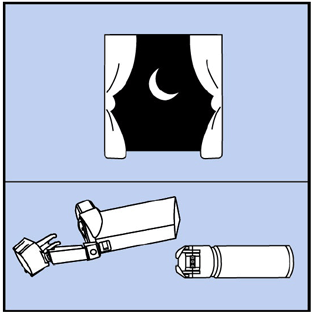
Vaihe 13. Kun toimilaite on kuiva, laita suojakorkki suukappaleeseen ja aseta sitten säiliö toimilaitteeseen ja varmista, että se sopii tiukasti. Ravista inhalaattoria hyvin, poista korkki ja suihkuta inhalaattoria kerran ilmaan pois kasvoiltasi. (Laskuri laskee yhden numeron alaspäin.) Aseta korkki takaisin suukappaleeseen.
Jos sinun on käytettävä inhalaattoria ennen kuin toimilaite on täysin kuiva:
- Ravista toimilaitteesta niin paljon vettä kuin pystyt.
- Laita korkki suukappaleeseen ja aseta sitten säiliö toimilaitteeseen ja varmista, että se sopii tiukasti.
- Ravista inhalaattoria hyvin ja suihkuta sitä kerran ilmaan pois kasvoiltasi.
- Ota VENTOLIN HFA -annos ohjeiden mukaan.
- Noudata yllä olevia puhdistusvaiheita 8–13.
VENTOLIN HFA -inhalaattorin vaihtaminen:
- Kun laskuri näyttää 020, sinun tulee täyttää reseptisi tai kysyä terveydenhuollon tarjoajalta, jos tarvitset toisen reseptin VENTOLIN HFA:lle.
- Heitä inhalaattori pois kun laskuri lukee 0 tai 12 kuukautta foliopussin avaamisen jälkeen sen mukaan, kumpi tulee ensin. Älä käytä inhalaattoria, kun laskuri on 000, koska et saa oikeaa lääkemäärää.
- Älä käytä inhalaattoria viimeisen käyttöpäivämäärän jälkeen, joka on merkitty pakkaukseen.
Muista, että käytät VENTOLIN HFA -inhalaattoriasi oikein:
- Säiliön tulee aina asettua tukevasti toimilaitteeseen.
- Hengitä syvään ja hitaasti sisään varmistaaksesi, että saat kaiken lääkkeen.
- Pidätä hengitystäsi noin 10 sekuntia lääkkeen sisäänhengityksen jälkeen. Hengitä sitten kokonaan ulos.
- Pidä aina suojakorkki suukappaleessa, kun inhalaattorisi ei ole käytössä.
- Säilytä inhalaattoria aina suukappale alaspäin.
- Puhdista inhalaattorisi vähintään kerran viikossa.
Jos sinulla on kysyttävää VENTOLIN HFA:sta tai inhalaattorin käytöstä, soita GlaxoSmithKlinelle (GSK) numeroon 1-888-825-5249 tai käy osoitteessa www.ventolin.com.
Nämä potilastiedot ja käyttöohjeet ovat Yhdysvaltain elintarvike- ja lääkeviraston hyväksymiä.
