Astman hoito: Combivent 50/20mcg Levosalbutamol Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Combivent® (ipratropiumbromidi ja albuterolisulfaatti) Hengitys Aerosoli
Bronchodilator-aerosoli Vain suun kautta hengitettäväksi
KUVAUS
KOMBIVENT Inhalaatioaerosoli on ipratropiumbromidin (monohydraattina) ja albuterolisulfaatin yhdistelmä.
Ipratropiumbromidi on antikolinerginen bronkodilaattori, joka on kemiallisesti kuvattu 8-atsoniabisyklo[3.2.1]oktaaniksi, 3-(3-hydroksi-1-okso-2-fenyylipropoksi)-8-metyyli-8-(1-metyylietyyli)-, bromidimonohydraattiksi, ( 3-endo, 8-syn)-: synteettinen kvaternaarinen ammoniumyhdiste, joka on kemiallisesti sukua atropiinille. Ipratropiumbromidi on valkoinen tai luonnonvalkoinen kiteinen aine, joka liukenee vapaasti veteen ja metanoliin, liukenee niukasti etanoliin ja ei liukene lipofiilisiin liuottimiin, kuten eetteriin, kloroformiin ja fluorihiilivetyihin.
Rakennekaava on:
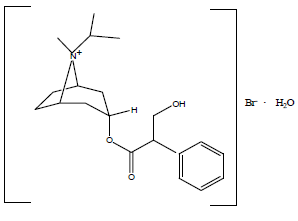 C20H30BrNO3•H2O ipratropiumbromidi Mol. Wt. 430.4
C20H30BrNO3•H2O ipratropiumbromidi Mol. Wt. 430.4
Albuterolisulfaatti, joka tunnetaan kemiallisesti nimellä (1,3-bentseenidimetanoli, α'-[[(1,1-dimetyylietyyli)amino]metyyli]-4-hydroksisulfaatti (2:1)(suola), (±)- on suhteellisen selektiivinen beeta2-adrenerginen keuhkoputkia laajentava lääke. Albuteroli on virallinen yleisnimi Yhdysvalloissa. Maailman terveysjärjestön suosittelema lääkkeen nimi on salbutamoli. Albuterolisulfaatti on valkoista luonnonvalkoista kiteistä jauhetta, joka liukenee hyvin veteen ja liukenee hieman alkoholiin, kloroformi ja eetteri. Rakennekaava on:
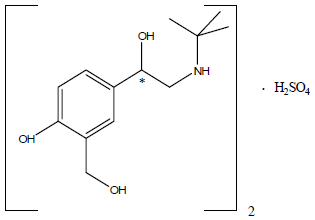 (C13H21NO3)2•H2SO4-albuterolisulfaatti Mol. Wt. 576,7
(C13H21NO3)2•H2SO4-albuterolisulfaatti Mol. Wt. 576,7
Combivent® (ipratropiumbromidi ja albuterolisulfaatti) Inhalaatioaerosoli sisältää ipratropiumbromidin ja albuterolisulfaatin mikrokiteisen suspension paineistetussa mitatun annoksen aerosoliyksikössä oraalista inhalaatiota varten. 200 inhalaatioyksikön nettopaino on 14,7 grammaa. Jokainen käyttölaite mittaa venttiilistä 21 mikrogrammaa ipratropiumbromidia ja 120 mikrogrammaa albuterolisulfaattia ja antaa 18 mikrogrammaa ipratropiumbromidia ja 103 mikrogrammaa albuterolisulfaattia (vastaa 90 mikrogrammaa albuteroliemästä) suukappaleesta. Apuaineet ovat diklooridifluorimetaani, diklooritetrafluorietaani ja trikloorimonofluorimetaani ponneaineina sekä soijalesitiini.
INDIKAATIOT
COMBIVENT Inhalation Aerosol on tarkoitettu käytettäväksi potilailla, joilla on krooninen obstruktiivinen keuhkoahtaumatauti (COPD) ja jotka käyttävät säännöllistä aerosolikeuhkoputkia laajentavaa lääkettä ja joilla on edelleen merkkejä bronkospasmista ja jotka tarvitsevat toisen bronkodilataattorin.
ANNOSTELU JA HALLINNOINTI
COMBIVENT®-inhalaatioaerosolin annos on kaksi inhalaatiota neljä kertaa päivässä. Potilaat voivat ottaa lisäinhalaatioita tarpeen mukaan; inhalaatioiden kokonaismäärä ei kuitenkaan saa ylittää 12:ta 24 tunnin aikana. COMBIVENT-inhalaatioaerosolin lisäannosten turvallisuutta ja tehoa, jotka kestävät yli 12 suihketta/24 tuntia, ei ole tutkittu. Myöskään ipratropiumin tai albuterolin ylimääräisten annosten turvallisuutta ja tehoa Combivent®:n (ipratropiumbromidi ja albuterolisulfaatti) inhalaatioaerosolin suositeltujen annosten lisäksi ei ole tutkittu. On suositeltavaa "koesuihkuttaa" kolme kertaa ennen ensimmäistä käyttöä ja tapauksissa, joissa aerosolia ei ole käytetty yli 24 tuntiin. Vältä suihkuttamista silmiin.
MITEN TOIMITETAAN
KOMBIVENTTI Hengitysaerosoli toimitetaan mitta-annosinhalaattorina, jossa on valkoinen suukappale, jossa on kirkas, väritön holkki ja oranssi suojakorkki. COMBIVENT 20mcg inhalaatioaerosolisäiliötä saa käyttää vain COMBIVENT 20mcg inhalaatioaerosolisuukappaleen kanssa, ei muiden suukappaleiden kanssa. Tätä suukappaletta ei saa käyttää muiden aerosolilääkkeiden kanssa. Jokainen käyttölaite mittaa venttiilistä 21 mikrogrammaa ipratropiumbromidia ja 120 mikrogrammaa albuterolisulfaattia ja antaa 18 mikrogrammaa ipratropiumbromidia ja 103 mikrogrammaa albuterolisulfaattia (vastaa 90 mikrogrammaa albuteroliemästä) suukappaleesta.
Jokainen 14,7 gramman kanisteri riittää 200 toimenpiteeseen ( NDC 0597-001314).
Varoitus: Säiliö tulee hävittää, kun merkitty määrä käyttökertoja on käytetty. Oikeaa lääkemäärää jokaisella painalluksella ei voida taata tämän jälkeen, vaikka säiliö ei olekaan täysin tyhjä.
Säilytä 25°C (77°F); retket sallittu 15°-30°C (59°-86°F) [katso USP-ohjattu huonelämpötila ]. Parhaan tuloksen saavuttamiseksi säilytä kanisteri huoneenlämmössä ennen käyttöä. Vältä liiallista kosteutta. Ravista säiliötä voimakkaasti vähintään 10 sekuntia ennen käyttöä.
Osoita lääketieteellisiä tiedusteluja: http://us.boehringer-ingelheim.com, (800) 542-6257 tai (800) 459-9906 TTY.
merkintä: Liittovaltion puhtaasta ilmaa koskeva laki edellyttää alla olevaa sisennettyä lausuntoa kaikilta kloorifluorihiilivetyjä (CFC-yhdisteitä) sisältäviltä tai niillä valmistetuilta tuotteilta:
Varoitus: Sisältää trikloorimonofluorimetaania (CFC-11), diklooridifluorimetaania (CFC-12) ja diklooritetrafluorietaania (CFC-114), aineita, jotka vahingoittavat kansanterveyttä ja ympäristöä tuhoamalla otsonia yläilmakehässä.
Yllä olevan kaltainen huomautus Varoitus on sijoitettu tämän tuotteen potilastietoihin Environmental Protection Agencyn (EPA) määräysten mukaisesti. Potilaan varoituksessa todetaan, että potilaan tulee kääntyä lääkärin puoleen, jos hänellä on kysyttävää vaihtoehdoista.
Sisältö paineen alla: Älä puhkaise. Älä käytä tai säilytä lämmön tai avotulen lähellä. Altistuminen yli 120 °F:n lämpötiloille voi aiheuttaa halkeamia. Älä koskaan heitä inhalaattoria tuleen tai jätteenpolttouuniin.
Jakelija: Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 USA. Ipratropiumbromidi lisensoi: Boehringer Ingelheim International GmbH. Tarkistettu: elokuu 2012
SIVUVAIKUTUKSET
Combivent® (ipratropiumbromidi ja albuterolisulfaatti) -inhalaatioaerosolia koskevat haittavaikutukset ovat peräisin kahdesta 12 viikkoa kestäneestä kontrolloidusta kliinisestä tutkimuksesta (N=358 COMBIVENT-inhalaatioaerosolille), kuten taulukosta 1 näkyy.
Muita haittavaikutuksia, joita on raportoitu alle kahdella prosentilla COMBIVENT-inhalaatioaerosolihoitoryhmän potilaista, ovat turvotus, väsymys, kohonnut verenpaine, huimaus, hermostuneisuus, parestesia, vapina, dysfonia, unettomuus, ripuli, suun kuivuminen, dyspepsia, oksentelu, rytmihäiriöt, sydämentykytys, takykardia, nivelkipu, angina pectoris, lisääntynyt yskös, makuaistin vääristyminen ja virtsatieinfektio/dysuria.
Allergisen tyyppisiä reaktioita, kuten ihoreaktioita, mukaan lukien ihottuma, kutina ja nokkosihottuma (mukaan lukien jättimäinen nokkosihottuma), angioedeemaa, mukaan lukien kielen, huulten ja kasvojen turvotus, laryngospasmi ja anafylaktinen reaktio, on raportoitu Combivent® (ipratropiumbromidi ja albuterolisulfaatti) inhalaatioaerosolien kanssa , joissakin tapauksissa positiivisella uudelleenhaastuksella. Monilla näistä potilaista on ollut allergioita muille lääkkeille ja/tai elintarvikkeille, mukaan lukien soijapavulle (ks VASTA-AIHEET ).
Markkinoinnin jälkeinen kokemus
Viiden vuoden lumekontrolloidussa tutkimuksessa sairaalahoitoja supraventrikulaarisen takykardian ja/tai eteisvärinän vuoksi esiintyi 0,5 %:lla keuhkoahtaumatautipotilailla, jotka saivat Atrovent® (ipratropiumbromidi) inhalaatioaerosoli CFC:tä.
Muita julkaistusta kirjallisuudesta ja/tai markkinoille tulon jälkeisestä seurannasta ipratropiumbromidia sisältävien tuotteiden käytöstä (yksin tai yhdessä albuterolin kanssa) tunnistettuja sivuvaikutuksia ovat: yliherkkyys, nielun turvotus, suun turvotus, virtsan kertymä, mydriaasi, bronkospasmi ( mukaan lukien paradoksaalinen bronkospasmi), kapeakulmaglaukooman saostuminen tai paheneminen, glaukooma, kohonnut silmänpaine, akuutti silmäkipu, halonäkö, näön hämärtyminen, akkomodaatiohäiriö, silmän ärsytys, sarveiskalvon turvotus, sidekalvon hyperemia, nenän tukkoisuus, eritteiden kuivuminen , limakalvon haavaumat, suutulehdus, aerosoliärsytys, kurkun ärsytys, kurkun kuivuminen, hengityksen vinkuminen, COPD-oireiden paheneminen, käheys, sydämentykytys, närästys, uneliaisuus, keskushermoston stimulaatio, koordinaatiovaikeudet, punoitus, hiustenlähtö, hypotensio, turvotus, pahoinvointi, oksentelu), maha-suolikanavan motiliteettihäiriö, ummetus, hypokalemia, mielenterveyshäiriöt, liikahikoilu, lihaskouristukset, lihasheikkous, myalgia, voimattomuus, sydänlihasiskemia, diastolinen verenpaine alentunut ja systolinen verenpaine kohonnut.
Metabolista asidoosia on raportoitu albuterolia sisältävien tuotteiden käytön yhteydessä.
HUUMEIDEN VUOROVAIKUTUKSET
KOMBIVENTTI Inhalaatioaerosolia on käytetty samanaikaisesti muiden lääkkeiden kanssa, mukaan lukien sympatomimeettiset keuhkoputkia laajentavat lääkkeet, metyyliksantiinit sekä oraaliset ja inhaloitavat steroidit, joita käytetään yleisesti kroonisen obstruktiivisen keuhkosairauden hoidossa. Albuterolia lukuun ottamatta ei ole olemassa virallisia tutkimuksia, joissa olisi täysin arvioitu COMBIVENT-inhalaatioaerosolin ja näiden lääkkeiden yhteisvaikutuksia turvallisuuden ja tehokkuuden suhteen.
Antikolinergiset aineet
Samanaikaisesti käytettyjen antikolinergisten lääkkeiden kanssa on mahdollista additiivinen yhteisvaikutus. Vältä siksi COMBIVENT 50 mg inhalaatioaerosolin antamista samanaikaisesti muiden antikolinergisiä aineita sisältävien lääkkeiden kanssa.
Beeta-adrenergiset aineet
COMBIVENT Inhalation Aerosolin ja muiden sympatomimeettisten aineiden yhteiskäytössä on noudatettava varovaisuutta kardiovaskulaaristen haittavaikutusten lisääntyneen riskin vuoksi.
Beetasalpaajat ja albuteroli estävät toistensa vaikutusta. Beetasalpaajia tulee käyttää varoen potilailla, joilla on hyperreaktiiviset hengitystiet.
Diureetit
Beeta-agonistit voivat pahentaa äkillisesti EKG-muutoksia ja/tai hypokalemiaa, jotka voivat johtua kaliumia säästämättömien diureettien (kuten loop- tai tiatsididiureettien) antamisesta, erityisesti jos beeta-agonistin suositeltu annos ylittyy. Vaikka näiden vaikutusten kliinistä merkitystä ei tunneta, varovaisuutta tulee noudattaa annettaessa beeta-agonisteja sisältäviä lääkkeitä, kuten COMBIVENT-inhalaatioaerosolia, yhdessä kaliumia säästämättömien diureettien kanssa. Harkitse kaliumtasojen seurantaa.
Monoamiinioksidaasin estäjät tai trisykliset masennuslääkkeet
YMPÄRISTÖINHALATUS Aerosolia tulee antaa äärimmäisen varovaisesti potilaille, joita hoidetaan monoamiinioksidaasin estäjillä tai trisyklisillä masennuslääkkeillä, tai kahden viikon kuluessa tällaisten lääkkeiden käytön lopettamisesta, koska albuterolin vaikutus sydän- ja verisuonijärjestelmään saattaa voimistua. Harkitse vaihtoehtoista hoitoa potilaille, jotka käyttävät MAO-lääkkeitä tai trisyklisiä masennuslääkkeitä.
VAROITUKSET
VAROTOIMENPITEET
Kenraali
Tietoa potilaille
Potilaita tulee varoittaa olemaan suihkuttamasta aerosolia silmiinsä, ja heille on kerrottava, että tämä voi aiheuttaa ahdaskulmaglaukooman, mydriaasin, silmänsisäisen paineen nousun, akuutin silmäkipun tai -epämukavuuden, tilapäisen näön hämärtymisen, näön hämärtymisen tai värjäytymisen. kuvat yhdessä sidekalvon ja sarveiskalvon tukkoisuuden aiheuttamien punaisten silmien kanssa. Potilaita tulee myös kertoa, että jos jokin näiden oireiden yhdistelmä kehittyy, heidän on otettava välittömästi yhteys lääkäriin.
COMBIVENT 20mcg inhalaatioaerosolin vaikutuksen tulisi kestää 4-5 tuntia tai kauemmin. KOMBIVENTTI Hengitysaerosolia ei tule käyttää suositeltua useammin. Älä lisää COMBIVENT-inhalaatioaerosolin annosta tai tiheyttä keskustelematta lääkärisi kanssa. Jos huomaat, että hoito COMBIVENT 20mcg inhalaatioaerosolilla heikkenee oireiden lievittämisessä, oireesi pahenevat ja/tai joudut käyttämään tuotetta tavallista useammin, on hakeuduttava välittömästi lääkärin hoitoon. Kun käytät COMBIVENT-inhalaatioaerosolia, muita inhaloitavia lääkkeitä tulee käyttää vain lääkärisi ohjeiden mukaan. Jos olet raskaana tai imetät, ota yhteyttä lääkäriisi COMBIVENT-inhalaatioaerosolin käytöstä. Combivent®:n (ipratropiumbromidi ja albuterolisulfaatti) asianmukainen käyttö Inhalaatioaerosoli sisältää ymmärryksen tavasta, jolla se tulee antaa (ks. Potilaan käyttöohjeet ).
Koska COMBIVENT 20 mikrogrammaa käytettäessä voi esiintyä huimausta, akkomodaatiohäiriötä, mydriaasia ja näön hämärtymistä, potilaita tulee varoittaa harjoittamasta tasapainoa ja näöntarkkuutta vaativia toimintoja, kuten auton ajamista tai koneiden tai koneiden käyttöä.
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Ipratropiumbromidi
Kahden vuoden suun kautta annetut karsinogeenisuustutkimukset rotilla ja hiirillä eivät ole osoittaneet karsinogeenista aktiivisuutta annoksilla 6 mg/kg asti. Tämä annos vastaa rotilla ja hiirillä noin 230 ja 110 kertaa ipratropiumbromidin suurinta suositeltua päivittäistä inhalaatioannosta aikuisilla, vastaavasti mg/m²:n perusteella. Tulokset useista mutageenisuustutkimuksista (Ames-testi, hiiren dominanttiletaalitesti, hiiren mikrotumatesti ja luuytimen kromosomipoikkeavuus kiinalaisilla hamstereilla) olivat negatiivisia.
Ipratropiumbromidin anto ei vaikuttanut uros- tai naarasrottien hedelmällisyyteen oraalisilla annoksilla 50 mg/kg asti (noin 1900 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella). Suun kautta annetulla 500 mg/kg:n annoksella (noin 19 000 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella) ipratropiumbromidi vähensi hedelmöittymistä.
Albuteroli
Kuten muutkin luokkansa aineet, albuteroli aiheutti merkittävän annoksesta riippuvan lisäyksen mesovariumin hyvänlaatuisten leiomyoomien ilmaantuvuudessa 2 vuotta kestäneessä tutkimuksessa rotilla ravinnon annoksilla 2, 10 ja 50 mg/kg (noin 15 65 ja 330 kertaa suurin suositeltu päivittäinen inhalaatioannos aikuisilla (mg/m²). Toisessa tutkimuksessa tämä vaikutus esti propranololin samanaikaisen antamisen. Näiden löydösten merkitystä ihmisille ei tunneta. 18 kuukauden tutkimus hiirillä 500 mg/kg asti (noin 1600 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella) ja 99 viikkoa kestänyt tutkimus hamstereilla oraalisilla annoksilla enintään 50 mg /kg (noin 220 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella) ei osoittanut merkkejä tuumorigeenisyydestä. Albuterolilla tehdyt tutkimukset eivät paljastaneet todisteita mutageneesista.
Rotilla tehdyt lisääntymistutkimukset albuterolisulfaatilla eivät osoittaneet merkkejä hedelmällisyyden heikkenemisestä.
Raskaus
KOMBIVENTTI Hengitysaerosoli
Teratogeeniset vaikutukset: Raskausluokka C
Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia Combivent® (ipratropiumbromidi ja albuterolisulfaatti) inhalaatioaerosolista, ipratropiumbromidista tai albuterolisulfaatista raskaana oleville naisille. Eläinten lisääntymistutkimuksia ei ole tehty COMBIVENT-inhalaatioaerosolilla. Albuterolisulfaatin on kuitenkin osoitettu olevan teratogeeninen hiirillä ja kaniineilla. KOMBIVENTTI Hengitysaerosolia tulee käyttää raskauden aikana vain, jos mahdollinen hyöty oikeuttaa mahdollisen riskin sikiölle.
Ipratropiumbromidi
Teratogeeniset vaikutukset
Oraaliset lisääntymistutkimukset suoritettiin annoksilla 10 mg/kg hiirillä, 1000 mg/kg rotilla ja 125 mg/kg kaniineilla. Nämä annokset vastaavat kullekin lajille noin 190, 38 000 ja 9 400 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella. Rotilla ja kaniineilla suoritettiin hengityksen lisääntymistutkimuksia annoksilla 1,5 ja 1,8 mg/kg (noin 55 ja 140 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella). Nämä tutkimukset eivät osoittaneet näyttöä ipratropiumbromidin teratogeenisista vaikutuksista. Suun kautta annetuilla annoksilla 90 mg/kg tai enemmän rotilla (noin 3 400 kertaa suurin suositeltu päivittäinen inhalaatioannos aikuisille mg/m²-perusteisesti) havaittiin alkiotoksisuutta lisääntyneenä resorptiona. Tätä vaikutusta ei pidetä merkityksellisenä ihmiskäytössä, koska se havaittiin suurilla annoksilla ja antoreittien eroista.
Albuteroli
Teratogeeniset vaikutukset
Albuterolin on osoitettu olevan teratogeeninen hiirillä ja kaniineilla. Lisääntymistutkimus CD-1-hiirillä, joille annettiin albuterolia ihonalaisesti (0,025, 0,25 ja 2,5 mg/kg), osoitti suulakihalkeamaa viidellä 111:stä (4,5 %) sikiöstä annoksella 0,25 mg/kg (vastaa suurinta suositeltua päivittäistä inhalaatioannosta aikuisilla mg/m² perusteella) ja 10:llä 108:sta (9,3 %) sikiöstä annoksella 2,5 mg/kg (noin 8 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella laskettuna). Mitään ei havaittu annoksella 0,025 mg/kg (vähemmän kuin aikuisten suurin suositeltu päivittäinen inhalaatioannos). Suulakihalkeama esiintyi myös 22:lla 72:sta (30,5 %) sikiöstä, joita oli hoidettu 2,5 mg/kg isoproterenolilla (positiivinen kontrolli). Lisääntymistutkimus oraalisella albuterolilla Stride Dutch -kaneilla paljasti kranioskiiksen 7:llä 19:stä (37 %) sikiöstä annoksella 50 mg/kg (noin 660 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella).
Työ ja toimitus
Koska beeta-agonisti saattaa häiritä kohdun supistumiskykyä, Combivent® (ipratropiumbromidi ja albuterolisulfaatti) -inhalaatioaerosolin käyttö keuhkoahtaumatautien hoitoon synnytyksen aikana tulee rajoittaa potilaisiin, joiden hyödyt ovat selvästi suuremmat kuin riskit.
Imettävät äidit
Ei tiedetä, erittyvätkö COMBIVENT-inhalaatioaerosolin komponentit äidinmaitoon.
Ipratropiumbromidi
Koska lipideihin liukenemattomat kvaternaariset kationit erittyvät äidinmaitoon, on noudatettava varovaisuutta, kun COMBIVENT Inhalation Aerosolia annetaan imettävälle äidille.
Albuteroli
Koska albuterolilla on eläinkokeissa todettu tuumorigeenisyyttä, on päätettävä, lopetetaanko imettäminen vai lääkkeen käyttö, ottaen huomioon lääkkeen merkitys äidille.
Käyttö lapsille
Turvallisuutta ja tehokkuutta lapsiväestössä ei ole osoitettu.
YLIANNOSTUS
Yliannostuksen vaikutusten odotetaan liittyvän ensisijaisesti albuterolisulfaattiin. Ipratropiumbromidin akuutti yliannostus hengitettynä on epätodennäköistä, koska ipratropiumbromidi ei imeydy hyvin systeemisesti aerosolin tai oraalisen annon jälkeen. Ipratropiumbromidin oraaliset tappavat annokset olivat hiirillä yli 1 001 mg/kg (noin 19 000 kertaa aikuisten suurin suositeltu päivittäinen inhalaatioannos mg/m²:n perusteella laskettuna); 1663 mg/kg rotilla (noin 62 000 kertaa suurin suositeltu päivittäinen inhalaatioannos aikuisilla mg/m²:n perusteella); ja 400 mg/kg koirilla (noin 50 000 kertaa suurin suositeltu päivittäinen inhalaatioannos aikuisilla, mg/m² perusteella). Kun albuterolisulfaatin tappava oraalinen mediaaniannos hiirillä ja rotilla oli suurempi kuin 2 000 mg/kg (noin 6 600 ja 13 000 kertaa suurin suositeltu päivittäinen inhalaatioannos aikuisilla mg/m²:n perusteella), inhaloitava keskimääräinen tappava annos ei voitu määrittää. Albuterolin yliannostuksen ilmenemismuotoja voivat olla anginakipu, kohonnut verenpaine, hypokalemia, takykardia jopa 200 lyöntiä minuutissa, metabolinen asidoosi ja HAITTAVAIKUTUKSET-kohdassa lueteltujen farmakologisten vaikutusten lisääntyminen. Kuten kaikki sympatomimeettiset aerosolilääkkeet, sydämenpysähdys ja jopa kuolema voivat liittyä väärinkäyttöön. Dialyysi ei ole sopiva hoito albuterolin yliannostukseen inhalaatioaerosolina. kardiovaskulaarisen beetasalpaajan, kuten metoprololitartraatin, harkittu käyttö saattaa olla aiheellista.
VASTA-AIHEET
KOMBIVENT Inhalaatioaerosoli on vasta-aiheinen potilaille, joilla on aiemmin ollut yliherkkyys soijalesitiinille tai vastaaville elintarvikkeille, kuten soijapavulle ja maapähkinälle. COMBIVENT Inhalation Aerosoli on myös vasta-aiheinen potilaille, jotka ovat yliherkkiä jollekin muulle lääkevalmisteen aineosalle tai atropiinille tai sen johdannaisille.
KLIININEN FARMAKOLOGIA
COMBIVENT 50 mg inhalaatioaerosoli on yhdistelmä antikolinergistä keuhkoputkia laajentavaa ipratropiumbromidia ja beeta2-adrenergistä bronkodilataattoria, albuterolisulfaattia.
Toimintamekanismi
Ipratropiumbromidi
Ipratropiumbromidi on antikolinerginen (parasympatolyyttinen) aine, joka eläinkokeiden perusteella näyttää estävän vagaalivälitteisiä refleksejä antagonisoimalla asetyylikoliinin, keuhkojen neuromuskulaarisissa liitoksissa vapautuvan välittäjäaineen, toimintaa. Antikolinergit estävät Ca++:n solunsisäisen pitoisuuden nousun, joka johtuu asetyylikoliinin vuorovaikutuksesta keuhkoputken sileän lihaksen muskariinireseptorien kanssa.
Albuterolisulfaatti
In vitro -tutkimukset ja in vivo -farmakologiset tutkimukset ovat osoittaneet, että albuterolilla on parempi vaikutus beeta2-adrenergisiin reseptoreihin verrattuna isoproterenoliin. Vaikka tiedetään, että beeta2-adrenergiset reseptorit ovat vallitsevia reseptoreita keuhkoputkien sileässä lihaksessa, viimeaikaiset tiedot osoittavat, että ihmisen sydämessä on beeta2-reseptoreiden populaatio, joka käsittää 10-50 % sydämen beeta-adrenergisista reseptoreista. Näiden reseptorien tarkkaa toimintaa ei kuitenkaan vielä tiedetä (katso VAROITUKSET ).
Beeta2-adrenergisten reseptorien aktivaatio hengitysteiden sileissä lihaksissa johtaa adenylyylisyklaasin aktivoitumiseen ja syklisen 3',5'-adenosiinimonofosfaatin (syklisen AMP) solunsisäisen pitoisuuden kasvuun. Tämä syklisen AMP:n lisääntyminen johtaa proteiinikinaasi A:n aktivoitumiseen, mikä estää myosiinin fosforylaatiota ja alentaa solunsisäistä ionista kalsiumpitoisuutta, mikä johtaa rentoutumiseen. Albuteroli rentouttaa kaikkien hengitysteiden sileät lihakset henkitorvesta terminaalisiin keuhkoputkiin. Albuteroli toimii toiminnallisena antagonistina, joka rentouttaa hengitysteitä asiaan liittyvästä kouristusta aiheuttavasta aineesta riippumatta, mikä suojaa kaikilta keuhkoputkia supistavilta haasteilta. Lisääntyneet sykliset AMP-pitoisuudet liittyvät myös välittäjäaineiden vapautumisen estämiseen syöttösoluista hengitysteissä.
Albuterolilla on useimmissa kliinisissä tutkimuksissa osoitettu olevan enemmän keuhkoputkien sileitä lihaksia rentouttavia vaikutuksia kuin isoproterenolilla vertailukelpoisina annoksina samalla kun se tuottaa vähemmän kardiovaskulaarisia vaikutuksia. Kaikki beeta-adrenergiset lääkkeet, mukaan lukien albuterolisulfaatti, voivat kuitenkin aiheuttaa merkittäviä kardiovaskulaarisia vaikutuksia joillakin potilailla (ks. VAROTOIMENPITEET ).
COMBIVENT 20mcg inhalaatioaerosoli
Combivent® (ipratropiumbromidi ja albuterolisulfaatti) Inhalaatioaerosolin odotetaan maksimoivan hoitovasteen potilailla, joilla on krooninen obstruktiivinen keuhkosairaus (COPD), vähentämällä bronkospasmia kahdella selvästi erilaisella mekanismilla, antikolinergisellä (parasympatolyyttisellä) ja sympatomimeettisellä mekanismilla. Sekä antikolinergisen aineen (ipratropiumbromidi) että beeta2-sympatomimeetin (albuterolisulfaatti) samanaikainen antaminen on suunniteltu hyödyttäväksi potilasta tuottamalla suurempi keuhkoputkia laajentava vaikutus kuin silloin, kun kumpaakaan lääkettä käytetään yksinään suositellulla annoksellaan.
Farmakokinetiikka
Ipratropiumbromidi
Suuri osa annetusta annoksesta niellään ulosteen erittymistä koskevien tutkimusten mukaan. Ipratropiumbromidi on kvaternäärinen amiini. Se ei imeydy helposti systeemiseen verenkiertoon keuhkojen pinnasta tai maha-suolikanavasta, kuten veren tasoa ja munuaisten erittymistä koskevat tutkimukset ovat vahvistaneet. Plasman ipratropiumbromidin tasot olivat alle määrityksen herkkyysrajan 100 pg/ml.
Eliminaation puoliintumisaika on noin 2 tuntia inhalaation tai suonensisäisen annon jälkeen. Ipratropiumbromidi sitoutuu minimaalisesti (0–9 % in vitro) plasman albumiiniin ja happamaan α1-glykoproteiiniin. Se metaboloituu osittain inaktiivisiksi esterihydrolyysituotteiksi. Laskimonsisäisen annon jälkeen noin puolet annoksesta erittyy muuttumattomana virtsaan. Rotilla tehdyt autoradiografiset tutkimukset ovat osoittaneet, että ipratropiumbromidi ei läpäise veri-aivoestettä.
Albuterolisulfaatti
Albuteroli on pidempivaikutteinen kuin isoproterenoli useimmilla potilailla, koska se ei ole substraatti katekoliamiinien soluunottoprosesseille eikä katekoli-O-metyylitransferaasin metabolialle. Sen sijaan lääke metaboloituu konjugatiivisesti albuteroli-4'-O-sulfaatiksi.
Farmakokineettisessä tutkimuksessa 12 terveellä vapaaehtoisella miespuolisella inhalaatiolla kahdella albuterolisulfaatin inhalaatiolla, 103 mikrogramman annos/inhalaatio suukappaleen kautta, plasman albuterolin huippupitoisuudet vaihtelivat 419-802 pg/ml (keskiarvo 599 ± 122 pg/ml). tuntia annon jälkeen. Tämän kerta-annoksen jälkeen 30,8 ± 10,2 % arvioidusta suukappaleannoksesta erittyi muuttumattomana 24 tunnin virtsaan. Koska albuterolisulfaatti imeytyy nopeasti ja täydellisesti, tässä tutkimuksessa ei voitu erottaa imeytymistä keuhkoihin ja maha-suolikanavaan.
Albuterolin suonensisäistä farmakokinetiikkaa tutkittiin vastaavassa 16 terveen miespuolisen vapaaehtoisen ryhmässä; keskimääräinen terminaalinen puoliintumisaika 30 minuutin 1,5 mg:n infuusion jälkeen oli 3,9 tuntia ja keskimääräinen puhdistuma 439 ml/min/1,73 m².
Suonensisäiset albuterolitutkimukset rotilla osoittivat, että albuteroli ylitti veri-aivoesteen ja saavutti aivopitoisuudet, jotka olivat noin 5 % plasman pitoisuuksista. Veri-aivoesteen ulkopuolisissa rakenteissa (käpy- ja aivolisäke) lääke saavutti yli 100-kertaisia pitoisuuksia koko aivoihin verrattuna.
Tiineillä rotilla tehdyt tutkimukset tritioidulla albuterolilla osoittivat, että noin 10 % emon verenkierrossa olevasta lääkkeestä siirtyi sikiöön. Jakauma sikiön keuhkoihin oli verrattavissa äidin keuhkoihin, mutta sikiön maksan jakautuminen oli 1 % äidin maksatasoista.
Laboratorio-eläimillä (minisiat, jyrsijät ja koirat) tehdyt tutkimukset ovat osoittaneet sydämen rytmihäiriöiden ja äkillisen kuoleman (jossa on histologisia todisteita sydänlihaksen nekroosista) esiintymistä, kun beeta-agonisteja ja metyyliksantiinia annettiin samanaikaisesti. Näiden löydösten merkitystä ihmisiin sovellettaessa ei tunneta.
COMBIVENT 50mg inhalaatioaerosoli
Ristikkäisessä farmakokineettisessä tutkimuksessa, johon osallistui 12 tervettä miespuolista vapaaehtoista, jossa verrattiin Combivent®:n (ipratropiumbromidi ja albuterolisulfaatti) kahden inhalaation imeytymistä ja erittymistä. kanisteri ei muuttanut merkittävästi kummankaan komponentin systeemistä imeytymistä.
Ipratropiumbromidipitoisuudet pysyivät havaittavissa olevien rajojen (
Erikoispopulaatiot
Combivent®:n (ipratropiumbromidi ja albuterolisulfaatti) farmakokinetiikkaa Inhalaatioaerosolin tai ipratropiumbromidin farmakokinetiikkaa ei ole tutkittu potilailla, joilla on maksan tai munuaisten vajaatoimintaa tai vanhuksilla (ks. VAROTOIMENPITEET ).
Huumeiden väliset vuorovaikutukset
Mitään erityisiä farmakokineettisiä tutkimuksia ei ole tehty mahdollisten lääkkeiden välisten yhteisvaikutusten arvioimiseksi.
Farmakodynamiikka
Ipratropiumbromidi
Ipratropiumbromidin inhalaation jälkeinen bronkodilataatio on ensisijaisesti paikallinen, paikkaspesifinen vaikutus, ei systeeminen.
Kontrolloidut kliiniset tutkimukset ovat osoittaneet, että ipratropiumbromidi ei muuta mukosiliaarista puhdistumaa eikä hengityseritteiden tilavuutta tai viskositeettia. Tutkimuksissa ilman positiivista kontrollia ipratropiumbromidi ei muuttanut pupillien kokoa, akkomodaatiota tai näöntarkkuutta (ks. HAITTAVAIKUTUKSET ).
Ventilaatio-/perfuusiotutkimukset eivät ole osoittaneet kliinisesti merkittäviä vaikutuksia keuhkojen kaasunvaihtoon tai valtimoiden happipaineeseen. Suositelluilla annoksilla ipratropiumbromidi ei aiheuta kliinisesti merkittäviä muutoksia pulssissa tai verenpaineessa.
Kliiniset tutkimukset
Kahdessa 12 viikkoa kestäneessä satunnaistetussa, kaksoissokkoutetussa, aktiivikontrolloidussa kliinisessä tutkimuksessa 1067 potilaalla, joilla oli krooninen obstruktiivinen keuhkosairaus (COPD), arvioitiin COMBIVENT 20 mikrogramman inhalaatioaerosolin keuhkoputkia laajentava teho (358 potilasta) verrattuna sen komponentteihin, ipratropiumbromidiin. (362 potilasta) ja albuterolisulfaattia (347 potilasta).
FEV1-sarjamittaukset (näkyy alla prosentuaalisena muutoksena testipäivän lähtötasosta) osoittivat, että COMBIVENT Inhalation Aerosoli paransi merkittävästi enemmän keuhkojen toimintaa kuin joko ipratropiumbromidi tai albuterolisulfaatti erikseen annettuna. Keskimääräinen aika FEV1:n 15 %:n nousun alkamiseen oli 15 minuuttia ja mediaaniaika FEV1:n huippuun oli yksi tunti COMBIVENT 20 mikrogramman inhalaatioaerosolilla ja sen komponenteilla. Keskimääräinen vaikutuksen kesto FEV1:llä mitattuna oli 4-5 tuntia COMBIVENT Inhalation Aerosolilla verrattuna 4 tuntiin ipratropiumbromidilla ja 3 tuntia albuterolisulfaatilla.
Prosenttimuutos mukautetussa keskiarvon FEV1:ssä testipäivän lähtötasosta - Arvioitavan tietojoukon päätepisteanalyysi 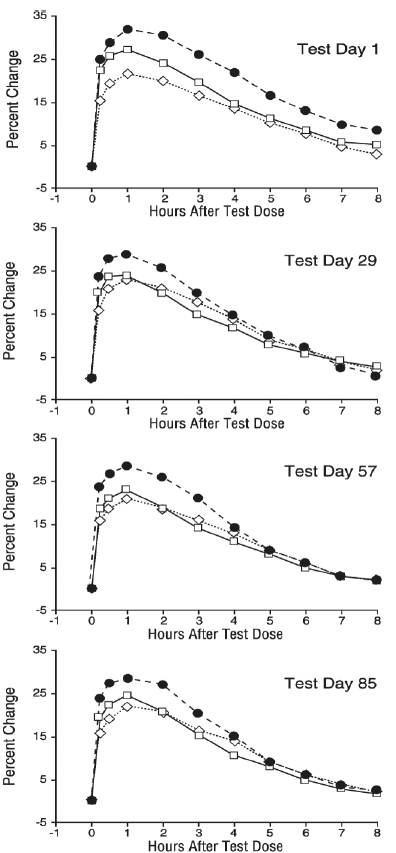
Nämä tutkimukset osoittivat, että Combivent®in (ipratropiumbromidi ja albuterolisulfaatti) inhalaatioaerosolin jokainen komponentti vaikutti yhdistelmän tuottamaan keuhkojen toiminnan paranemiseen, erityisesti ensimmäisten 4–5 tunnin aikana annostelun jälkeen, ja että COMBIVENT-inhalaatioaerosoli oli huomattavasti tehokkaampi. kuin ipratropiumbromidi tai albuterolisulfaatti yksinään annettuna.
Kahdessa kontrolloidussa 12 viikon tutkimuksessa COMBIVENT 50 mg inhalaatioaerosoli ei aiheuttanut muutoksia toissijaisissa tehokkuusparametreissa, mukaan lukien oirepisteet, lääkärin yleisarvioinnit ja aamun PEFR, joita kaikkia seurattiin koko tutkimusjakson ajan.
POTILASTIEDOT
Potilaan käyttöohjeet
Combivent® (ipratropiumbromidi ja albuterolisulfaatti) Hengitys Aerosoli
Lue täydelliset ohjeet huolellisesti ennen käyttöä
Käytä COMBIVENT 50 mg inhalaatioaerosolia juuri sen verran kuin lääkärisi on määrännyt. Älä muuta annostasi tai kuinka usein käytät COMBIVENT 20mcg inhalaatioaerosolia keskustelematta lääkärisi kanssa. Keskustele lääkärisi kanssa, jos sinulla on kysyttävää lääketieteellisestä tilastasi tai hoidostasi.
Kerro lääkärillesi kaikista käyttämistäsi lääkkeistä. COMBIVENT 50 mg inhalaatioaerosoli ja jotkut muut lääkkeet voivat olla yhteisvaikutuksia keskenään. Älä käytä muita inhaloitavia lääkkeitä COMBIVENT 20 mcg inhalaatioaerosolin kanssa, ellei lääkärisi ole niin määrännyt.
1. Aseta metallisäiliö suukappaleen läpinäkyvään päähän (katso kuva 1). Varmista, että säiliö on työnnetty kokonaan ja lujasti suukappaleeseen. COMBIVENT-inhalaatioaerosolisäiliötä saa käyttää vain COMBIVENT-inhalaatioaerosolisuukappaleen kanssa. Tätä suukappaletta ei saa käyttää muiden inhaloitavien lääkkeiden kanssa.
Kuvio 1 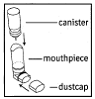
2. Poista oranssi pölysuojus. Jos suojus ei ole suukappaleessa, varmista ennen käyttöä, ettei suukappaleessa ole mitään. Parhaan tuloksen saavuttamiseksi kanisterin tulee olla huoneenlämpöinen ennen käyttöä.
3. Ravista ja testaa suihke. Suorita tämä vaihe ennen ensimmäistä käyttöä ja aina, kun aerosolia ei ole käytetty yli 24 tuntiin; muussa tapauksessa siirry suoraan vaiheeseen 4.
Kun säiliötä on ravistettu voimakkaasti vähintään 10 sekuntia (katso ravisteluohjeet kohdasta 4), "koesuihkuta" ilmaan 3 kertaa. Vältä roiskumista silmiin.
4. Ravista säiliötä voimakkaasti vähintään 10 sekuntia. Pidä säiliöstä kiinni kuvan 2 mukaisesti.
TÄRKEÄÄ: Voimakas ravistelu vähintään 10 sekuntia ennen jokaista ruiskutusta on erittäin tärkeää tuotteen oikeanlaisen suorituskyvyn kannalta.
Saat parhaat tulokset suorittamalla vaiheet 5 ja 6 30 sekunnin kuluessa säiliön ravistamisesta.
Kuva 2 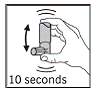
5. Hengitä ulos (hengitä) syvään suun kautta. Pidä säiliö pystyasennossa kuvan 3 mukaisesti peukalon ja sormien välissä, aseta suukappale suuhusi ja sulje huulesi. Pidä silmäsi kiinni, jotta lääkettä ei suihkuta silmiisi. Combivent® (ipratropiumbromidi ja albuterolisulfaatti) Inhalaatio Aerosoli voi aiheuttaa näön hämärtymistä, ahdaskulmaglaukooman tai tämän tilan pahenemista tai silmäkipua, jos lääkettä ruiskutetaan silmiin.
Kuva 3 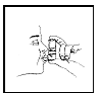
6. Hengitä sisään (hengitä) hitaasti suun kautta ja suihkuta samalla tuotetta suuhusi.
Suihkuta tuotetta painamalla säiliötä kerran lujasti suukappaletta vasten kuvan 4 mukaisesti. Jatka syvään hengittämistä.
Kuva 4 
7. Pidätä hengitystäsi 10 sekuntia, poista suukappale suustasi ja hengitä hitaasti ulos kuvan 5 mukaisesti.
Kuva 5 
8. Odota noin 2 minuuttia, ravista inhalaattoria voimakkaasti vähintään 10 sekuntia uudelleen (vaiheessa 4 kuvatulla tavalla) ja toista vaiheet 5–7.
9. Aseta oranssi pölysuojus takaisin paikoilleen käytön jälkeen.
10. Pidä suukappale puhtaana. Pese kuumalla vedellä. Jos käytät saippuaa, huuhtele huolellisesti puhtaalla vedellä. Kuivaa huolellisesti ennen käyttöä. Kun se on kuiva, aseta suukappaleen korkki takaisin, kun et käytä lääkevalmistetta.
11. Pidä kirjaa käytettyjen suihkeiden määrästä ja hävitä 200 ruiskutuksen jälkeen. Vaikka säiliö ei ole tyhjä, et voi olla varma lääkkeen määrästä jokaisessa suihkeessa 200 ruiskutuksen jälkeen.
12. Jos määräämäsi annoksesi ei helpota tai hengitysoireesi pahenevat, hakeudu välittömästi lääkärin hoitoon.
merkintä: Liittovaltion puhtaasta ilmaa koskeva laki edellyttää alla olevaa sisennettyä lausuntoa kaikilta kloorifluorihiilivetyjä (CFC-yhdisteitä) sisältäviltä tai niillä valmistetuilta tuotteilta:
Tämä tuote sisältää trikloorimonofluorimetaania (CFC-11), diklooridifluorimetaania (CFC-12) ja diklooritetrafluorietaania (CFC-114), aineita, jotka vahingoittavat ympäristöä tuhoamalla otsonia yläilmakehässä.
Combivent® (ipratropiumbromidi ja albuterolisulfaatti) inhalaatioaerosolin sisältö on paineen alaisena. Älä puhkaise säiliötä. Älä käytä tai säilytä lämmön tai avotulen lähellä. Altistuminen yli 120 °F:n lämpötiloille voi aiheuttaa halkeamia. Älä koskaan heitä säiliötä tuleen tai polttouuniin.
Pidä COMBIVENT Inhalation Aerosoli poissa lasten ulottuvilta.
Vältä roiskumista silmiin.
Osoita lääketieteellisiä tiedusteluja: http://us.boehringer-ingelheim.com, (800) 542-6257 tai (800) 459-9906 TTY.
Säilytä 25°C (77°F); retket sallittu 15°-30°C (59°-86°F) [katso USP-ohjattu huonelämpötila ]. Parhaan tuloksen saavuttamiseksi säilytä kanisteri huoneenlämmössä ennen käyttöä. Vältä liiallista kosteutta.
