Lanoxin 0.25mg Digoxin Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Lanoxin on ja miten sitä käytetään
Lanoxin 0,25 mg on reseptilääke, jota käytetään eteisvärinän ja sydämen vajaatoiminnan oireiden hoitoon. Lanoxin 0,25 mg voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Lanoksiini kuuluu lääkeluokkaan, jota kutsutaan antidysrythmics, V, Inotropic Agents.
Mitkä ovat Lanoxin 0,25mg:n mahdolliset sivuvaikutukset?
Lanoxin voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- pahoinvointi,
- oksentelua,
- ripuli,
- vatsakipu,
- nopea, hidas tai epätasainen syke,
- huimaus,
- veriset tai mustat, tervamaiset ulosteet,
- hämmennystä,
- heikkous,
- hallusinaatiot,
- epätavallisia ajatuksia tai käyttäytymistä,
- rintojen turvotus tai arkuus,
- näön hämärtyminen,
- kellastunut näkö,
- laihtuminen (lapsilla),
- kasvun viivästyminen (lapsilla) ja
- käyttäytymisen muutokset (lapsilla)
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Lanoxinin yleisimmät sivuvaikutukset ovat:
- pahoinvointi,
- ripuli,
- heikkous,
- huimaus,
- päänsärky,
- ahdistus,
- masennus ja
- ihottuma
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Lanoxinin mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
LANOXIN (digoksiini) on yksi sydämen (tai digitalis) glykosideista, läheisesti sukua oleva lääkeryhmä, jolla on yhteisiä spesifisiä vaikutuksia sydänlihakseen. Näitä lääkkeitä löytyy useista kasveista. Digoksiini uutetaan Digitalis lanata -kasvin lehdistä. Termiä "digitalis" käytetään kuvaamaan koko glykosidien ryhmää. Glykosidit koostuvat kahdesta osasta: sokerista ja kardenolidista (siis "glykosidit").
Digoksiini kuvataan kemiallisesti nimellä (3β,5β,12β)-3-[(O-2,6-dideoksi-β-D-ribo-heksopyranosyyli-(1→4)-O-2,6-dideoksi-β-D -ribo-heksopyranosyyli-(1->4)-2,6-dideoksi-p-D-riboheksopyranosyyli)oksi]-12,14-dihydroksi-card-20(22)-enolidi. Sen molekyylikaava on C41H64O14, sen molekyylipaino on 780,95 ja sen rakennekaava on:
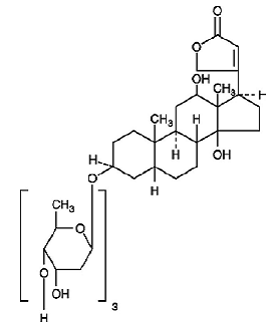
Digoksiini esiintyy hajuttomina valkoisina kiteinä, jotka sulavat ja hajoavat yli 230 °C:ssa. Lääke on käytännössä liukenematon veteen ja eetteriin; liukenee heikosti laimennettuun (50 %) alkoholiin ja kloroformiin; ja liukenee vapaasti pyridiiniin.
LANOXIN 0,25 mg injektio ja injektio Pediatric ovat steriilejä digoksiiniliuoksia suonensisäiseen tai lihaksensisäiseen injektioon. Ajoneuvo sisältää 40 % propyleeniglykolia ja 10 % alkoholia. Injektio puskuroidaan pH-arvoon 6,8-7,2 0,17 % kaksiemäksisellä natriumfosfaatilla ja 0,08 % vedettömällä sitruunahapolla. Jokainen 2 ml:n ampulli LANOXIN 0,25 mg -injektiota sisältää 500 mikrogrammaa (0,5 mg) digoksiinia (250 mikrogrammaa [0,25 mg] ml:aa kohti). Laimennusta ei vaadita. Jokainen 1 ml:n ampulli LANOXIN 0,25 mg Injection Pediatric -valmistetta sisältää 100 mikrogrammaa (0,1 mg) digoksiinia. Laimennusta ei vaadita.
INDIKAATIOT
Sydämen vajaatoiminta aikuisilla
LANOXIN 0,25 mg on tarkoitettu aikuisten lievän tai keskivaikean sydämen vajaatoiminnan hoitoon. LANOXIN lisää vasemman kammion ejektiofraktiota ja parantaa sydämen vajaatoiminnan oireita, mistä on osoituksena parantunut harjoituskyky ja vähentynyt sydämen vajaatoimintaan liittyvien sairaalahoitojen ja ensiapuhoito, mutta sillä ei ole vaikutusta kuolleisuuteen. LANOXIN 0,25 mg:aa tulee mahdollisuuksien mukaan käyttää yhdessä diureetin ja angiotensiinia konvertoivan entsyymin (ACE) estäjän kanssa.
Sydämen vajaatoiminta lapsipotilailla
LANOXIN lisää sydänlihaksen supistumiskykyä lapsipotilailla, joilla on sydämen vajaatoiminta.
Eteisvärinä aikuisilla
LANOXIN on tarkoitettu kammiovasteen säätelyyn aikuispotilailla, joilla on krooninen eteisvärinä.
ANNOSTELU JA HALLINNOINTI
Tärkeitä annostus- ja antotietoja
Valittaessa LANOXIN 0,25 mg -annostusohjelmaa on tärkeää ottaa huomioon tekijät, jotka vaikuttavat digoksiinipitoisuuksiin veressä (esim. ruumiinpaino, ikä, munuaisten toiminta, samanaikaiset lääkkeet), koska digoksiinin toksiset tasot ovat vain hieman korkeammat kuin terapeuttiset tasot. Annostelu voidaan aloittaa joko kyllästysannoksella, jota seuraa ylläpitoannostus, jos nopea titraus halutaan, tai aloittaa ylläpitoannoksella ilman kyllästysannosta.
Digoksiinin parenteraalista antoa tulee käyttää vain, kun nopean digitalisoinnin tarve on kiireellinen tai kun lääkettä ei voida ottaa suun kautta. Lihaksensisäinen injektio voi aiheuttaa voimakasta kipua pistoskohdassa, joten suonensisäinen anto on edullinen. Jos lääke on annettava lihakseen, se tulee ruiskuttaa syvälle lihakseen ja sen jälkeen hierontaa. Aikuisille ei saa pistää enempää kuin 500 mikrogrammaa LANOXIN 0,25 mg -injektiota yhteen kohtaan. Lapsipotilaille ei saa pistää enempää kuin 200 mikrogrammaa LANOXIN 0,25 mg Injection Pediatricia yhteen kohtaan.
Anna annos vähintään 5 minuutin ajan ja vältä bolusantoa systeemisen ja sepelvaltimon vasokonstriktion estämiseksi. LANOXIN 0,25 mg injektion ja injektion lasten sekoittamista muiden lääkkeiden kanssa samassa astiassa tai samanaikaista antoa samassa laskimoletkussa ei suositella.
LANOXIN 0,25 mg injektio ja injektio Pediatric voidaan antaa laimentamattomana tai laimennettuna vähintään 4-kertaisella tilavuudella steriiliä injektionesteisiin käytettävää vettä, 0,9 % natriumkloridi-injektiota tai 5 % dekstroosia. Alle 4-kertaisen laimennusaineen käyttö voi johtaa digoksiinin saostumiseen. Laimennetun tuotteen välitöntä käyttöä suositellaan.
Jos tuberkuliiniruiskuja käytetään hyvin pienten annosten mittaamiseen, älä huuhtele parenteraalisella liuoksella sen jälkeen, kun sen sisältö on työnnetty ulos kestoverisuonikatetriin, jotta vältetään digoksiinin liiallinen antaminen.
Harkitse LANOXIN-annoksen keskeyttämistä tai pienentämistä ennen sähköistä kardioversiota [katso VAROITUKSET JA VAROTOIMET ].
Ladattava annostusohjelma aikuisille ja lapsipotilaille
Ylläpitoannostelu aikuisille ja yli 10-vuotiaille lapsipotilaille
Ylläpitoannos perustuu laihaan painoon, munuaisten toimintaan, ikään ja samanaikaisiin tuotteisiin [katso KLIININEN FARMAKOLOGIA ].
Suositellut aloitusylläpitoannokset aikuisille ja yli 10-vuotiaille lapsipotilaille, joilla on normaali munuaisten toiminta, on annettu taulukossa 2. Annoksia voidaan suurentaa 2 viikon välein kliinisen vasteen, seerumin lääketasojen ja toksisuuden mukaan.
Taulukossa 3 esitetään suositeltu (kerran vuorokaudessa) ylläpitoannos aikuisille ja yli 10-vuotiaille lapsipotilaille (anna kerran päivässä) laihan painon ja munuaisten toiminnan mukaan. Annokset perustuvat tutkimuksiin aikuisilla sydämen vajaatoimintapotilailla. Vaihtoehtoisesti ylläpitoannos voidaan arvioida seuraavalla kaavalla (huippuvarastot menetetään joka päivä eliminaation kautta):
Kokonaisylläpitoannos = latausannos (eli huippuvarastot) x % päivittäinen menetys/100 (% päivittäinen menetys = 14 + kreatiniinipuhdistuma/5)
Pienennä LANOXIN-annosta potilailla, joiden laiha paino on epätavallisen pieni osa heidän kokonaispainostaan liikalihavuuden tai turvotuksen vuoksi.
Ylläpitoannostelu alle 10-vuotiaille lapsipotilaille
Aloitusylläpitoannos sydämen vajaatoiminnan hoitoon alle 10-vuotiailla lapsipotilailla perustuu laihaan painoon, munuaisten toimintaan, ikään ja samanaikaisiin tuotteisiin [ks. KLIININEN FARMAKOLOGIA ]. Lapsipotilaiden suositellut aloitusylläpitoannokset on annettu taulukossa 4. Näissä suosituksissa oletetaan, että munuaisten toiminta on normaali.
Taulukossa 5 esitetään keskimääräiset päivittäiset ylläpitoannokset alle 10-vuotiaille lapsipotilaille (annettava kahdesti päivässä), joilla on sydämen vajaatoiminta iän, laihaan painon ja munuaisten toiminnan perusteella.
Seuranta turvallisuuden, tehokkuuden ja terapeuttisten veriarvojen arvioimiseksi
Tarkkaile digoksiinitoksisuuden merkkejä ja oireita ja kliinistä vastetta. Säädä annosta toksisuuden, tehon ja veren pitoisuuksien perusteella.
Seerumin digoksiinipitoisuudet alle 0,5 ng/ml on yhdistetty tehon heikkenemiseen, kun taas yli 2 ng/ml tasot on yhdistetty lisääntyneeseen toksisuuteen ilman lisääntynyttä hyötyä.
Tulkitse seerumin digoksiinipitoisuutta yleisessä kliinisessä kontekstissa, äläkä käytä erillistä seerumin digoksiinipitoisuuden mittausta perustana LANOXIN-annoksen suurentamiseen tai pienentämiseen. Endogeeniset digoksiinin kaltaiset aineet voivat nostaa virheellisesti seerumin digoksiinipitoisuuksia [ks. HUUMEIDEN VUOROVAIKUTUKSET ]. Jos määritys on herkkä näille aineille, harkitse digoksiinin perustason saamista ennen LANOXIN-hoidon aloittamista ja hoidon jälkeisten arvojen korjaamista raportoidulla lähtötasolla.
Selvitä seerumin digoksiinipitoisuudet juuri ennen seuraavaa suunniteltua LANOXIN 0,25 mg -annosta tai vähintään 6 tuntia viimeisen annoksen jälkeen. Digoksiinipitoisuus on todennäköisesti 10-25 % pienempi, kun näyte otetaan juuri ennen seuraavaa annosta (24 tuntia annostelun jälkeen) verrattuna näytteenottoon 8 tunnin kuluttua annostelusta (käyttämällä kerta-annosta). Digoksiinipitoisuuksissa on kuitenkin vain pieniä eroja käytettäessä kahdesti vuorokaudessa tapahtuvaa annostusta riippumatta siitä, onko näytteenotto 8 vai 12 tuntia annoksen jälkeen.
Siirtyminen suonensisäisestä digoksiinista suun kautta otettavaan digoksiiniin
Kun vaihdat suonensisäisistä digoksiinivalmisteista suun kautta otettaviin, ota huomioon biologisen hyötyosuuden erot laskettaessa ylläpitoannoksia (katso taulukko 6).
MITEN TOIMITETAAN
Annostusmuodot ja vahvuudet
LANOXIN-injektio: Ampullit 500 mikrogrammaa (0,5 mg) 2 ml:ssa (250 mikrogrammaa [0,25 mg] per 1 ml).
LANOXIN 0,25 mg injektio Pediatric: Ampullit 100 mikrogrammaa (0,1 mg) 1 ml:ssa.
Varastointi ja käsittely
LANOXIN (digoksiini) -injektio, 500 mikrogrammaa (0,5 mg) 2 ml:ssa (250 mikrogrammaa [0,25 mg] ml:ssa); laatikko 10 ampullia ( NDC 70515 260 10)
LANOXIN (digoksiini) Injektio Pediatric, 100 mikrogrammaa (0,1 mg) 1 ml:ssa; laatikko 10 ampullia ( NDC 70515 262 10)
Säilytä 25 °C:ssa (77 °F); 15 °C - 30 °C (59 °F - 86 °F) [katso USP Controlled Room Temperature] ja suojattava valolta.
Valmistettu: Covis Pharma, Zug, 6300 Switzerland. Tarkistettu elokuussa 2018
SIVUVAIKUTUKSET
Seuraavat haittavaikutukset on sisällytetty tarkemmin etiketin Varoitukset ja varotoimet -osiossa:
- Sydämen rytmihäiriöt [katso VAROITUKSET JA VAROTOIMET ]
- Digoksiinimyrkyllisyys [katso VAROITUKSET JA VAROTOIMET ]
Kokemus kliinisistä kokeista
Koska kliiniset tutkimukset suoritetaan hyvin vaihtelevissa olosuhteissa, lääkkeen kliinisissä tutkimuksissa havaittuja haittavaikutuksia ei voida verrata suoraan toisen lääkkeen kliinisissä tutkimuksissa havaittuihin nopeuksiin, eivätkä ne välttämättä kuvasta kliinisissä käytännöissä havaittuja nopeuksia.
Yleensä LANOXIN 0,25 mg:n haittavaikutukset ovat annoksesta riippuvaisia ja niitä esiintyy suuremmilla annoksilla kuin mitä tarvitaan terapeuttisen vaikutuksen saavuttamiseksi. Tästä syystä haittavaikutukset ovat harvinaisempia, kun LANOXIN 0,25 mg:aa käytetään suositellulla annosalueella, pidetään terapeuttisella seerumin pitoisuudella ja kun samanaikaisiin lääkkeisiin ja tiloihin kiinnitetään erityistä huomiota.
DIG-tutkimuksessa (tutkimus, jossa tutkittiin digoksiinin vaikutusta kuolleisuuteen ja sairastuvuuteen sydämen vajaatoimintaa sairastavilla potilailla) sairaalahoidon ilmaantuvuus epäillyn digoksiinitoksisuuden vuoksi oli 2 % LANOXINia saaneilla potilailla verrattuna 0,9 % lumelääkettä saaneisiin potilaisiin [ks. Kliiniset tutkimukset ].
Digoksiinin haittavaikutusten yleisen ilmaantuvuuden on raportoitu olevan 5-20 %, ja 15-20 % haittavaikutuksista katsotaan vakaviksi. Sydäntoksisuus aiheuttaa noin puolet, maha-suolikanavan häiriöt noin neljänneksen ja keskushermosto- ja muu toksisuus noin neljänneksen näistä haittatapahtumista.
Ruoansulatuskanava
Pahoinvoinnin ja oksentelun lisäksi digoksiinin käyttöön on yhdistetty vatsakipuja, suoliston iskemiaa ja suoliston verenvuotonekroosia.
CNS
Digoksiini voi aiheuttaa päänsärkyä, heikkoutta, huimausta, apatiaa, sekavuutta ja mielenhäiriöitä (kuten ahdistusta, masennusta, deliriumia ja hallusinaatioita).
muu
Gynekomastiaa on ajoittain havaittu pitkäaikaisen digoksiinin käytön jälkeen. Trombosytopeniaa ja makulopapulaarista ihottumaa ja muita ihoreaktioita on havaittu harvoin.
HUUMEIDEN VUOROVAIKUTUKSET
Digoksiinilla on kapea terapeuttinen indeksi, ja seerumin digoksiinipitoisuuksien sekä mahdollisten kliinisen toksisuuden merkkien ja oireiden seuranta on tarpeen aloitettaessa, säädettäessä tai lopetettaessa lääkkeitä, joilla voi olla yhteisvaikutuksia digoksiinin kanssa. Lääkkeen määrääjien tulee tutustua kaikkien digoksiinin kanssa samanaikaisesti määrättyjen lääkkeiden reseptitietoihin saadakseen tietoja mahdollisista lääkkeiden yhteisvaikutuksista.
P-glykoproteiinin (PGP) indusoijat/inhibiittorit
Digoksiini on P-glykoproteiinin substraatti suolistosta imeytymisen, munuaistiehyen osan ja sapen ja suoliston erityksen tasolla. Siksi P-glykoproteiinia indusoivat/estävät lääkkeet voivat muuttaa digoksiinin farmakokinetiikkaa.
Farmakokineettiset lääkevuorovaikutukset
Farmakokineettisiä yhteisvaikutuksia on havaittu ja raportoitu ensisijaisesti, kun digoksiinia annetaan samanaikaisesti suun kautta. On hyvin vähän tutkimuksia, jotka ovat arvioineet lääkkeiden yhteisvaikutusta, kun digoksiinia annetaan IV-reittiä. Digoksiinialtistuksen muutoksen suuruus IV-reitin kautta on yleensä pienempi kuin suun kautta. Alla oleva taulukko sisältää saatavilla olevat interaktiotiedot käytettäessä digoksiini IV -formulaatiota (NA tarkoittaa, että ei ole saatavilla).
Mahdollisesti merkittävät farmakodynaamiset lääkevuorovaikutukset
Farmakodynaamisten yhteisvaikutusten suuren vaihtelun vuoksi digoksiinin annostus on yksilöitävä, kun potilaat saavat näitä lääkkeitä samanaikaisesti.
Lääke/laboratoriotestien vuorovaikutukset
Endogeeniset aineet, joiden koostumus on tuntematon (digoksiinin kaltaiset immunoreaktiiviset aineet [DLIS]) voivat häiritä tavallisia digoksiinin radioimmunomäärityksiä. Häiriö aiheuttaa useimmiten tulosten virheellisen positiivisen tai virheellisesti kohonneen, mutta joskus se aiheuttaa tulosten virheellisen pienenemisen. Jotkut määritykset ovat alttiimpia näille puutteille kuin toiset. Saatavilla on useita LC/MS/MS-menetelmiä, jotka saattavat olla vähemmän herkkiä DLIS-häiriöille. DLIS-soluja esiintyy jopa puolella vastasyntyneistä ja vaihteleva prosenttiosuus raskaana olevista naisista, hypertrofisesta kardiomyopatiasta kärsivistä potilaista, potilaista, joilla on munuaisten tai maksan vajaatoiminta, ja muita potilaita, joiden tilavuus on jostain syystä kasvanut. DLIS:n mitatut tasot (digoksiiniekvivalentteina) ovat yleensä alhaisia (0,2-0,4 ng/ml), mutta joskus ne saavuttavat tasoja, joita voitaisiin pitää terapeuttisina tai jopa myrkyllisinä.

Joissakin määrityksissä spironolaktoni, kanrenoni ja kaliumkanrenoaatti voidaan havaita virheellisesti digoksiiniksi pitoisuuksina 0,5 ng/ml asti. Jotkut perinteiset kiinalaiset ja ayurvedic-lääkkeet, kuten Chan Su, Siperian ginseng, Aasian ginseng, Ashwagandha tai Dashen, voivat aiheuttaa samanlaisia häiriöitä.
Spironolaktoni ja DLIS sitoutuvat paljon laajemmin proteiineihin kuin digoksiini. Tämän seurauksena spironolaktoni tai DLIS vaikuttavat vähemmän vapaan digoksiinipitoisuuden määrityksiin proteiinivapaassa ultrafiltraatissa (jotka ovat yleensä noin 25 % pienempiä kuin kokonaistasot, mikä vastaa tavanomaista proteiineihin sitoutumista). On huomattava, että ultrasuodatus ei ratkaise kaikkia vaihtoehtoisten lääkkeiden häiriöongelmia. LC/MS/MS-menetelmän käyttö voi olla parempi vaihtoehto sen tuottamien hyvien tulosten perusteella, erityisesti spesifisyyden ja kvantisointirajan kannalta.
VAROITUKSET
Mukana osana VAROTOIMENPITEET osio.
VAROTOIMENPITEET
Kammiovärinä potilailla, joilla on lisä-AV-tie (Wolff-Parkinson-White-oireyhtymä)
Wolff-Parkinson-Whiten oireyhtymää sairastavilla potilailla, joille kehittyy eteisvärinä, on suuri kammiovärinän riski. Näiden potilaiden hoito digoksiinilla johtaa suurempaan johtumisen hidastumiseen eteiskammiosolmukkeessa kuin lisäreiteissä, ja näin ollen riskit nopeasta kammiovasteesta, joka johtaa kammiovärinään, lisääntyvät.
Sinusbradykardia ja sino-eteiskatkos
LANOXIN voi aiheuttaa vakavaa sinusbradykardiaa tai sinoatriaalikatkosta erityisesti potilailla, joilla on aiemmin ollut sinussolmussairaus, ja se voi aiheuttaa pitkälle edenneen tai täydellisen sydänkatkoksen potilailla, joilla on jo epätäydellinen AV-katkos. Harkitse sydämentahdistimen asentamista ennen digoksiinihoitoa.
Digoksiini toksisuus
Digoksiinimyrkytyksen merkkejä ja oireita ovat anoreksia, pahoinvointi, oksentelu, näkömuutokset ja sydämen rytmihäiriöt [ensimmäisen asteen, toisen asteen (Wenckebach) tai kolmannen asteen sydänkatkos (mukaan lukien asystolia); eteistakykardia ja esto; AV dissosiaatio; kiihtynyt solmurytmi; unifokaaliset tai monimuotoiset kammioiden ennenaikaiset supistukset (erityisesti iso- tai kolmiulotteiset supistukset); kammiotakykardia; ja kammiovärinä]. Toksisuus liittyy yleensä digoksiinipitoisuuksiin, jotka ovat yli 2 ng/ml, vaikka oireita voi esiintyä myös alhaisemmilla tasoilla. Alhainen paino, korkea ikä tai munuaisten vajaatoiminta, hypokalemia, hyperkalsemia tai hypomagnesemia voivat altistaa digoksiinitoksuudelle. Hanki seerumin digoksiinitasot potilailla, joilla on digoksiinihoidon merkkejä tai oireita, ja keskeytä tai säädä annosta tarvittaessa [ks. HAITTAVAIKUTUKSET ja YLIANNOSTUS ]. Arvioi seerumin elektrolyytit ja munuaisten toiminta säännöllisesti.
Varhaisin ja yleisin digoksiinitoksisuuden ilmentymä imeväisille ja lapsille on sydämen rytmihäiriöiden ilmaantuminen, mukaan lukien sinusbradykardia. Lapsilla digoksiinin käyttö voi aiheuttaa rytmihäiriöitä. Yleisimpiä ovat johtumishäiriöt tai supraventrikulaariset takyarytmiat, kuten eteistakykardia (katkosten kanssa tai ilman) ja liitostakykardia (solmuperäinen) takykardia. Ventrikulaariset rytmihäiriöt ovat harvinaisempia. Sinusbradykardia voi olla merkki uhkaavasta digoksiinimyrkytyksestä erityisesti pikkulapsilla, vaikka ensimmäisen asteen sydänkatkos puuttuisikin. Kaikki rytmihäiriöt tai sydämen johtumishäiriöt, jotka kehittyvät digoksiinia saavalle lapselle, on aluksi oletettava digoksiinimyrkytyksen seurauksena.
Koska aikuispotilailla, joilla on sydämen vajaatoiminta, on joitakin yhteisiä oireita digoksiinitoksisuuden kanssa, voi olla vaikeaa erottaa digoksiinitoksisuutta sydämen vajaatoiminnasta. Niiden etiologian virheellinen tunnistaminen saattaa saada kliinikon jatkamaan tai lisäämään LANOXIN-annosta, vaikka annostelu olisi itse asiassa keskeytettävä. Jos näiden merkkien ja oireiden etiologia ei ole selvä, mittaa seerumin digoksiinitaso.
Ventrikulaaristen rytmihäiriöiden riski sähköisen kardioversion aikana
Saattaa olla toivottavaa pienentää LANOXIN-annosta tai lopettaa LANOXIN-hoito 1-2 päivän ajaksi ennen eteisvärinän sähköistä kardioversiota, jotta vältetään kammiorytmihäiriöt, mutta lääkäreiden on otettava huomioon kammiovasteen lisääntymisen seuraukset, jos digoksiinia vähennetään tai lopetetaan. Jos epäillään digitalistoksisuutta, elektiivistä kardioversiota tulee lykätä. Jos kardioversion viivyttäminen ei ole järkevää, tulee valita mahdollisimman alhainen energiataso, jotta vältytään kammiorytmihäiriöiltä.
Iskemian riski potilailla, joilla on akuutti sydäninfarkti
LANOXIN 0,25 mg:n käyttöä ei suositella potilaille, joilla on akuutti sydäninfarkti, koska digoksiini voi lisätä sydänlihaksen hapen tarvetta ja johtaa iskemiaan.
Vasokonstriktio potilailla, joilla on sydänlihastulehdus
LANOXIN 0,25 mg voi aiheuttaa vasokonstriktiota ja edistää tulehdusta edistävien sytokiinien tuotantoa; siksi vältä käyttöä potilailla, joilla on sydänlihastulehdus.
Sydämen tehon heikkeneminen potilailla, joilla on säilynyt vasemman kammion systolinen toiminta
Potilailla, joilla on sydämen vajaatoiminta, johon liittyy säilynyt vasemman kammion ejektiofraktio, sydämen minuuttitilavuus saattaa heikentyä LANOXINin käytön yhteydessä. Tällaisia sairauksia ovat restriktiivinen kardiomyopatia, supistava perikardiitti, amyloidinen sydänsairaus ja akuutti cor pulmonale. Potilailla, joilla on idiopaattinen hypertrofinen subaorttastenoosi, ulosvirtauksen esto voi pahentua digoksiinin inotrooppisten vaikutusten vuoksi. Potilaat, joilla on amyloidinen sydänsairaus, voivat olla alttiimpia digoksiinitoksuudelle terapeuttisilla tasoilla, koska digoksiini sitoutuu lisääntyneeseen solunulkoisiin amyloidifibrilleihin.
LANOXIN 0,25 mg:n käyttöä tulee yleensä välttää näillä potilailla, vaikka sitä on käytetty kammionopeuden säätelyyn eteisvärinää sairastavien potilaiden alaryhmässä.
Vähentynyt teho potilailla, joilla on hypokalsemia
Hypokalsemia voi mitätöidä digoksiinin vaikutukset ihmisillä; näin ollen digoksiini voi olla tehoton, kunnes seerumin kalsium on palautunut normaaliksi. Nämä yhteisvaikutukset liittyvät siihen tosiasiaan, että digoksiini vaikuttaa sydämen supistumiskykyyn ja kiihtyvyyteen samalla tavalla kuin kalsium.
Muuttunut vaste kilpirauhashäiriöissä ja hypermetabolisissa tiloissa
Kilpirauhasen vajaatoiminta voi vähentää digoksiinin tarvetta.
Sydämen vajaatoiminta ja/tai eteisrytmihäiriöt, jotka johtuvat hypermetabolisista tai hyperdynaamisista tiloista (esim. hypertyreoosi, hypoksia tai arteriovenoosinen shuntti), voidaan parhaiten hoitaa puuttumalla taustalla olevaan sairauteen. Hypermetabolisiin tiloihin liittyvät eteisen rytmihäiriöt ovat erityisen resistenttejä digoksiinihoidolle. Potilaat, joilla on beri beri -sydänsairaus, eivät välttämättä reagoi riittävästi digoksiiniin, jos taustalla olevaa tiamiinin puutetta ei hoideta samanaikaisesti.
Ei-kliininen toksikologia
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Digoksiini ei osoittanut genotoksisuutta in vitro -tutkimuksissa (Ames-testi ja hiiren lymfooma). Tietoja digoksiinin karsinogeenisuudesta ei ole saatavilla, eikä sen mahdollisuutta vaikuttaa hedelmällisyyteen ole tutkittu.
Käyttö tietyissä populaatioissa
Raskaus
Raskausluokka C
LANOXIN 0,25 mg tulee antaa raskaana olevalle naiselle vain, jos se on selvästi tarpeen. Ei myöskään tiedetä, voiko digoksiini aiheuttaa sikiövaurioita, kun sitä annetaan raskaana olevalle naiselle, tai voiko se vaikuttaa lisääntymiskykyyn. Digoksiinilla ei ole tehty lisääntymistutkimuksia eläimillä.
Työ ja toimitus
Kliinisistä tutkimuksista ei ole riittävästi tietoa digoksiinin turvallisuuden ja tehon määrittämiseksi synnytyksen ja synnytyksen aikana.
Imettävät äidit
Tutkimukset ovat osoittaneet, että digoksiini jakautuu äidinmaitoon ja että maidon ja seerumin pitoisuussuhde on noin 0,6-0,9. Imetettävän lapsen arvioitu altistuminen digoksiinille imetyksen aikana on kuitenkin paljon pienempi kuin tavallinen imeväisten ylläpitoannos. Siksi tällä määrällä ei pitäisi olla farmakologista vaikutusta lapseen.
Käyttö lapsille
LANOXINin turvallisuutta ja tehokkuutta kammioiden nopeuden säätelyssä ei ole osoitettu eteisvärinää sairastavilla lapsilla.
LANOXINin turvallisuutta ja tehokkuutta lasten sydämen vajaatoiminnan hoidossa ei ole osoitettu riittävissä ja hyvin kontrolloiduissa tutkimuksissa. Kuitenkin julkaistussa kirjallisuudessa lapsista, joilla on eri syistä johtuva sydämen vajaatoiminta (esim. kammioiden väliseinän vauriot, antrasykliinitoksisuus, avoin valtimotiehyt), digoksiinihoito on yhdistetty hemodynaamisten parametrien ja kliinisten merkkien ja oireiden paranemiseen.
Vastasyntyneiden vauvojen digoksiinin sietokyky vaihtelee huomattavasti. Keskoset ja epäkypsät lapset ovat erityisen herkkiä digoksiinin vaikutuksille, ja lääkkeen annosta ei pidä vain pienentää, vaan se on yksilöitävä heidän kypsyysasteensa mukaan.
Geriatrinen käyttö
Suurin osa digoksiinista saaduista kliinisistä kokemuksista on saatu iäkkäillä potilailla. Tämä kokemus ei ole osoittanut eroja vasteessa tai haittavaikutuksissa iäkkäiden ja nuorempien potilaiden välillä. Tämän lääkkeen tiedetään kuitenkin erittyvän olennaisesti munuaisten kautta, ja tämän lääkkeen toksisten reaktioiden riski voi olla suurempi potilailla, joilla on heikentynyt munuaisten toiminta. Koska iäkkäillä potilailla on todennäköisemmin heikentynyt munuaisten toiminta, on oltava varovainen annoksen valinnassa, jonka tulisi perustua munuaisten toimintaan, ja munuaisten toiminnan seuranta voi olla hyödyllistä [ks. ANNOSTELU JA HALLINNOINTI ].
Munuaisten vajaatoiminta
Digoksiinin puhdistuma voidaan ensisijaisesti korreloida munuaisten toiminnan kanssa, kuten kreatiniinipuhdistuma osoittaa. Taulukoissa 3 ja 5 esitetään digoksiinin tavanomaiset päivittäiset ylläpitoannokset kreatiniinipuhdistuman perusteella [ks. ANNOSTELU JA HALLINNOINTI ].
Digoksiini erittyy pääasiassa munuaisten kautta; siksi potilaat, joilla on munuaisten vajaatoiminta, tarvitsevat tavallista pienempiä ylläpitoannoksia digoksiinia [ks ANNOSTELU JA HALLINNOINTI ]. Pidentyneen eliminaation puoliintumisajan vuoksi tarvitaan pidempi aika saavuttaakseen seerumin alkuperäisen tai uuden vakaan tilan pitoisuuden munuaisten vajaatoimintaa sairastavilla potilailla kuin potilailla, joilla on normaali munuaisten toiminta. Jos digoksiiniannoksen pienentämisestä ei huolehdita asianmukaisesti, tällaisilla potilailla on suuri toksisuuden riski, ja toksiset vaikutukset kestävät näillä potilailla pidempään kuin potilailla, joiden munuaisten toiminta on normaali.
Maksan vajaatoiminta
Plasman digoksiinipitoisuudet akuuttia hepatiittia sairastavilla potilailla ovat yleensä terveiden koehenkilöiden ryhmän profiilien alueella.
Imeytymishäiriö
Digoksiinin imeytyminen heikkenee joissakin imeytymishäiriöissä, kuten kroonisessa ripulissa.
YLIANNOSTUS
Merkit ja oireet aikuisilla ja lapsilla
Toksisuuden merkit ja oireet ovat yleensä samankaltaisia kuin aiemmin kuvatut [katso HAITTAVAIKUTUKSET ], mutta voi esiintyä useammin ja voi olla vakavampaa. Digoksiinitoksisuuden merkit ja oireet yleistyvät yli 2 ng/ml tasoilla. Kuitenkin päätettäessä, johtuvatko potilaan oireet digoksiinista, kliininen tila sekä seerumin elektrolyyttitasot ja kilpirauhasen toiminta ovat tärkeitä tekijöitä [ks. ANNOSTELU JA HALLINNOINTI ].
Aikuiset
Yleisimmät digoksiinitoksisuuden merkit ja oireet ovat pahoinvointi, oksentelu, ruokahaluttomuus ja väsymys, joita esiintyy 30–70 %:lla yliannostuspotilaista. Erittäin korkeat seerumipitoisuudet aiheuttavat hyperkalemiaa erityisesti potilailla, joilla on heikentynyt munuaisten toiminta. Melkein kaikentyyppiset sydämen rytmihäiriöt on yhdistetty digoksiinin yliannostukseen, ja useat rytmihäiriöt ovat yleisiä samalla potilaalla. Sydänvaikutusten huippu ilmaantuu 3-6 tuntia nielemisen jälkeen ja voi kestää 24 tuntia tai pidempään. Rytmihäiriöitä, joita pidetään tyypillisempänä digoksiinimyrkyllisyydelle, ovat uusi Mobitzin tyypin 1 AV-katkos, kiihtyneet liitosrytmit, ei-paroksysmaalinen eteistakykardia AV-katkoksen kanssa ja kaksisuuntainen kammiotakykardia. Asystolan tai kammiovärinän aiheuttama sydämenpysähdys on yleensä kohtalokas. Digoksiinitoksisuus liittyy seerumin pitoisuuteen. Koska digoksiinipitoisuudet seerumissa nousevat yli 1,2 ng/ml:n, haittavaikutukset voivat lisääntyä. Lisäksi alhaisemmat kaliumpitoisuudet lisäävät haittavaikutusten riskiä. Aikuisilla, joilla on sydänsairaus, kliiniset havainnot viittaavat siihen, että 10–15 mg:n digoksiinin yliannostus johtaa puoleen potilaiden kuolemaan. Yli 25 mg:n annos, jonka sai aikuinen, jolla ei ole sydänsairautta, näytti olevan tasaisesti tappava, jos Digoxin Immune Fab (DIGIBIND®, DIGIFAB®) ei annettu.
Sydämen ulkopuolisista ilmenemismuodoista maha-suolikanavan oireet (esim. pahoinvointi, oksentelu, ruokahaluttomuus) ovat hyvin yleisiä (jopa 80 % ilmaantuvuus) ja edeltävät sydänoireita noin puolella potilaista useimmissa kirjallisuusraporteissa. Neurologiset oireet (esim. huimaus, erilaiset keskushermoston häiriöt), väsymys ja huonovointisuus ovat hyvin yleisiä. Visuaalisia ilmenemismuotoja voi esiintyä myös yleisimmin värinäön poikkeavuuksina (keltaisen vihreän hallitseva). Neurologiset ja visuaaliset oireet voivat jatkua, kun muut myrkyllisyyden merkit ovat hävinneet. Kroonisessa toksisuudessa epäspesifiset sydämen ulkopuoliset oireet, kuten huonovointisuus ja heikkous, voivat olla vallitsevia.
Lapset
Lapsipotilailla toksisuuden merkkejä ja oireita voi ilmetä digoksiiniannoksen aikana tai pian sen jälkeen. Usein esiintyvät ei-sydänvaikutukset ovat samanlaisia kuin aikuisilla, vaikka pahoinvointia ja oksentelua ei todeta usein imeväisillä ja pienillä lapsipotilailla. Muita raportoituja yliannostuksen ilmenemismuotoja ovat laihtuminen vanhemmissa ikäryhmissä, vauvojen menestymisen epäonnistuminen, suoliliepeen valtimoiskemian aiheuttama vatsakipu, uneliaisuus ja käyttäytymishäiriöt, mukaan lukien psykoottiset jaksot. Aikuisilla potilailla esiintyviä rytmihäiriöitä ja rytmihäiriöiden yhdistelmiä voi esiintyä myös lapsipotilailla, vaikka sinustakykardiaa, supraventrikulaarista takykardiaa ja nopeaa eteisvärinää havaitaan harvemmin lapsipotilailla. Lapsipotilaille kehittyy todennäköisemmin AV johtumishäiriöitä tai sinusbradykardiaa. Digoksiinilla hoidetun lapsen rytmihäiriöiden on katsottava liittyvän digoksiiniin, kunnes toisin suljetaan pois. Kliiniset havainnot viittaavat siihen, että 1–3-vuotiailla lapsipotilailla, joilla ei ole sydänsairautta, 6–10 mg:n digoksiinin yliannostus johtaisi puoleen potilaiden kuolemaan. Samassa populaatiossa yli 10 mg:n annos johti kuolemaan, jos Digoxin Immune Fab -valmistetta ei annettu.
Hoito
Krooninen yliannostus
Jos epäilet myrkyllisyyttä, lopeta LANOXIN 0,25 mg:n käyttö ja aseta potilas sydänmonitoriin. Oikeat tekijät, kuten elektrolyyttihäiriöt, kilpirauhasen toimintahäiriö ja samanaikaiset lääkkeet [ks. ANNOSTELU JA HALLINNOINTI ]. Korjaa hypokalemia antamalla kaliumia siten, että seerumin kaliumpitoisuus pysyy välillä 4,0-5,5 mmol/l. Kaliumia annetaan yleensä suun kautta, mutta jos rytmihäiriön korjaaminen on kiireellistä ja seerumin kaliumpitoisuus on alhainen, kalium voidaan antaa suonensisäisesti. Tarkkaile elektrokardiogrammia kaliumtoksisuuden varalta (esim. T-aaltojen huippuunsa) ja tarkkaile vaikutusta rytmihäiriöön. Vältä kaliumsuoloja potilailla, joilla on bradykardia tai sydänkatkos. Oireisia rytmihäiriöitä voidaan hoitaa Digoxin Immune Fab -valmisteella.
Akuutti yliannostus
Potilaiden, jotka ovat tahallaan tai vahingossa niellyt suuria annoksia digoksiinia, tulee saada aktiivihiiltä suun kautta tai nenä-mahaletkun kautta riippumatta nauttimisesta kuluneesta ajasta, koska digoksiini kiertää suolistossa enterohepaattisen verenkierron kautta. Sydämen seurannan lisäksi LANOXIN-hoito on keskeytettävä väliaikaisesti, kunnes haittavaikutus häviää. Oikeat tekijät, jotka voivat vaikuttaa haittavaikutuksiin [katso VAROITUKSET JA VAROTOIMET ]. Erityisesti korjaa hypokalemia ja hypomagnesemia. Digoksiini ei poistu tehokkaasti elimistöstä dialyysillä sen suuren ekstravaskulaarisen jakautumistilavuuden vuoksi. Henkeä uhkaavat rytmihäiriöt (kammiotakykardia, kammiovärinä, korkea-asteinen AV-katkos, bradyarrytma, sinuspysähdys) tai hyperkalemia edellyttävät Digoxin Immune Fab -valmisteen antamista. Digoxin Immune Fabin on osoitettu olevan 80–90 % tehokas poistamaan digoksiinitoksisuuden merkkejä ja oireita. Digoksiinin aiheuttama bradykardia ja sydäntukokset ovat parasympaattisesti välittämiä ja reagoivat atropiiniin. Väliaikaista sydämentahdistinta voidaan myös käyttää. Ventrikulaariset rytmihäiriöt voivat reagoida lidokaiiniin tai fenytoiiniin. Kun suuri määrä digoksiinia on nautittu, erityisesti potilailla, joilla on munuaisten vajaatoiminta, voi esiintyä hyperkalemiaa, joka johtuu kaliumin vapautumisesta luurankolihaksista. Tässä tapauksessa Digoxin Immune Fab -hoito on aiheellista; glukoosi- ja insuliinihoito voi olla tarpeen, jos hyperkalemia on hengenvaarallinen. Kun haittavaikutus on hävinnyt, LANOXIN 0,25 mg -hoito voidaan aloittaa uudelleen annoksen huolellisen uudelleenarvioinnin jälkeen.
VASTA-AIHEET
LANOXIN on vasta-aiheinen potilailla, joilla on:
- Kammiovärinä [katso VAROITUKSET JA VAROTOIMET ]
- Tunnettu yliherkkyys digoksiinille (näkyviä reaktioita ovat selittämätön ihottuma, suun, huulten tai kurkun turvotus tai hengitysvaikeudet). Yliherkkyysreaktio muille digitalisvalmisteille on yleensä vasta-aihe digoksiinille.
KLIININEN FARMAKOLOGIA
Toimintamekanismi
Kaikki digoksiinin vaikutukset välittyvät sen vaikutuksista Na-K ATPaasiin. Tämä entsyymi, "natriumpumppu", on vastuussa solunsisäisen ympäristön ylläpitämisestä koko kehossa siirtämällä natriumioneja pois soluista ja kaliumioneja soluihin. Estämällä Na-K ATPaasi, digoksiini
- lisää solunsisäisen kalsiumin saatavuutta sydänlihaksessa ja johtumisjärjestelmässä, mikä lisää inotropiaa, lisää automaattisuutta ja pienentää johtumisnopeutta
- aiheuttaa epäsuorasti autonomisen hermoston parasympaattista stimulaatiota, millä on seurauksellisia vaikutuksia sinoatriaaliseen (SA) ja eteiskammioon (AV)
- vähentää katekoliamiinin takaisinottoa hermopäätteissä, mikä tekee verisuonista herkempiä endogeenisille tai eksogeenisille katekoliamiineille
- lisää baroreseptorien herkistymistä, mikä lisää kaulavaltimoontelohermotoimintaa ja tehostaa sympaattista vetäytymistä missä tahansa keskimääräisen valtimopaineen nousussa
- lisää (korkeammilla pitoisuuksilla) sympaattista ulosvirtausta keskushermostosta (CNS) sekä sydämen että perifeerisiin sympaattisiin hermoihin
- mahdollistaa (korkeammilla pitoisuuksilla) solunsisäisen kaliumin progressiivisen ulosvirtauksen, mikä lisää seerumin kaliumtasoja.
Näiden suorien ja epäsuorien vaikutusten kardiologisia seurauksia ovat sydänlihaksen systolisen supistumisen voiman ja nopeuden lisääntyminen (positiivinen inotrooppinen vaikutus), sydämen sykkeen hidastuminen (negatiivinen kronotrooppinen vaikutus), AV-solmun läpi tapahtuvan johtumisnopeuden väheneminen ja lasku. sympaattisen hermoston ja reniini-angiotensiinijärjestelmän aktivaatioasteella (neurohormonaalinen deaktivoiva vaikutus).
Farmakodynamiikka
Ajat LANOXIN-valmisteiden farmakologisen vaikutuksen alkamiseen ja huippuvaikutuksen saavuttamiseen on esitetty taulukossa 7.
Hemodynaamiset vaikutukset
Lyhyt- ja pitkäkestoinen hoito lääkkeellä lisää sydämen minuuttitilavuutta ja alentaa keuhkovaltimon painetta, keuhkokapillaarin kiilapainetta ja systeemistä verisuonten vastusta sydämen vajaatoimintapotilailla. Näihin hemodynaamisiin vaikutuksiin liittyy vasemman kammion ejektiofraktion kasvu ja loppusystolisten ja loppudiastolisten mittojen pieneneminen.
EKG:n muutokset
Terapeuttisten LANOXIN-annosten käyttö voi aiheuttaa PR-välin pidentymistä ja ST-segmentin laskua EKG:ssa. LANOXIN voi aiheuttaa vääriä positiivisia ST-T-muutoksia EKG:ssa rasitustestin aikana. Nämä sähköfysiologiset vaikutukset eivät ole osoitus toksisuudesta. LANOXIN ei laske merkittävästi sykettä harjoituksen aikana.
Farmakokinetiikka
Huomautus: Seuraavat tiedot ovat aikuisilla tehdyistä tutkimuksista, ellei toisin mainita.
LANOXINin oraalisten valmisteiden systeemisen saatavuuden ja vastaavien annosten vertailut on esitetty taulukossa 6 [ks. ANNOSTELU JA HALLINNOINTI ].
Jakelu
Lääkkeen annon jälkeen havaitaan 6-8 tunnin kudos jakautumisvaihe. Tätä seuraa lääkkeen seerumipitoisuuden aleneminen paljon asteittaisemmin, mikä riippuu digoksiinin eliminaatiosta elimistöstä. Seerumin pitoisuus-aikakäyrän varhaisen osan (absorptio/jakaantumisvaiheet) huippukorkeus ja kaltevuus riippuvat antoreitistä ja formulaation imeytymisominaisuuksista. Kliiniset todisteet osoittavat, että varhaiset korkeat seerumipitoisuudet eivät heijasta digoksiinin pitoisuutta sen vaikutuskohdassa, mutta että pitkäaikaisessa käytössä vakaan tilan jakautumisen jälkeiset seerumipitoisuudet ovat tasapainossa kudospitoisuuksien kanssa ja korreloivat farmakologisten vaikutusten kanssa. Yksittäisillä potilailla nämä jakautumisen jälkeiset seerumipitoisuudet voivat olla hyödyllisiä arvioitaessa terapeuttisia ja toksisia vaikutuksia [ks. ANNOSTELU JA HALLINNOINTI ].
Digoksiini keskittyy kudoksiin ja siksi sillä on suuri näennäinen jakautumistilavuus (noin 475-500 l). Digoksiini läpäisee sekä veri-aivoesteen että istukan. Synnytyksen aikana seerumin digoksiinipitoisuus vastasyntyneellä on samanlainen kuin äidin seerumin pitoisuus. Noin 25 % plasman digoksiinista sitoutuu proteiineihin. Seerumin digoksiinipitoisuudet eivät merkittävästi muutu suuret muutokset rasvakudoksen painossa, joten sen jakautumistila korreloi parhaiten laihan (eli ihanteellisen) ruumiinpainon, ei kokonaispainon kanssa.
Aineenvaihdunta
Vain pieni osa (13 %) digoksiiniannoksesta metaboloituu terveillä vapaaehtoisilla. Virtsan metaboliitit, joihin kuuluvat dihydrodigoksiini, digoksigeniinibisdigitoksosidi ja niiden glukuronidi- ja sulfaattikonjugaatit, ovat luonteeltaan polaarisia, ja niiden oletetaan muodostuvan hydrolyysin, hapettumisen ja konjugoinnin kautta. Digoksiinin metabolia ei ole riippuvainen sytokromi P-450 -järjestelmästä, eikä digoksiinin tiedetä indusoivan tai estävän sytokromi P-450 -järjestelmää.
Erittyminen
Digoksiinin eliminaatio noudattaa ensimmäisen asteen kinetiikkaa (eli milloin tahansa eliminoituvan digoksiinin määrä on verrannollinen kehon kokonaispitoisuuteen). Terveille vapaaehtoisille suonensisäisen annon jälkeen 50–70 % digoksiiniannoksesta erittyy muuttumattomana virtsaan. Digoksiinin erittyminen munuaisten kautta on verrannollinen kreatiniinipuhdistumaan ja on suurelta osin riippumaton virtsan virtauksesta. Terveillä vapaaehtoisilla, joilla on normaali munuaisten toiminta, digoksiinin puoliintumisaika on 1,5-2 päivää. Anuriapotilaiden puoliintumisaika on pidennetty 3,5-5 päivään. Digoksiinia ei poisteta tehokkaasti elimistöstä dialyysin, vaihtotransfuusion tai kardiopulmonaalisen ohituksen aikana, koska suurin osa lääkkeestä sitoutuu ekstravaskulaarisiin kudoksiin.
Erikoispopulaatiot
Geriatria
Ikääntymiseen liittyvän munuaisten toiminnan heikkenemisen vuoksi iäkkäiden potilaiden odotetaan eliminoituvan digoksiinista hitaammin kuin nuorempien potilaiden. Iäkkäillä potilailla digoksiinin jakautumistilavuus voi myös olla pienempi ikääntymisestä johtuvan vähärasvaisen lihasmassan vähenemisen vuoksi. Näin ollen digoksiinin annos on valittava huolellisesti ja sitä on seurattava iäkkäillä potilailla [katso Käyttö tietyissä populaatioissa ].
Sukupuoli
Tutkimuksessa, johon osallistui 184 potilasta, digoksiinin puhdistuma oli 12 % pienempi naisilla kuin miehillä. Tämä ero ei todennäköisesti ole kliinisesti merkittävä.
Maksan vajaatoiminta
Koska vain pieni osa (noin 13 %) digoksiiniannoksesta metaboloituu, maksan vajaatoiminnan ei odoteta merkittävästi muuttavan digoksiinin farmakokinetiikkaa. Pienessä tutkimuksessa plasman digoksiinipitoisuusprofiilit akuuttia hepatiittia sairastavilla potilailla olivat yleensä terveiden koehenkilöiden ryhmän profiilien rajoissa. Annoksen muuttamista ei suositella potilaille, joilla on maksan vajaatoiminta; seerumin digoksiinipitoisuuksia tulee kuitenkin käyttää tarpeen mukaan annostelun ohjaamiseksi näille potilaille.
Munuaisten vajaatoiminta
Koska digoksiinin puhdistuma korreloi kreatiniinipuhdistuman kanssa, munuaisten vajaatoimintaa sairastavilla potilailla on yleensä pidentynyt digoksiinin eliminaation puoliintumisaika ja suurempi altistus digoksiinille. Sen vuoksi titraa näillä potilailla huolellisesti kliinisen vasteen ja seerumin digoksiinipitoisuuksien seurannan perusteella tarvittaessa.
Rotu
Rotuerojen vaikutusta digoksiinin farmakokinetiikkaan ei ole virallisesti tutkittu. Koska digoksiini eliminoituu pääasiassa muuttumattomana lääkkeenä munuaisten kautta ja koska kreatiniinin puhdistumassa ei ole merkittäviä eroja rotujen välillä, rodusta johtuvia farmakokineettisiä eroja ei odoteta.
Kliiniset tutkimukset
Krooninen sydämen vajaatoiminta
Kahteen 12 viikon kaksoissokkoutettuun lumekontrolloituun tutkimukseen osallistui 178 (RADIANCE-tutkimus) ja 88 (PROVED-tutkimus) aikuispotilasta, joilla oli NYHA-luokan II tai III sydämen vajaatoiminta ja joita oli aiemmin hoidettu suun kautta otettavalla digoksiinilla, diureetilla ja ACE:n estäjällä (RADIANCE). vain) ja satunnaistettiin saamaan lumelääkettä tai hoitoa LANOXIN-tableteilla. Molemmat tutkimukset osoittivat, että LANOXIN-hoitoon satunnaistettujen potilaiden kuntoilukyky säilyi paremmin. LANOXIN-hoidon jatkaminen vähensi sydämen vajaatoiminnan pahenemisen riskiä, mistä ovat osoituksena sydämen vajaatoimintaan liittyvät sairaalahoidot ja ensiapu sekä samanaikaisen sydämen vajaatoiminnan hoidon tarve.
LANOXIN 0,25 mg:n DIG-koe potilailla, joilla on sydämen vajaatoiminta
Digitalis Investigation Groupin (DIG) päätutkimus oli 37 viikkoa kestänyt, satunnaistettu, kaksoissokkokuolleisuustutkimus, jossa digoksiinia verrattiin lumelääkkeeseen 6 800 aikuispotilaalla, joilla oli sydämen vajaatoiminta ja vasemman kammion ejektiofraktio alle tai yhtä suuri kuin 0,45. Satunnaistamisen yhteydessä 67 % oli NYHA-luokan I tai II luokkaa, 71 %:lla oli iskeeminen etiologia sydämen vajaatoiminta, 44 % oli saanut digoksiinia ja useimmat saivat samanaikaisesti ACE:n estäjää (94 %) ja diureetteja (82 %). Kuten yllä kuvatuissa pienemmissä tutkimuksissa, potilaat, jotka olivat saaneet avoimia digoksiinia, poistettiin tästä hoidosta ennen satunnaistamista. Satunnaistaminen digoksiiniin liittyi jälleen sairaalahoidon ilmaantuvuuden merkittävään vähenemiseen riippumatta siitä, laskettiinko se sydämen vajaatoiminnan vuoksi sairaalahoitojen lukumääränä (suhteellinen riski 75 %), riskinä joutua ainakin yhteen tällaiseen sairaalahoitoon tutkimuksen aikana (RR 72 %) tai sairaalahoitojen määrä mistä tahansa syystä (RR 94 %). Toisaalta satunnaistamisella digoksiiniin ei ollut ilmeistä vaikutusta kuolleisuuteen (RR 99 %, luotettavuusrajat 91-107 %).
Krooninen eteisvärinä
Digoksiinia on myös tutkittu keinona kontrolloida kammiovastetta krooniseen eteisvärinään aikuisilla. Digoksiini alensi leposykettä, mutta ei sykettä harjoituksen aikana.
Kolmessa eri satunnaistetussa kaksoissokkotutkimuksessa, joihin osallistui yhteensä 315 aikuispotilasta, digoksiinia verrattiin lumelääkkeeseen äskettäin alkaneen eteisvärinän muuntamiseksi sinusrytmiksi. Konversio oli yhtä todennäköistä ja yhtä nopeaa digoksiini- ja lumeryhmässä. Satunnaistetussa 120 potilaan tutkimuksessa, jossa verrattiin digoksiinia, sotalolia ja amiodaronia, digoksiiniin satunnaistetuilla potilailla oli alhaisin ilmaantuvuus sinusrytmiin ja vähiten tyydyttävä nopeuskontrolli, kun konversiota ei tapahtunut.
Ainakin yhdessä tutkimuksessa digoksiinia tutkittiin keinona viivyttää eteisvärinän palautumista aikuispotilailla, joilla tämä rytmihäiriö uusiutuu usein. Tämä oli satunnaistettu, kaksoissokkoutettu, 43 potilaan ristikkäistutkimus. Digoksiini pidensi oireiden toistuvien episodien välistä keskimääräistä aikaa 54 %, mutta sillä ei ollut vaikutusta jatkuvan elektrokardiografisen seurannan aikana havaittujen fibrillaatiojaksojen esiintymistiheyteen.
POTILASTIEDOT
- Kerro potilaille, että digoksiinia käytetään sydämen vajaatoiminnan ja sydämen rytmihäiriöiden hoitoon.
- Neuvo potilaita ottamaan tätä lääkettä ohjeiden mukaisesti.
- Kerro potilaille, että monet lääkkeet voivat olla vuorovaikutuksessa LANOXINin kanssa. Neuvo potilaita ilmoittamaan lääkärilleen ja apteekkiin, jos he käyttävät reseptivapaita lääkkeitä, mukaan lukien kasviperäisiä lääkkeitä, tai jos he saavat uuden reseptin.
- Kerro potilaalle, että verikokeita tarvitaan sen varmistamiseksi, että hänen LANOXIN 0,25 mg -annos on hänelle sopiva.
- Neuvo potilaita ottamaan yhteyttä lääkäriin tai terveydenhuollon ammattilaiseen, jos heillä on pahoinvointia, oksentelua, jatkuvaa ripulia, sekavuutta, heikkoutta tai näköhäiriöitä (mukaan lukien näön hämärtyminen, vihreä-keltaiset värihäiriöt, haloefekti), koska nämä voivat olla merkkejä siitä, että annos LANOXIN voi olla liian korkea.
- Kertokaa vanhempia tai huoltajia siitä, että liian korkeiden LANOXIN-annosten oireita voi olla vaikea tunnistaa imeväisillä ja lapsipotilailla. Oireet, kuten laihtuminen, vauvojen menestymisen epäonnistuminen, vatsakipu ja käyttäytymishäiriöt voivat olla merkkejä digoksiinitoksisuudesta.
- Neuvo potilasta seuraamaan ja kirjaamaan sykettä ja verenpainetta päivittäin.
- Neuvo hedelmällisessä iässä olevia naisia, jotka tulevat tai suunnittelevat raskautta, keskustelemaan lääkärin kanssa ennen LANOXIN-hoidon aloittamista tai jatkamista.
