Cartia XT 180mg Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Cartia on ja miten sitä käytetään?
Cartia on reseptilääke, jota käytetään rintakivun (angina pectoris), korkean verenpaineen (hypertension), paroksysmaalisen supraventrikulaarisen takykardian ja eteisvärinän (flutter) oireiden hoitoon. Cartiaa voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Cartia kuuluu lääkeryhmään nimeltä Antidysrythmics, IV; Kalsiumkanavan salpaajat; Kalsiumkanavasalpaajat, ei-dihydropyridiini.
Mitkä ovat Cartian mahdolliset sivuvaikutukset?
Cartia voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- rintakipu,
- hitaat sydämenlyönnit,
- sykkivät sydämenlyönnit,
- lepattaa rinnassasi,
- huimaus,
- turvotus,
- nopea painonnousu,
- hengenahdistus,
- kuume,
- kipeä kurkku,
- palavat silmät,
- ihokipu ja
- punainen tai violetti ihottuma, johon liittyy rakkuloita ja hilseilyä
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Cartian yleisimpiä sivuvaikutuksia ovat:
- lievä päänsärky,
- lievä huimaus ja
- vilustumisoireet (nenän tukkoisuus, aivastelu, kurkkukipu)
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Cartian mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
Diltiatsemihydrokloridi on kalsiumionien soluvirtauksen estäjä (hidaskanavan salpaaja tai kalsiumin antagonisti). Kemiallisesti diltiatseemihydrokloridi on 1,5-bentsotiatsepin-4(5H)oni,3-(asetyylioksi)-5-[2-(dimetyyliamino)etyyli]-2,3-dihydro-2-(4-metoksifenyyli)-, monohydrokloridi ,(+)-cis-. Kemiallinen rakenne on:
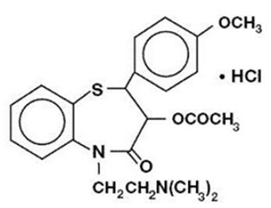
Diltiatsemihydrokloridi on valkoinen tai luonnonvalkoinen kiteinen jauhe, jolla on karvas maku. Se liukenee veteen, metanoliin ja kloroformiin. Sen molekyylipaino on 450,98. Diltiatsemihydrokloridin pitkitetysti vapauttava kapseli (kerran vuorokausiannos) on muotoiltu kerran päivässä annettavaksi pitkittyvästi vapautuvaksi kapseliksi, joka sisältää 120 mg, 180 mg, 240 mg tai 300 mg diltiatseemihydrokloridia.
Lisäksi jokainen kapseli sisältää seuraavat inaktiiviset aineosat: asetyylitributyylisitraatti, ammoniometakrylaattikopolymeeri-NF, D & C Red #28, D & C Yellow #10, D & C Yellow #10 Aluminum Lake, etyyliselluloosa, FD & C Blue #1 Aluminium Lake, FD & C Blue #2 Aluminium Lake, FD & C Red #40, FD & C Red #40 Aluminium Lake, gelatiini-NF, magnesiumstearaatti, metakryylihappokopolymeeri-NF, propyleeniglykoli, polysorbaatti 80-NF, tärkkelys , sakkaroosi, talkki USP ja titaanidioksidi. 180 mg ja 240 mg kapselit sisältävät keltaista rautaoksidia. Lisäksi 240 mg:n kapseli sisältää myös mustaa rautaoksidia ja punaista rautaoksidia.
Suun kautta annettavaksi.
Tämä lääke täyttää USP Drug Release 9:n.
INDIKAATIOT
Diltiatsemihydrokloridin pitkittyvästi vapauttavat kapselit USP (kerran päivässä annostelu) on tarkoitettu verenpaineen hoitoon. Sitä voidaan käyttää yksinään tai yhdessä muiden verenpainetta alentavien lääkkeiden kanssa.
Diltiatsemihydrokloridin pitkittyvästi vapauttavat kapselit USP (kerran päivässä annostelu) on tarkoitettu kroonisen stabiilin angina pectoris ja sepelvaltimon kouristuksen aiheuttaman angina pectoriksen hoitoon.
ANNOSTELU JA HALLINNOINTI
Potilaat, joita hoidetaan pelkällä diltiatseemilla tai yhdistelmänä muiden lääkkeiden kanssa, voidaan vaihtaa diltiatseemihydrokloridin pitkittyvästi vapauttaviin kapseleihin USP (kerran vuorokaudessa annettava annos) lähimmällä vastaavalla päiväannoksella. Joillakin potilailla voidaan tarvita suurempia annoksia diltiatseemihydrokloridin pitkittyvästi vapauttavia kapseleita USP (kerran päivässä annostus). Potilaita tulee seurata tarkasti. Myöhempi titraus suurempiin tai pienempiin annoksiin saattaa olla tarpeen, ja se tulee aloittaa kliinisesti perustellun mukaisesti. Yli 360 mg:n annoksilla on rajoitetusti yleistä kliinistä kokemusta, mutta 540 mg:n annoksia on tutkittu kliinisissä tutkimuksissa. Sivuvaikutusten ilmaantuvuus lisääntyy annoksen kasvaessa, kun ensimmäisen asteen AV-katkos, huimaus ja sinusbradykardia ovat vahvimmin sidoksissa annokseen.
Hypertensio
Annostus on sovitettava titraamalla potilaan yksilöllisten tarpeiden mukaan. Kun sitä käytetään monoterapiana, kohtuulliset aloitusannokset ovat 180–240 mg kerran vuorokaudessa, vaikka jotkut potilaat saattavat reagoida pienempiin annoksiin. Suurin verenpainetta alentava vaikutus havaitaan yleensä 14 päivän kroonisessa hoidossa; siksi annoksen muuttaminen tulee suunnitella vastaavasti. Tavallinen kliinisissä tutkimuksissa tutkittu annosalue oli 240-360 mg kerran vuorokaudessa. Yksittäiset potilaat voivat reagoida suurempiin annoksiin, jopa 480 mg kerran vuorokaudessa.
Angina pectoris
Angina pectoriksen hoitoon käytettävät annokset on sovitettava kunkin potilaan tarpeiden mukaan alkaen annoksesta 120 tai 180 mg kerran vuorokaudessa. Yksittäiset potilaat voivat reagoida suurempiin annoksiin, jopa 480 mg kerran vuorokaudessa. Tarvittaessa titraus voidaan suorittaa 7-14 päivän aikana.
Diltiazem Hydrochloride pitkävaikutteiset kapselit USP (kerran päivässä annostus)
Samanaikainen käyttö muiden sydän- ja verisuonilääkkeiden kanssa
MITEN TOIMITETAAN
HUOMAA: TUOTTEE VOI OLLA HAJU.
Varastointiolosuhteet
Säilytä 20° - 25°C (68° - 77°F) [Katso USP-ohjattu huonelämpötila ].
Vältä liiallista kosteutta.
Annostele tiiviiseen, valonkestävään astiaan USP:n mukaisesti.
Valmistaja: Actavis Laboratories FL, Inc., Fort Lauderdale, FL 33314 USA. Jakelija: Actavis Pharma, Inc., Parsippany, NJ 07054 USA. Tarkistettu: joulukuuta 2014
SIVUVAIKUTUKSET
Vakavat haittavaikutukset ovat olleet harvinaisia tähän mennessä tehdyissä tutkimuksissa, mutta on otettava huomioon, että potilaat, joilla on heikentynyt kammiotoiminta ja sydämen johtumishäiriöt, on yleensä jätetty näiden tutkimusten ulkopuolelle.
Seuraavassa taulukossa esitetään yleisimmät haittavaikutukset, jotka on raportoitu lumekontrolloiduissa angina- ja hypertensiotutkimuksissa potilailla, jotka saivat diltiatseemihydrokloridin pitkitetysti vapauttavaa kapselivalmistetta (kerran vuorokaudessa annosteltuna) enintään 360 mg:n annokseen asti, ja lumelääkepotilaiden luvut on esitetty vertailun vuoksi.
Diltiazem Hydrochloride Depotkapseli (kerran päivässä) Plasebokontrolloidut angina- ja hypertensiotutkimukset yhdistettynä
Kliinisissä tutkimuksissa diltiatseemihydrokloridia pitkitetysti vapauttavista kapseleista (kerta-annostus), diltiatseemihydrokloriditableteista ja diltiatseemihydrokloridi-pitkivaikutteisista kapseleista, joihin osallistui yli 3 200 potilasta, yleisimmät tapahtumat (eli yli 1 %) olivat turvotus (4,6 %). , päänsärky (4,6 %), huimaus (3,5 %), voimattomuus (2,6 %), ensimmäisen asteen AV-katkos (2,4 %), bradykardia (1,7 %), punoitus (1,4 %), pahoinvointi (1,4 %) ja ihottuma ( 1,2 %).
Lisäksi seuraavia tapahtumia raportoitiin harvoin (alle 1 %) angina- tai verenpainetutkimuksissa:
Sydän: Angina pectoris, rytmihäiriöt, AV-katkos (toisen tai kolmannen asteen), nipun haarakatkos, kongestiivinen sydämen vajaatoiminta, EKG:n poikkeavuudet, hypotensio, sydämentykytys, pyörtyminen, takykardia, kammion ekstrasystolit.
Hermosto: Epänormaalit unet, muistinmenetys, masennus, kävelyhäiriöt, hallusinaatiot, unettomuus, hermostuneisuus, parestesia, persoonallisuuden muutos, uneliaisuus, tinnitus, vapina.
Ruoansulatuskanava: Anoreksia, ummetus, ripuli, suun kuivuminen, dysgeusia, dyspepsia, lievä SGOT-, SGPT-, LDH- ja alkalisen fosfataasin nousu (ks. VAROITUKSET , Akuutti maksavaurio ), jano, oksentelu, painon nousu.
Ihotauti: Petekiat, valoherkkyys, kutina, urtikaria.
Muuta: Amblyopia, CPK:n nousu, hengenahdistus, nenäverenvuoto, silmien ärsytys, hyperglykemia, hyperurikemia, impotenssi, lihaskrampit, nenän tukkoisuus, nokturia, nivelkipu, polyuria, seksuaaliset vaikeudet.
Seuraavia markkinoille tulon jälkeisiä tapahtumia on raportoitu harvoin diltiatseemia saaneilla potilailla: akuutti yleistynyt eksantematoottinen pustuloosi, allergiset reaktiot, hiustenlähtö, angioedeema (mukaan lukien kasvojen tai periorbitaalinen turvotus), asystolia, erythema multiforme (mukaan lukien Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi), eksfoliatiivinen dermatiitti , ekstrapyramidaaliset oireet, ienhyperplasia, hemolyyttinen anemia, pidentynyt verenvuotoaika, leukopenia, valoherkkyys (mukaan lukien jäkälän keratoosi ja hyperpigmentaatio auringonvalossa), purppura, retinopatia, myopatia ja trombosytopenia. Lisäksi on havaittu tapahtumia, kuten sydäninfarkti, joita ei voida helposti erottaa näiden potilaiden taudin luonnollisesta historiasta. Useita hyvin dokumentoituja yleistynyttä ihottumaa, joista osa on luonnehdittu leukosytoklastiseksi vaskuliitiksi, on raportoitu. Lopullista syy-seuraussuhdetta näiden tapahtumien ja diltiatseemihoidon välillä ei kuitenkaan ole vielä selvitetty.
Jos haluat ilmoittaa EPÄILLEISTÄ HAITTAVAIKUTUKSISTA, ota yhteyttä Actavikseen numeroon 1-800-272-5525 tai FDA:han numeroon 1-800-FDA-1088 tai www.fda.gov/medwatch.
HUUMEIDEN VUOROVAIKUTUKSET
Mahdollisten additiivisten vaikutusten vuoksi varovaisuutta ja huolellista titrausta on syytä noudattaa potilailla, jotka saavat diltiatseemia samanaikaisesti muiden aineiden kanssa, joiden tiedetään vaikuttavan sydämen supistumiskykyyn ja/tai johtumiseen (ks. VAROITUKSET ). Farmakologiset tutkimukset osoittavat, että beetasalpaajia tai digitalista käytettäessä samanaikaisesti diltiatseemin kanssa voi olla additiivinen vaikutus AV johtumisen pidentämiseen (ks. VAROITUKSET ).
Kuten kaikkien lääkkeiden kohdalla, varovaisuutta on noudatettava hoidettaessa potilaita useilla lääkkeillä. Diltiatsemi on sekä sytokromi P-450 3A4 -entsyymijärjestelmän substraatti että estäjä. Muilla lääkkeillä, jotka ovat tämän entsyymijärjestelmän spesifisiä substraatteja, estäjiä tai indusoijia, voi olla merkittävä vaikutus diltiatseemin tehoon ja sivuvaikutusprofiiliin. Potilaat, jotka käyttävät muita lääkkeitä, jotka ovat CYP450 3A4:n substraatteja, ja erityisesti potilaat, joilla on munuaisten ja/tai maksan vajaatoiminta, saattavat tarvita annoksen muuttamista aloitettaessa tai lopetettaessa samanaikainen diltiatseemihoito optimaalisen terapeuttisen veren tason ylläpitämiseksi.
Anestesia-aineet
Kalsiumkanavasalpaajat voivat tehostaa sydämen supistumiskykyä, johtavuutta ja automaattisuutta sekä anestesia-aineisiin liittyvää verisuonten laajentumista. Kun anestesia-aineita ja kalsiuminsalpaajia käytetään samanaikaisesti, ne tulee titrata huolellisesti.
Bentsodiatsepiinit
Tutkimukset osoittivat, että diltiatseemi suurensi midatsolaamin ja triatsolaamin AUC-arvoa 3-4-kertaiseksi ja Cmax-arvoa 2-kertaiseksi lumelääkkeeseen verrattuna. Midatsolaamin ja triatsolaamin eliminaation puoliintumisaika piteni myös (1,5-2,5-kertaiseksi), kun niitä annettiin samanaikaisesti diltiatseemin kanssa. Nämä farmakokineettiset vaikutukset, jotka havaitaan diltiatseemin samanaikaisen annon aikana, voivat lisätä sekä midatsolaamin että triatsolaamin kliinisiä vaikutuksia (esim. pitkittynyt sedaatio).
Beetasalpaajat
Kontrolloidut ja kontrolloimattomat kotimaiset tutkimukset viittaavat siihen, että diltiatseemin ja beetasalpaajien samanaikainen käyttö on yleensä hyvin siedettyä, mutta saatavilla olevat tiedot eivät riitä ennustamaan samanaikaisen hoidon vaikutuksia potilailla, joilla on vasemman kammion toimintahäiriö tai sydämen johtumishäiriö.
Diltiatsemihydrokloridin samanaikainen antaminen propranololin kanssa viidelle normaalille vapaaehtoiselle johti propranololipitoisuuden nousuun kaikilla koehenkilöillä ja propranololin biologinen hyötyosuus kasvoi noin 50 %. In vitro diltiatseemi näyttää syrjäyttävän propranololin sitoutumiskohdistaan. Jos yhdistelmähoito aloitetaan tai lopetetaan yhdessä propranololin kanssa, propranololin annoksen muuttaminen saattaa olla perusteltua (ks. VAROITUKSET ).
Buspironi
Yhdeksällä terveellä koehenkilöllä diltiatseemi suurensi merkittävästi buspironin keskimääräistä AUC-arvoa 5,5-kertaiseksi ja Cmax-arvoa 4,1-kertaiseksi lumelääkkeeseen verrattuna. Diltiatseemi ei vaikuttanut merkittävästi buspironin T½- ja Tmax-arvoihin. Buspironin tehostuneet vaikutukset ja toksisuus voivat olla mahdollisia käytettäessä samanaikaisesti diltiatseemin kanssa. Myöhemmät annoksen muuttaminen voi olla tarpeen samanaikaisen käytön aikana, ja sen tulee perustua kliiniseen arviointiin.
Karbamatsepiini
Diltiatseemin ja karbamatsepiinin samanaikaisen käytön on raportoitu nostaneen seerumin karbamatsepiinin pitoisuuksia (nousu 40 % - 72 %), mikä joissakin tapauksissa aiheuttaa toksisuutta. Potilaita, jotka saavat näitä lääkkeitä samanaikaisesti, tulee tarkkailla mahdollisen lääkevuorovaikutuksen varalta.
Simetidiini
Kuudella terveellä vapaaehtoisella tehdyssä tutkimuksessa on osoitettu merkittävän nousun diltiatseemin huippupitoisuuksissa plasmassa (58 %) ja käyrän alapuolella (53 %) viikon mittaisen simetidiinihoidon jälkeen 1 200 mg:lla päivässä ja kerta-annoksella diltiatseemi 60 mg. Ranitidiini aiheutti pienempiä, ei-merkittäviä lisäyksiä. Vaikutus saattaa johtua siitä, että simetidiini estää maksan sytokromi P-450:n, diltiatseemin ensikierron metaboliasta vastaavan entsyymijärjestelmän. Tällä hetkellä diltiatseemihoitoa saavia potilaita tulee tarkkailla huolellisesti farmakologisen vaikutuksen muutosten varalta, kun simetidiinihoito aloitetaan ja lopetetaan. Diltiatseemiannoksen muuttaminen saattaa olla perusteltua.
Klonidiini
Sinusbradykardiaa, joka on johtanut sairaalahoitoon ja sydämentahdistimen asettamiseen, on raportoitu klonidiinin käytön yhteydessä diltiatseemin kanssa. Seuraa sykettä potilailla, jotka saavat samanaikaisesti diltiatseemia ja klonidiinia.
Syklosporiini
Farmakokineettinen yhteisvaikutus diltiatseemin ja siklosporiinin välillä on havaittu tutkimuksissa, joihin osallistui munuais- ja sydämensiirtopotilaita. Munuais- ja sydämensiirtopotilailla siklosporiinin annosta oli pienennettävä 15–48 %, jotta siklosporiinin vähimmäispitoisuudet säilyisivät samanlaisina kuin ennen diltiatseemin lisäämistä. Jos näitä aineita annetaan samanaikaisesti, siklosporiinipitoisuuksia on seurattava, erityisesti kun diltiatseemihoito aloitetaan, sitä muutetaan tai lopetetaan.
Siklosporiinin vaikutusta diltiatseemin pitoisuuksiin plasmassa ei ole arvioitu.
Digitalis
Digoksiinin ja diltiatseemin antaminen 24 terveelle mieshenkilölle nosti plasman digoksiinipitoisuuksia noin 20 %. Toinen tutkija ei löytänyt digoksiinitasojen nousua 12 potilaalla, joilla oli sepelvaltimotauti. Koska digoksiinitasojen vaikutuksesta on saatu ristiriitaisia tuloksia, on suositeltavaa, että digoksiinipitoisuuksia seurataan diltiatseemihoitoa aloitettaessa, säädettäessä ja lopetettaessa mahdollisen liiallisen tai alidigitalisoinnin välttämiseksi (ks. VAROITUKSET ).
Kinidiini
Diltiatsemi lisää merkittävästi kinidiinin AUC(0-→)-arvoa 51 %, T½ 36 % ja pienentää sen oraalista CL:tä 33 %. Kinidiinin haittavaikutusten seuranta voi olla perusteltua ja annosta muuttaa vastaavasti.
Rifampiini
Rifampiinin samanaikainen anto diltiatseemin kanssa alensi diltiatseemipitoisuudet plasmassa havaitsemattomille tasoille. Diltiatsemin ja rifampiinin tai minkä tahansa tunnetun CYP3A4-induktorin samanaikaista käyttöä tulee välttää mahdollisuuksien mukaan ja harkita vaihtoehtoista hoitoa.
Statiinit
Diltiatsemi on CYP3A4:n estäjä, ja sen on osoitettu suurentavan merkittävästi joidenkin statiinien AUC-arvoa. CYP3A4:n kautta metaboloituvien statiinien myopatian ja rabdomyolyysin riski voi lisääntyä, jos diltiatseemia käytetään samanaikaisesti. Jos mahdollista, käytä CYP3A4-metaboloitumatonta statiinia yhdessä diltiatseemin kanssa; Muussa tapauksessa tulee harkita sekä diltiatseemin että statiinin annoksen muuttamista sekä tarkkaa tarkkailua statiiniin liittyvien haittatapahtumien merkkien ja oireiden varalta.
Terveessä vapaaehtoisessa ristikkäistutkimuksessa (N=10) simvastatiinin kerta-annoksen 20 mg anto samanaikaisesti 120 mg kahdesti vuorokaudessa diltiatseemi SR:n kanssa johti simvastatiinin keskimääräisen AUC-arvon 5-kertaiseen nousuun verrattuna simvastatiiniin. yksin. Koehenkilöillä, joilla oli suurentunut keskimääräinen vakaan tilan altistus diltiatseemille, simvastatiinialtistus moninkertaistui. Tietokonepohjaiset simulaatiot osoittivat, että päivittäisellä 480 mg:n diltiatseemiannoksella voidaan odottaa 8-9-kertaista keskimääräistä simvastatiinin AUC-arvon nousua. Jos simvastatiinin ja diltiatseemin samanaikainen anto on tarpeen, rajaa simvastatiinin vuorokausiannos 10 mg:aan ja diltiatseemin 240 mg:aan.
Kymmenen henkilön satunnaistetussa, avoimessa, 4-suuntaisessa ristikkäistutkimuksessa diltiatseemin (120 mg kahdesti vuorokaudessa diltiatseemi SR 2 viikon ajan) samanaikainen anto lovastatiinin 20 mg:n kerta-annoksen kanssa johti 3-4-kertaiseen keskiarvon nousuun. lovastatiinin AUC ja verrattuna pelkkään lovastatiiniin. Samassa tutkimuksessa ei havaittu merkitsevää muutosta 20 mg:n kerta-annoksen pravastatiinin AUC-arvossa eikä diltiatseemin samanaikaisen annon aikana. Lovastatiini tai pravastatiini eivät vaikuttaneet merkittävästi diltiatseemipitoisuuksiin plasmassa.
VAROITUKSET
Sydämen johtuminen
Diltiatsemi pidentää AV-solmukkeen refraktaarisia jaksoja pidentämättä merkittävästi sinussolmun palautumisaikaa, paitsi potilailla, joilla on sairas sinusoireyhtymä. Tämä vaikutus voi harvoin johtaa epänormaalin hitaaseen sykeen (erityisesti potilailla, joilla on sairas poskiontelooireyhtymä) tai toisen tai kolmannen asteen AV-salpaukseen (13 potilaalla 3290:stä eli 0,40 %). Diltiatseemin samanaikainen käyttö beetasalpaajien tai digitaliksen kanssa voi aiheuttaa additiivisia vaikutuksia sydämen johtumiseen. Potilaalle, jolla oli Prinzmetalin angina pectoris, kehittyi asystoliajaksoja (2–5 sekuntia) 60 mg:n kerta-annoksen jälkeen diltiatseemia (ks. HAITTAVAIKUTUKSET ).
Sydämen vajaatoiminta
Vaikka diltiatseemilla on negatiivinen inotrooppinen vaikutus eristettyihin eläinkudosvalmisteisiin, hemodynaamiset tutkimukset ihmisillä, joilla on normaali kammiotoiminta, eivät ole osoittaneet sydänindeksin laskua eikä johdonmukaisia negatiivisia vaikutuksia supistumiskykyyn (dp/dt). Akuutti tutkimus suun kautta otettavasta diltiatseemista potilailla, joilla oli heikentynyt kammiotoiminta (ejektiofraktio 24 % ± 6 %), osoitti kammioiden toiminnan indeksien paranemista ilman merkittävää supistumistoiminnan heikkenemistä (dp/dt). Kongestiivisen sydämen vajaatoiminnan pahenemista on raportoitu potilailla, joilla on aiempaa heikentynyt kammiotoiminta. Kokemus diltiatseemihydrokloridin käytöstä yhdessä beetasalpaajien kanssa potilailla, joilla on heikentynyt kammiotoiminta, on rajoitettu. Tätä yhdistelmää käytettäessä tulee noudattaa varovaisuutta.
Hypotensio
Diltiatseemihoitoon liittyvä verenpaineen lasku voi joskus johtaa oireiseen hypotensioon.
Akuutti maksavaurio
Kliinisissä tutkimuksissa on havaittu lievää transaminaasiarvojen nousua sekä samanaikaisesti alkalisen fosfataasin ja bilirubiinin nousua tai ilman. Tällaiset nousut olivat yleensä ohimeneviä ja hävisivät usein jopa diltiatseemihoidon jatkuessa. Harvinaisissa tapauksissa on havaittu merkittäviä entsyymien, kuten alkalisen fosfataasin, LDH:n, SGOT:n, SGPT:n, kohoamista ja muita akuutin maksavaurion aiheuttamia ilmiöitä. Näillä reaktioilla oli taipumus ilmaantua aikaisin hoidon aloittamisen jälkeen (1-8 viikkoa) ja ne ovat palautuneet lääkehoidon lopettamisen jälkeen. Suhde diltiatseemiin on joissakin tapauksissa epävarma, mutta joissain tapauksissa todennäköinen (ks VAROTOIMENPITEET ).
VAROTOIMENPITEET
Kenraali
Diltiatsemihydrokloridi metaboloituu laajalti maksassa ja erittyy munuaisten ja sappeen. Kuten minkä tahansa pidempiaikaisen lääkkeen kohdalla, munuaisten ja maksan toiminnan laboratorioparametreja tulee seurata säännöllisin väliajoin. Lääkettä tulee käyttää varoen potilailla, joilla on munuaisten tai maksan vajaatoiminta. Subakuuteissa ja kroonisissa koirilla ja rotilla tehdyissä tutkimuksissa, joiden tarkoituksena oli aiheuttaa toksisuutta, suuriin diltiatseemiannoksiin liittyi maksavaurioita. Erityisissä subakuuteissa maksatutkimuksissa suun kautta annetut 125 mg/kg:n tai suuremmat annokset rotilla liittyivät histologisiin muutoksiin maksassa, jotka palautuivat, kun lääke lopetettiin. Koirilla annokset 20 mg/kg liittyivät myös maksan muutoksiin; nämä muutokset kuitenkin korjautuivat annostelua jatkettaessa.
Dermatologiset tapahtumat (ks HAITTAVAIKUTUKSET voi olla ohimenevää ja hävitä diltiatseemin jatkuvasta käytöstä huolimatta. Harvoin on kuitenkin raportoitu myös ihottumia, jotka etenevät erythema multiformeksi ja/tai eksfoliatiiviseksi dermatiitiksi. Jos dermatologinen reaktio jatkuu, lääke on lopetettava.
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Rotilla tehdyssä 24 kuukautta kestäneessä tutkimuksessa suun kautta annetuilla annoksilla enintään 100 mg/kg/vrk ja 21 kuukauden tutkimuksessa hiirillä suun kautta annetuilla annostasoilla enintään 30 mg/kg/vrk ei havaittu todisteita karsinogeenisuudesta. Mutageenisia vasteita ei myöskään havaittu in vitro tai in vivo nisäkässolumäärityksissä tai in vitro bakteereissa. Mitään viitteitä hedelmällisyyden heikkenemisestä ei havaittu uros- ja naarasrotilla tehdyssä tutkimuksessa oraalisilla annoksilla 100 mg/kg/vrk asti.
Raskaus
Luokka C. Lisääntymistutkimuksia on suoritettu hiirillä, rotilla ja kaniineilla. Viidestä kymmeneen kertaa suurempien annosten antaminen (mg/kg perusteella) kuin päivittäinen suositeltu terapeuttinen annos on johtanut alkio- ja sikiökuolleisuuteen. Näiden annosten on joissakin tutkimuksissa raportoitu aiheuttavan luuston poikkeavuuksia. Perinataalisissa/postnataalisissa tutkimuksissa kuolleena syntyneiden ilmaantuvuus lisääntyi annoksilla, jotka olivat 20 kertaa suurempia kuin ihmisannos.
Ei ole olemassa hyvin kontrolloituja tutkimuksia raskaana olevilla naisilla; siksi käytä diltiatseemia raskaana oleville naisille vain, jos mahdollinen hyöty oikeuttaa mahdollisen riskin sikiölle.
Imettävät äidit
Diltiatsemi erittyy äidinmaitoon. Eräässä raportissa ehdotetaan, että pitoisuudet rintamaidossa voivat olla likimääräisiä seerumipitoisuuksia. Jos diltiatseemin käyttö katsotaan välttämättömäksi, on otettava käyttöön vaihtoehtoinen pikkulasten ruokintamenetelmä.
Käyttö lapsille
Turvallisuutta ja tehokkuutta lapsipotilailla ei ole osoitettu.
Geriatrinen käyttö
Kliinisissä diltiatseemitutkimuksissa ei ollut riittävästi 65-vuotiaita ja sitä vanhempia koehenkilöitä sen määrittämiseksi, reagoivatko he eri tavalla kuin nuoremmat. Muut raportoidut kliiniset kokemukset eivät ole osoittaneet eroja iäkkäiden ja nuorempien potilaiden vasteissa. Yleensä iäkkään potilaan annoksen valinnassa tulee olla varovainen, yleensä alkaen annosalueen alimmasta päästä, mikä heijastaa maksan, munuaisten tai sydämen toiminnan heikkenemisen sekä samanaikaisen sairauden tai muun lääkehoidon yleisyyttä.
YLIANNOSTUS
Suun kautta otettavat LD50-arvot hiirillä ja rotilla vaihtelevat 415 - 740 mg/kg ja 560 - 810 mg/kg, vastaavasti. Laskimonsisäiset LD50-arvot näissä lajeissa olivat 60 ja 38 mg/kg, vastaavasti. Oraalisen LD50:n koirilla katsotaan olevan yli 50 mg/kg, kun taas apinoilla havaittiin kuolleisuutta annoksella 360 mg/kg.
Myrkyllistä annosta ihmiselle ei tunneta. Laajan aineenvaihdunnan vuoksi veren pitoisuudet diltiatseemin vakioannoksen jälkeen voivat vaihdella yli kymmenkertaisesti, mikä rajoittaa veripitoisuuksien käyttökelpoisuutta yliannostustapauksissa.
Diltiatseemin yliannostusta on raportoitu määrinä, jotka vaihtelevat välillä
Diltiatseemin yliannostuksen jälkeen havaittuja tapahtumia olivat bradykardia, hypotensio, sydänkatkos ja sydämen vajaatoiminta. Useimmissa yliannostusraporteissa kuvattiin jotain tukitoimenpiteitä ja/tai lääkehoitoa. Bradykardia reagoi usein suotuisasti atropiiniin, samoin kuin sydänkatkos, vaikka sydämentahdistusta käytettiin usein myös sydäntukoksen hoitoon. Verenpaineen ylläpitämiseen käytettiin nesteitä ja vasopressoreita, ja sydämen vajaatoiminnan tapauksissa annettiin inotrooppisia aineita. Lisäksi jotkut potilaat saivat hoitoa hengitystuella, mahahuuhtelulla, aktiivihiilellä ja/tai suonensisäisellä kalsiumilla.
Kalsiumin suonensisäisen annon tehokkuus diltiatseemin yliannostuksen farmakologisten vaikutusten kumoamisessa on ollut epäjohdonmukainen. Muutamissa raportoiduissa tapauksissa kalsiumkanavasalpaajien yliannostus, johon liittyi hypotensiota ja bradykardiaa, joka oli alun perin resistentti atropiinille, reagoi paremmin atropiiniin sen jälkeen, kun potilaat saivat suonensisäistä kalsiumia. Joissakin tapauksissa suonensisäistä kalsiumia (1 g kalsiumkloridia tai 3 g kalsiumglukonaattia) on annettu 5 minuutin aikana ja toistettu 10–20 minuutin välein tarpeen mukaan. Kalsiumglukonaattia on myös annettu jatkuvana infuusiona nopeudella 2 g tunnissa 10 tunnin ajan. Kalsiumin infuusiota 24 tuntia tai pidempään voidaan tarvita. Potilaita tulee seurata hyperkalsemian merkkien varalta.
Yliannostuksen tai liiallisen vasteen sattuessa on käytettävä asianmukaisia tukitoimenpiteitä ruoansulatuskanavan dekontaminaation lisäksi. Diltiatsemi ei näytä poistuvan peritoneaalisella tai hemodialyysillä. Rajalliset tiedot viittaavat siihen, että plasmafereesi tai hiilen hemoperfuusio voivat nopeuttaa diltiatseemin eliminaatiota yliannostuksen jälkeen. Diltiatseemin tunnettujen farmakologisten vaikutusten ja/tai raportoitujen kliinisten kokemusten perusteella voidaan harkita seuraavia toimenpiteitä:
Bradykardia: Anna atropiinia (0,6-1 mg). Jos emättimen salpaus ei anna vastetta, anna isoproterenolia varoen.
Korkean asteen AV-esto: Käsittele kuten yllä olevaa bradykardiaa. Kiinteä korkea-asteinen AV-katkos tulee hoitaa sydämentahdistuksella.
Sydämen vajaatoiminta: Anna inotrooppisia aineita (isoproterenolia, dopamiinia tai dobutamiinia) ja diureetteja.
Hypotensio: Vasopressorit (esim. dopamiini tai norepinefriini).
Todellisen hoidon ja annoksen tulee riippua kliinisen tilanteen vakavuudesta sekä hoitavan lääkärin harkinnasta ja kokemuksesta.
VASTA-AIHEET
Diltiatsemi on vasta-aiheinen (1) potilailla, joilla on sairas sinus-oireyhtymä paitsi jos käytössä on toimiva kammiotahdistin, (2) potilailla, joilla on toisen tai kolmannen asteen AV-salpaus paitsi jos läsnä on toimiva kammiotahdistin, (3) potilailla, joilla on toimiva kammiotahdistin. hypotensio (alle 90 mmHg systolinen), (4) potilaat, jotka ovat osoittaneet yliherkkyyttä lääkkeelle, ja (5) potilaat, joilla on akuutti sydäninfarkti ja keuhkokongestio, jotka on dokumentoitu röntgenkuvauksella vastaanoton yhteydessä.
KLIININEN FARMAKOLOGIA
Diltiatsemihydrokloridi-pitkävaikutteisten kapseleiden USP (kerran päivässä annostelu) terapeuttisten vaikutusten uskotaan liittyvän sen kykyyn estää kalsiumionien sisäänvirtaus soluihin sydämen ja verisuonten sileän lihaksen kalvodepolarisaation aikana.
Toimintamekanismit
Hypertensio
Diltiatsemihydrokloridin pitkittyvästi vapauttavat kapselit USP (kerran päivässä annostelu) tuottaa verenpainetta alentavan vaikutuksensa ensisijaisesti rentouttamalla verisuonten sileää lihasta ja siitä johtuvaa perifeerisen verisuonten vastuksen vähenemistä. Verenpaineen laskun suuruus liittyy kohonneen verenpaineen asteeseen; näin ollen verenpainepotilailla on verenpainetta alentava vaikutus, kun taas normaalipainepotilailla verenpaine laskee vain vähän.
Angina pectoris
Diltiatsemihydrokloridi pitkittyvästi vapauttavien kapseleiden USP (kerran päivässä annostelu) on osoitettu lisäävän harjoituksen sietokykyä, mikä johtuu luultavasti sen kyvystä vähentää sydänlihaksen hapen tarvetta. Tämä saavutetaan alentamalla sykettä ja systeemistä verenpainetta submaksimaalisella ja maksimaalisella työkuormalla. Diltiaseemin on osoitettu olevan tehokas sepelvaltimoiden, sekä epikardiaalisen että subendokardiaalisen, laajentaja. Diltiatseemi estää spontaanin ja ergonoviinin aiheuttaman sepelvaltimon kouristuksen.
Eläinmalleissa diltiatseemi häiritsee hidasta sisäänpäin suuntautuvaa (depolarisoivaa) virtaa kiihtyvässä kudoksessa. Se aiheuttaa viritys-supistus irtoamisen eri sydänkudoksissa ilman muutoksia toimintapotentiaalin konfiguraatiossa. Diltiatsemi saa aikaan sepelvaltimoiden sileän lihaksen rentoutumisen ja sekä suurten että pienten sepelvaltimoiden laajentamisen lääketasoilla, jotka aiheuttavat vain vähän tai ei ollenkaan negatiivista inotrooppista vaikutusta. Seurauksena oleva sepelvaltimon verenvirtauksen (epikardiaalinen ja subendokardiaalinen) lisääntyminen tapahtuu iskeemisissä ja ei-iskeemisissä malleissa, ja niihin liittyy annosriippuvainen systeemisen verenpaineen lasku ja perifeerisen vastuksen lasku.
Hemodynaamiset ja sähköfysiologiset vaikutukset
Kuten muutkin kalsiumkanavaantagonistit, diltiatseemi vähentää sinoatriaalista ja atrioventrikulaarista johtumista eristetyissä kudoksissa ja sillä on negatiivinen inotrooppinen vaikutus eristettyissä valmisteissa. Terveellä eläimellä AH-välin pidentymistä voidaan havaita suuremmilla annoksilla.
Ihmisellä diltiatseemi ehkäisee spontaaneja ja ergonoviinin aiheuttamia sepelvaltimon kouristuksia. Se aiheuttaa perifeerisen verisuonten vastuksen laskua ja lievää verenpaineen laskua normotensiivisillä henkilöillä ja alentaa iskeemistä sydänsairautta sairastavien potilaiden rasitustoleranssitutkimuksissa syke-verenpainetuotetta missä tahansa työkuormissa. Tähän mennessä tehdyt tutkimukset, pääasiassa potilailla, joilla on hyvä kammiotoiminta, eivät ole paljastaneet todisteita negatiivisesta inotrooppisesta vaikutuksesta; sydämen minuuttitilavuus, ejektiofraktio ja vasemman kammion loppudiastolinen paine eivät ole muuttuneet. Tällaisilla tiedoilla ei ole ennustavaa arvoa vaikutuksille potilailla, joilla on huono kammiotoiminta, ja sydämen vajaatoiminnan lisääntymistä on raportoitu potilailla, joilla on jo ennestään kammioiden toimintahäiriö. Toistaiseksi on vähän tietoa diltiatseemin ja beetasalpaajien yhteisvaikutuksista potilailla, joilla on huono kammiotoiminta. Diltiatseemi alentaa yleensä hieman leposykettä.
Hypertensiivisillä potilailla diltiatseemihydrokloridin pitkitetysti vapauttavat kapselit USP (kerran päivässä annostelu) tuottaa verenpainetta alentavaa vaikutusta sekä makuu- että seisoma-asennossa. Kaksoissokkoutetussa, rinnakkaistutkimuksessa, jossa käytettiin annoksia 90–540 mg kerran vuorokaudessa, diltiatseemihydrokloridin pitkitetysti vapauttava kapseli (kerran vuorokaudessa annostelu) alensi selässä olevan diastolisen verenpainetta näennäisesti lineaarisesti koko ajan. tutkittu annosalue. Diastolisen verenpaineen muutokset mitattuna alimmillaan lumelääkettä saaneilla annoksilla 90 mg, 180 mg, 360 mg ja 540 mg olivat -2,9, -4,5, -6,1, -9,5 ja -10,5 mmHg. Posturaalinen hypotensio havaitaan harvoin äkillisen pystyasennon ottaessa. Kroonisiin verenpainetta alentaviin vaikutuksiin ei liity refleksitakykardiaa. Diltiatsemihydrokloridin pitkittyvästi vapauttavat kapselit USP (kerran päivässä annostelu) vähentää verisuonten vastusta, lisää sydämen minuuttitilavuutta (lisäämällä aivohalvauksen tilavuutta); ja aiheuttaa lievän laskun tai ei muuta sykettä. Dynaamisen harjoituksen aikana diastolisen paineen nousu estyy, kun taas maksimi saavutettava systolinen paine yleensä laskee. Krooninen hoito diltiatseemihydrokloridin pitkittyvästi vapauttavilla kapseleilla USP (kerran päivässä annostelu) ei aiheuta muutoksia tai lisää plasman katekoliamiinien määrää. Reniini-angiotensiini-aldosteroni-akselin aktiivisuuden lisääntymistä ei ole havaittu. Diltiatsemihydrokloridin pitkittyvästi vapauttavat kapselit USP (kerran päivässä annostus) vähentävät angiotensiini II:n munuais- ja perifeerisiä vaikutuksia. Hypertensiiviset eläinmallit reagoivat diltiatseemiin verenpaineen laskulla ja lisääntyneellä virtsan erittymisellä ja natriureesilla muuttamatta virtsan natrium/kalium-suhdetta.
Kaksoissokkoutetussa, rinnakkaisessa annos-vastetutkimuksessa, jossa käytettiin annoksia 60 mg - 480 mg kerran vuorokaudessa, diltiatseemihydrokloridin pitkitetysti vapauttava kapseli (kerran vuorokaudessa annettava annos) pidensi harjoituksen lopettamiseen kuluvaa aikaa lineaarisesti koko annoksen aikana. tutkittu alue. Bruce-harjoitusprotokollaa käyttävän harjoituksen päättymiseen kuluva aika parantui 60 mg:n, 120 mg:n, 240 mg:n, 360 mg:n ja 480 mg:n plasebon alimmalla tasolla mitattuna 29, 40, 56, 51, 69 ja 68 sekuntia. , vastaavasti. Kun diltiatseemihydrokloridin pitkitetysti vapauttavan kapselin annoksia (kerran vuorokaudessa annettava annos) suurennettiin, rasitusrintakipujen yleinen esiintymistiheys väheni. Diltiatsemihydrokloridi-depotkapselia (kerran vuorokaudessa), 180 mg kerran vuorokaudessa tai lumelääkettä annettiin kaksoissokkotutkimuksessa potilaille, jotka saivat samanaikaista hoitoa pitkävaikutteisilla nitraateilla ja/tai beetasalpaajilla. Harjoituksen lopettamiseen kuluva aika pidentyi merkittävästi ja angina pectoris -tiheys väheni merkittävästi. Tässä tutkimuksessa haittatapahtumien yleinen esiintymistiheys diltiatseemihydrokloridin pitkitetysti vapauttavalla kapselilla (annos kerran päivässä) oli sama kuin lumeryhmässä.
Laskimonsisäinen diltiatseemi 20 mg:n annoksina pidentää AH:n johtumisaikaa ja AV-solmukkeen toiminnallisia ja tehokkaita refraktaarisia jaksoja noin 20 %. Tutkimuksessa, jossa annettiin 300 mg:n diltiatseemihydrokloridin kerta-annoksia suun kautta kuudella normaalilla vapaaehtoisella, keskimääräinen maksimaalinen PR-ajan piteneminen oli 14 % ilman ensimmäisen asteen AV-salpausta suurempia tapauksia. Diltiatseemiin liittyvä AH-ajan pidentyminen ei ole selvempää potilailla, joilla on ensimmäisen asteen sydänkatkos. Potilailla, joilla on sairas poskiontelooireyhtymä, diltiatseemi pidentää merkittävästi poskiontelosyklin pituutta (jopa 50 % joissakin tapauksissa).
Diltiatsemihydrokloridin jatkuva oraalinen antaminen potilaille jopa 540 mg/vrk annoksina on johtanut PR-välin vähäiseen pidentymiseen ja toisinaan aiheuttanut epänormaalia pitenemistä (ks. VAROITUKSET ).
Farmakokinetiikka ja aineenvaihdunta
Diltiatsemi imeytyy hyvin maha-suolikanavasta ja sillä on laaja ensikierron vaikutus, jolloin absoluuttinen hyötyosuus (verrattuna suonensisäiseen antoon) on noin 40 %. Diltiatsemi metaboloituu laajasti, jolloin vain 2–4 % muuttumattomasta lääkkeestä erittyy virtsaan. Lääkkeet, jotka indusoivat tai estävät maksan mikrosomaalisia entsyymejä, voivat muuttaa diltiatseemin jakautumista.
Kokonaisradioaktiivisuuden mittaus lyhyen laskimonsisäisen annon jälkeen terveillä vapaaehtoisilla viittaa siihen, että läsnä on muita tunnistamattomia metaboliitteja, jotka saavuttavat suuremmat pitoisuudet kuin diltiatseemi ja jotka eliminoituvat hitaammin; kokonaisradioaktiivisuuden puoliintumisaika on noin 20 tuntia verrattuna diltiatseemin 2-5 tuntiin.
In vitro -sitoutumistutkimukset osoittavat, että diltiatseemi sitoutuu 70–80 % plasman proteiineihin. Kilpailevat in vitro ligandisitoutumistutkimukset ovat myös osoittaneet, että digoksiinin, hydroklooritiatsidin, fenyylibutatsonin, propranololin, salisyylihapon tai varfariinin terapeuttiset pitoisuudet eivät muuta diltiatseemin sitoutumista. Plasman eliminaation puoliintumisaika yhden tai useamman lääkkeen annon jälkeen on noin 3,0-4,5 tuntia. Desasetyylidiltiatseemia on myös plasmassa 10-20 % alkuperäisestä lääkkeestä ja se on 25-50 % yhtä tehokas sepelvaltimon vasodilataattorina kuin diltiatseemi. Terapeuttiset plasman diltiatseemipitoisuudet näyttävät olevan 50-200 ng/ml. Lineaarisuudesta poikkeaa, kun annosvahvuuksia lisätään; puoliintumisaika pitenee hieman annoksen myötä. Tutkimuksessa, jossa verrattiin potilaita, joilla oli normaali maksan toiminta, maksakirroosipotilaisiin, havaittiin puoliintumisajan pidentyminen ja 69 %:n lisääntyminen biologisessa hyötyosuudessa maksan vajaatoimintapotilailla. Yhdessä tutkimuksessa yhdeksällä potilaalla, joilla oli vakava munuaisten vajaatoiminta, ei havaittu eroa diltiatseemin farmakokineettisessä profiilissa verrattuna potilaisiin, joilla oli normaali munuaisten toiminta.
Diltiazem Hydrochloride pitkävaikutteiset kapselit (kerran vuorokaudessa)
Verrattuna vakaan tilan diltiatseemitablettien hoitoon yli 95 % lääkkeestä imeytyy diltiatseemihydrokloridin pitkitetysti vapauttavista kapseleista (kerran vuorokaudessa annettava annos). Yksittäinen 360 mg:n annos kapselia johtaa havaittaviin plasmapitoisuuksiin 2 tunnin sisällä ja huippupitoisuuksiin plasmassa 10-14 tunnin kuluttua; imeytyminen tapahtuu koko annosteluvälin ajan. Kun diltiatseemihydrokloridin pitkitetysti vapauttava kapseli (kerran vuorokaudessa) annettiin samanaikaisesti runsasrasvaisen aamiaisen kanssa, diltiatseemin imeytymisen laajuus ei vaikuttanut. Annosta ei tapahdu. Näennäinen eliminaation puoliintumisaika kerta- tai toistuvan annoksen jälkeen on 5-8 tuntia. Poikkeama lineaarisuudesta on samanlainen kuin diltiatseemitableteilla ja diltiatseemihydrokloridikapseleilla (kahdesti päivässä). Kun diltiatseemihydrokloridin pitkitetysti vapauttavien kapseleiden annosta (kerran vuorokaudessa annettava annos) nostetaan 120 mg:n vuorokausiannoksesta 240 mg:aan, käyrän alla oleva pinta-ala kasvaa 2,7-kertaiseksi. Kun annosta nostetaan 240 mg:sta 360 mg:aan, käyrän alla oleva pinta-ala kasvaa 1,6-kertaiseksi.
POTILASTIEDOT
Tietoja ei ole annettu. Katso VAROITUKSET ja VAROTOIMENPITEET osiot.
