Imodium 2mg Loperamide Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Imodium 2mg on ja miten sitä käytetään?
Imodium 2mg on reseptilääke, jota käytetään akuutin ripulin, kroonisen ripulin ja matkustajaripulin oireiden hoitoon. Imodiumia voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Imodium kuuluu lääkeryhmään nimeltä Antidiarreals.
Mitkä ovat Imodiumin mahdolliset sivuvaikutukset?
Imodium voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- vetistä tai veristä ripulia,
- vatsakipu tai turvotus,
- jatkuva tai paheneva ripuli,
- nopeat tai jyskyttävät sydämenlyönnit,
- lepattaa rinnassasi,
- hengenahdistus ja
- huimaus
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Imodiumin yleisimpiä sivuvaikutuksia ovat:
- ummetus,
- huimaus,
- uneliaisuus,
- pahoinvointi ja
- vatsakramppeja
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Imodiumin mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
IMODIUM® (loperamidihydrokloridi), 4-(p-kloorifenyyli)-4-hydroksi-N,N-dimetyyli-a, a-difenyyli-1-piperidiinibutyyriamidimonohydrokloridi, on synteettinen ripulilääke suun kautta käytettäväksi.
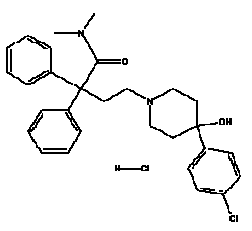
IMODIUM® (loperamidi hcl) on saatavana 2 mg:n kapseleina.
Inaktiiviset aineet ovat: Laktoosi, maissitärkkelys, talkki ja magnesiumstearaatti. IMODIUM® (loperamidi hcl) kapselit sisältävät FD&C Yellow No. 6:n.
INDIKAATIOT
IMODIUM® (loperamidihydrokloridi) on tarkoitettu akuutin epäspesifisen ripulin ja tulehdukselliseen suolistosairauteen liittyvän kroonisen ripulin hallintaan ja oireiden lievitykseen. IMODIUM® (loperamidi hcl) on tarkoitettu myös ileostomien vuotojen vähentämiseen.
ANNOSTELU JA HALLINNOINTI
(1 kapseli = 2 mg)
Potilaiden tulee saada asianmukainen neste- ja elektrolyyttikorvaus tarpeen mukaan.
Akuutti ripuli
Aikuiset: Suositeltu aloitusannos on 4 mg (kaksi kapselia), jonka jälkeen 2 mg (yksi kapseli) jokaisen muodostumattoman ulosteen jälkeen. Päivittäinen annos ei saa ylittää 16 mg (kahdeksan kapselia). Kliininen paraneminen havaitaan yleensä 48 tunnin kuluessa.
Lapset: 2–5-vuotiailla lapsilla (20 kg tai vähemmän) tulee käyttää reseptivapaata nestemäistä formulaatiota (IMODIUM® (loperamidi hcl) AD 1 mg/5 ml); 6–12-vuotiaille voidaan käyttää joko IMODIUM® (loperamidi hcl) kapseleita tai IMODIUM® (loperamidi hcl) AD-nestettä. 2–12-vuotiaille lapsille seuraava kapseleiden tai nesteiden aikataulu täyttää yleensä aloitusannosvaatimukset:
Suositeltu ensimmäisen päivän annostusaikataulu
kahdesta viiteen vuotta: 1 mg tid (3 mg vuorokausiannos) (13 - 20 kg) Kuudesta kahdeksaan vuotta: 2 mg kahdesti (4 mg vuorokausiannos) (20 - 30 kg) 8 - 12 vuotta: 2 mg tid (6 mg vuorokausiannos) (yli 30 kg) )
Suositeltu myöhempi päivittäinen annos
Ensimmäisen hoitopäivän jälkeen on suositeltavaa antaa seuraavat IMODIUM®-annokset (loperamidi hcl) (1 mg/10 kg ruumiinpainoa) vasta löysän ulosteen jälkeen. Päivittäinen kokonaisannos ei saa ylittää ensimmäisenä päivänä suositeltuja annoksia.
Krooninen ripuli
Lapset: Vaikka IMODIUM® (loperamidi hcl) on tutkittu rajoitetulla määrällä lapsia, joilla on krooninen ripuli; terapeuttista annosta kroonisen ripulin hoitoon lapsipotilailla ei ole vahvistettu.
Aikuiset: Suositeltu aloitusannos on 4 mg (kaksi kapselia), jota seuraa 2 mg (yksi kapseli) jokaisen muodostumattoman ulosteen jälkeen, kunnes ripuli on hallinnassa, minkä jälkeen IMODIUM®:n (loperamidi hcl) annosta tulee pienentää yksilöllisten tarpeiden mukaan. Kun optimaalinen päiväannos on määritetty, tämä määrä voidaan sitten antaa yhtenä annoksena tai jaettuina annoksina.
Keskimääräinen päivittäinen ylläpitoannos kliinisissä tutkimuksissa oli 4-8 mg (kahdesta neljään kapselia). 16 mg:n (kahdeksan kapselin) annos ylittyi harvoin. Jos kliinistä paranemista ei havaita 16 mg:n vuorokausihoidon jälkeen vähintään 10 päivän ajan, oireita ei todennäköisesti saada hallintaan lisäannolla. IMODIUM® (loperamidi hcl) antoa voidaan jatkaa, jos ripulia ei voida riittävästi hallita ruokavaliolla tai erityisellä hoidolla.
Lapset alle 2 vuotta
IMODIUMin (loperamidi hcl) käyttöä alle 2-vuotiaille lapsille ei suositella. Harvoin on raportoitu paralyyttistä ileuksesta, johon liittyy vatsan turvotusta. Suurin osa näistä raporteista esiintyi akuutin punataudin, yliannostuksen ja hyvin pienten alle kahden vuoden ikäisten lasten yhteydessä.
Vanhukset
Varsinaisia farmakokineettisiä tutkimuksia ei ole tehty iäkkäillä henkilöillä. Kuitenkaan iäkkäiden ripulipotilaiden lääkkeen jakautumisessa ei raportoitu merkittäviä eroja nuoriin potilaisiin verrattuna. Vanhuksille annosta ei tarvitse muuttaa.
Munuaisten vajaatoiminta
Munuaisten vajaatoimintaa sairastavien potilaiden farmakokineettisiä tietoja ei ole saatavilla. Koska metaboliitit ja muuttumaton lääke erittyvät pääasiassa ulosteeseen, annostusta ei tarvitse muuttaa potilailla, joilla on munuaisten vajaatoiminta (ks. VAROTOIMET -osiossa ).
Maksan vajaatoiminta
Vaikka farmakokineettisiä tietoja ei ole saatavilla potilaista, joilla on maksan vajaatoiminta, IMODIUM-valmistetta (loperamidi hcl) tulee käyttää varoen tällaisilla potilailla, koska ensikierron metabolia on hidastunut. (katso VAROTOIMENPITEET ).
MITEN TOIMITETAAN
Kapselit - jokainen kapseli sisältää 2 mg loperamidihydrokloridia. Kapseleissa on vaaleanvihreä runko-osa ja tummanvihreä kansi, jonka toiseen osaan on painettu "JANSSEN" ja toiseen osaan "IMODIUM". IMODIUM® (loperamidi hcl) kapselit toimitetaan 100 pulloissa.
NDC 50458-400-10.........(100 KAPSELIA)
Säilytä 15°-25°C (59°-77°F).
Janssen Pharmaceutica Inc. Tarkistettu syyskuussa 1996, heinäkuussa 1998. FDA Rev date: 21.10.2005
SIVUVAIKUTUKSET
Kliinisen tutkimuksen tiedot
IMODIUM®:n (loperamidihydrokloridin) kliinisissä tutkimuksissa raportoituja haittavaikutuksia on vaikea erottaa ripulioireyhtymään liittyvistä oireista. Kliinisissä IMODIUM®-tutkimuksissa (loperamidi hcl) kirjatut haittakokemukset olivat yleensä vähäisiä ja itsestään rajoittuvia. Niitä havaittiin yleisemmin kroonisen ripulin hoidon aikana.
Raportoidut haittatapahtumat on koottu yhteenveto riippumatta tutkijoiden syy-yhteyden arvioinnista.
1) Haittatapahtumat neljästä lumekontrolloidusta tutkimuksesta potilailla, joilla on akuutti ripuli Haittatapahtumat, joiden ilmaantuvuus oli 1,0 % tai enemmän ja joita raportoitiin vähintään yhtä usein loperamidihydrokloridia saaneilla potilailla kuin lumelääkettä saaneilla, on esitetty alla olevassa taulukossa.
Haittatapahtumat, joiden ilmaantuvuus oli 1,0 % tai suurempi ja joita raportoitiin useammin lumelääkettä saaneilla potilailla kuin loperamidihydrokloridia saaneilla potilailla, olivat suun kuivuminen, ilmavaivat, vatsakrampit ja koliikki.
2) Haittatapahtumat 20 lumekontrolloidusta tutkimuksesta potilailla, joilla on krooninen ripuli
Haittatapahtumat, joiden ilmaantuvuus oli 1,0 % tai enemmän ja joita raportoitiin vähintään yhtä usein loperamidihydrokloridia saaneilla potilailla kuin lumelääkettä saaneilla potilailla, on esitetty alla olevassa taulukossa.
Haittatapahtumat, joiden ilmaantuvuus oli vähintään 1,0 % ja joita raportoitiin useammin lumelääkettä saaneilla potilailla kuin loperamidihydrokloridia saaneilla potilailla, olivat pahoinvointi, oksentelu, päänsärky, meteorismi, vatsakipu, vatsakrampit ja koliikki.
3) Haittatapahtumat 76 kontrolloidusta ja kontrolloimattomasta tutkimuksesta potilailla, joilla on akuutti tai krooninen ripuli
Haittatapahtumat, joiden ilmaantuvuus on 1,0 % tai enemmän potilailla kaikista tutkimuksista, on esitetty alla olevassa taulukossa.
Markkinoinnin jälkeistä kokemusta
Seuraavia haittatapahtumia on raportoitu:
Ihon ja ihonalaisen kudoksen häiriöt
Ihottumaa, kutinaa, urtikariaa, angioedeemaa ja erittäin harvinaisia rakkuloita, mukaan lukien erythema multiforme, Stevens-Johnsonin oireyhtymä ja toksinen epidermaalinen nekrolyysi, on raportoitu käytettäessä IMODIUM-valmistetta (loperamidi hcl).
Immuunijärjestelmän häiriöt
Yksittäisiä allergisia reaktioita ja joissakin tapauksissa vakavia yliherkkyysreaktioita, mukaan lukien anafylaktinen sokki ja anafylaktoidisia reaktioita, on raportoitu IMODIUMin (loperamidi hcl) käytön yhteydessä.

Ruoansulatuskanavan häiriöt
Suun kuivuminen, vatsakipu, turvotus tai epämiellyttävä tunne, pahoinvointi, oksentelu, ilmavaivat, dyspepsia, ummetus, paralyyttinen ileus, megakoolon, mukaan lukien toksinen megakoolon (ks. VASTA-AIHEET ja VAROITUKSET ).
Munuaisten ja virtsateiden häiriöt
Virtsanpidätys
Hermoston häiriöt
Uneliaisuus, huimaus
Yleiset häiriöt ja hallinnolliset olosuhteet
Väsymys
Useat kliinisissä tutkimuksissa ja loperamidin markkinoille tulon jälkeisessä kokemuksessa raportoidut haittatapahtumat ovat taustalla olevan ripulioireyhtymän (vatsakipu/vatsakipu, pahoinvointi, oksentelu, suun kuivuminen, väsymys, uneliaisuus, huimaus, ummetus ja ilmavaivat) yleisiä oireita. . Näitä oireita on usein vaikea erottaa ei-toivotuista lääkevaikutuksista.
Huumeiden väärinkäyttö ja riippuvuus
Väärinkäyttö
Erityinen kliininen tutkimus, jonka tarkoituksena oli arvioida loperamidin väärinkäyttöpotentiaalia suurilla annoksilla, johti havaintoon erittäin alhaisesta väärinkäytöstä.
Riippuvuus
Morfiinista riippuvaisilla apinoilla tehdyt tutkimukset osoittivat, että loperamidihydrokloridi ihmisille suositeltuja annoksia suuremmilla annoksilla esti morfiinin vieroitusoireita. Kuitenkin ihmisillä naloksonialtistuspupillitesti, joka positiivisena osoittaa opiaattien kaltaisia vaikutuksia, suoritettu yhden suuren annoksen jälkeen tai yli kahden vuoden IMODIUM®:n (loperamidihydrokloridin) terapeuttisen käytön jälkeen, oli negatiivinen. Suun kautta annettu IMODIUM® (loperamidi hcl) (magnesiumstearaatin kanssa formuloitu loperamidi) on sekä erittäin liukenematonta että tunkeutuu keskushermostoon huonosti.
HUUMEIDEN VUOROVAIKUTUKSET
Ei-kliiniset tiedot ovat osoittaneet, että loperamidi on P-glykoproteiinin substraatti. Loperamidin (16 mg kerta-annos) samanaikainen anto 600 mg:n kerta-annoksen joko kinidiiniä tai ritonaviiria, jotka molemmat ovat P-glykoproteiinin estäjiä, johti 2-3-kertaiseen plasman loperamidipitoisuuden nousuun. Koska loperamidin ja kinidiinin ja ritonaviirin samanaikainen käyttö voi voimistaa sentraalisia vaikutuksia, varovaisuutta on noudatettava annettaessa loperamidia suositelluilla annoksilla (2 mg, enintään 16 mg vuorokaudessa) P-glykoproteiinin estäjien kanssa.
Kun kerta-annos 16 mg loperamidia annetaan samanaikaisesti 600 mg:n sakinaviirin kerta-annoksen kanssa, loperamidi vähensi sakinaviirialtistusta 54 %, mikä saattaa olla kliinistä merkitystä sakinaviirin terapeuttisen tehon heikkenemisen vuoksi. Sakinaviirin vaikutus loperamidiin on vähemmän kliininen. Siksi sakinaviirin terapeuttista tehoa on seurattava tarkasti, kun loperamidia annetaan sakinaviirin kanssa.
VAROITUKSET
Neste- ja elektrolyyttivaje esiintyy usein potilailla, joilla on ripuli. Tällaisissa tapauksissa sopivan nesteen ja elektrolyyttien antaminen on erittäin tärkeää. IMODIUM®:n (loperamidi hcl) käyttö ei sulje pois sopivan neste- ja elektrolyyttihoidon tarvetta.
Yleisesti ottaen IMODIUM-valmistetta (loperamidi hcl) ei tule käyttää, kun peristaltiikan estoa halutaan välttää, koska se voi aiheuttaa merkittäviä jälkitauteja, mukaan lukien ileus, megakoolon ja toksinen megakooloni. IMODIUM (loperamidi hcl) on lopetettava välittömästi, kun ummetus, vatsan turvotus tai ileus kehittyy.
Ripulin hoito IMODIUMilla (loperamidi hcl) on vain oireenmukaista. Aina kun taustalla oleva etiologia voidaan määrittää, erityistä hoitoa tulee antaa tarvittaessa (tai tarvittaessa).
AIDS-potilaiden, joita hoidetaan IMODIUM-valmisteella (loperamidi hcl) ripuliin, hoito tulee lopettaa heti, kun vatsan turvotuksen merkkejä ilmenee. On yksittäisiä raportteja myrkyllisistä megakoolonista AIDS-potilailla, joilla on sekä virus- että bakteeripatogeenien aiheuttama tarttuva paksusuolentulehdus, jota on hoidettu loperamidihydrokloridilla. {ref EDMS-PSDB-2564186, s. 12}
IMODIUM®:ia (loperamidi hcl) tulee käyttää erityisen varoen pienille lapsille, koska vasteen vaihtelu tässä ikäryhmässä on suurempi. Kuivuminen, erityisesti nuoremmilla lapsilla, voi edelleen vaikuttaa IMODIUM®-vasteen vaihteluun (loperamidi hcl).
VAROTOIMENPITEET
Kenraali
Erittäin harvinaisia allergisia reaktioita, mukaan lukien anafylaksia ja anafylaktinen sokki, on raportoitu. Akuutissa ripulissa, jos kliinistä paranemista ei havaita 48 tunnin kuluessa, IMODIUM®:n (loperamidihydrokloridi) anto tulee lopettaa ja potilaita tulee neuvoa ottamaan yhteyttä lääkäriin. Vaikka farmakokineettisiä tietoja ei ole saatavilla potilaista, joilla on maksan vajaatoiminta, IMODIUM-valmistetta (loperamidi hcl) tulee käyttää varoen tällaisilla potilailla, koska ensikierron metabolia on hidastunut. Potilaita, joilla on maksan vajaatoiminta, tulee seurata tarkasti keskushermostotoksisuuden merkkien varalta. Munuaisten vajaatoimintaa sairastavien potilaiden farmakokineettisiä tietoja ei ole saatavilla. Koska on raportoitu, että suurin osa lääkkeestä metaboloituu ja metaboliitit tai muuttumaton lääke erittyy pääasiassa ulosteeseen, munuaisten vajaatoimintaa sairastavien potilaiden annostusta ei tarvitse muuttaa. Varsinaisia tutkimuksia ei ole tehty loperamidin farmakokinetiikan arvioimiseksi iäkkäillä henkilöillä. Kahdessa tutkimuksessa, joihin otettiin iäkkäitä potilaita, ei kuitenkaan havaittu merkittäviä eroja lääkkeen jakautumisessa iäkkäillä ripulipotilailla verrattuna nuoriin potilaisiin.
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
18 kuukautta kestäneessä rotalla tehdyssä tutkimuksessa suun kautta annetuilla annoksilla enintään 40 mg/kg/vrk (21 kertaa ihmisen enimmäisannos 16 mg/vrk, kehon pinta-alan vertailun perusteella), ei havaittu todisteita karsinogeneesistä.
Loperamidi ei ollut genotoksinen Ames-testissä, SOS-kromotestissä E. colissa, hallitsevassa tappavassa testissä naarashiirillä eikä hiiren alkiosolutransformaatiomäärityksessä.
Hedelmällisyyttä ja lisääntymiskykyä arvioitiin rotilla käyttämällä oraalisia annoksia 2,5, 10 ja 40 mg/kg/vrk yhdessä tutkimuksessa ja 1, 5, 10, 20 ja 40 mg/kg/vrk (vain naaraat) toisessa tutkimuksessa. opiskella. Suun kautta antaminen 20 mg/kg/vrk (noin 11 kertaa ihmisen annos kehon pinta-alan vertailun perusteella) ja suurempi annos aiheutti voimakasta heikentämistä naisen hedelmällisyyteen. Naarasrottien hoidolla enintään 10 mg/kg/vrk suun kautta (noin 5 kertaa ihmisen annos kehon pinta-alan vertailun perusteella) ei ollut vaikutusta hedelmällisyyteen. Urosrottien hoito annoksella 40 mg/kg/vrk po (noin 21 kertaa ihmisen annos kehon pinta-alan vertailun perusteella) aiheutti urospuolisten hedelmällisyyden heikkenemistä, kun taas 10 mg/kg/vrk (noin 5 kertaa ihmisen annokseen verrattuna) annoksella, joka perustuu kehon pinta-alan vertailuun) ei vaikuttanut.
Raskaus
Teratogeeniset vaikutukset, raskaus, kategoria C
Teratologisia tutkimuksia on suoritettu rotilla käyttämällä suun kautta annettavia annoksia 2,5, 10 ja 40 mg/kg/vrk ja kaniineilla oraalisilla annoksilla 5, 20 ja 40 mg/kg/vrk. Nämä tutkimukset eivät ole paljastaneet näyttöä heikentyneestä hedelmällisyydestä tai haitoista sikiölle annoksilla, jotka ovat enintään 10 mg/kg/vrk rotilla (5 kertaa ihmisen annos, joka perustuu kehon pinta-alan vertailuun) ja 40 mg/kg/vrk kaniineilla (43). kertaa ihmisen annos kehon pinta-alan vertailun perusteella). Rottien hoito annoksella 40 mg/kg/vrk po (21 kertaa ihmisen annos kehon pinta-alan vertailun perusteella) aiheutti huomattavaa hedelmällisyyden heikkenemistä. Tutkimukset eivät tuottaneet näyttöä teratogeenisesta aktiivisuudesta. Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia raskaana oleville naisille. Loperamidia tulee käyttää raskauden aikana vain, jos mahdollinen hyöty oikeuttaa sikiölle mahdollisesti aiheutuvan riskin.
Ei-teratogeeniset vaikutukset
Rotilla tehdyssä peri- ja postnataalisessa lisääntymistutkimuksessa 40 mg/kg/vrk suun kautta annettiin jälkeläisten kasvu- ja eloonjäämishäiriöitä.
Imettävät äidit
Pieniä määriä loperamidia voi erittyä äidinmaitoon. Siksi IMODIUM-valmistetta (loperamidi hcl) ei suositella imetyksen aikana.
Käyttö lapsille
Katso " VAROITUKSET " Osio, jossa on tietoa vastauksen suuremmasta vaihtelusta tässä ikäryhmässä.
Jos lapset saavat vahingossa yliannostuksen IMODIUM®-valmistetta, katso " YLIANNOSTUS "Osio ehdotetusta hoidosta.
YLIANNOSTUS
Yliannostustapauksissa (mukaan lukien maksan vajaatoiminnasta johtuva suhteellinen yliannostus) voi esiintyä virtsanpidätystä, paralyyttistä ileusta ja keskushermoston lamaa. Lapset voivat olla herkempiä keskushermostovaikutuksille kuin aikuiset. Kliiniset tutkimukset ovat osoittaneet, että heti loperamidihydrokloridin nauttimisen jälkeen annettu aktiivihiililiete voi vähentää systeemiseen verenkiertoon imeytyvän lääkkeen määrää jopa yhdeksänkertaisesti. Jos oksentelua esiintyy spontaanisti nieltäessä, 100 gramman aktiivihiililiete tulee antaa suun kautta heti, kun nestettä on kertynyt.
Jos oksentelua ei ole esiintynyt, mahahuuhtelu on suoritettava ja sen jälkeen annetaan 100 g aktiivihiililietettä mahaletkun kautta. Yliannostustapauksissa potilaita tulee seurata keskushermoston laman oireiden varalta vähintään 24 tunnin ajan.
Jos yliannostusoireita ilmaantuu, naloksonia voidaan antaa vastalääkkeenä. Jos naloksoni reagoi, elintoimintoja on seurattava huolellisesti lääkkeen yliannostuksen oireiden uusiutumisen varalta vähintään 24 tunnin ajan viimeisen naloksoniannoksen jälkeen.
Koska loperamidin vaikutus on pitkittynyt ja naloksonin kesto on lyhyt (yhdestä kolmeen tuntia), potilasta on seurattava tarkasti ja hänelle on annettava toistuvasti naloksonia tarpeen mukaan. Koska suhteellisen vähän lääkettä erittyy virtsaan, pakotetun diureesin ei odoteta olevan tehokas IMODIUM® (loperamidihydrokloridi) yliannostuksessa.
Kliinisissä tutkimuksissa aikuinen, joka otti kolme 20 mg:n annosta 24 tunnin aikana, pahoinpiteli toisen annoksen jälkeen ja oksensi kolmannen annoksen jälkeen. Tutkimuksissa, jotka oli suunniteltu tutkimaan mahdollisia sivuvaikutuksia, jopa 60 mg:n loperamidihydrokloridin tahallinen nauttiminen yhtenä annoksena terveille koehenkilöille ei aiheuttanut merkittäviä haittavaikutuksia.
VASTA-AIHEET
IMODIUM (loperamidi hcl) on vasta-aiheinen potilailla, jotka ovat yliherkkiä loperamidihydrokloridille tai jollekin apuaineista.
IMODIUM (loperamidi hcl) on vasta-aiheinen potilaille, joilla on vatsakipua ripulin puuttuessa.
IMODIUM (loperamidi hcl) -valmistetta ei suositella alle 24 kuukauden ikäisille imeväisille.
IMODIUM (loperamidi hcl) ei tule käyttää ensisijaisena hoitona:
- potilailla, joilla on akuutti punatauti, jolle on ominaista veri ulosteessa ja korkea kuume,
- potilailla, joilla on akuutti haavainen paksusuolitulehdus,
potilailla, joilla on invasiivisten organismien, mukaan lukien Salmonella, Shigella ja Campylobacter, aiheuttama bakteeriperäinen enterokoliitti,
- potilailla, joilla on laajakirjoisten antibioottien käyttöön liittyvä pseudomembranoottinen koliitti.
KLIININEN FARMAKOLOGIA
In vitro ja eläintutkimukset osoittavat, että IMODIUM® (loperamidihydrokloridi) hidastaa suolen motiliteettia ja vaikuttaa veden ja elektrolyyttien liikkumiseen suolen läpi. Loperamidi sitoutuu suolen seinämässä oleviin opiaattireseptoreihin. Näin ollen se estää asetyylikoliinin ja prostaglandiinien vapautumista, mikä vähentää peristaltiaa ja pidentää suoliston läpikulkuaikaa. Loperamidi lisää peräaukon sulkijalihaksen sävyä, mikä vähentää inkontinenssia ja kiireellisyyttä.
Ihmisellä IMODIUM® (loperamidi hcl) pidentää suoliston sisällön kulkuaikaa. Se vähentää päivittäistä ulosteen määrää, lisää viskositeettia ja bulkkitiheyttä sekä vähentää nesteen ja elektrolyyttien menetystä. Toleranssia ripulia estävälle vaikutukselle ei ole havaittu. Kliiniset tutkimukset ovat osoittaneet, että loperamidin näennäinen eliminaation puoliintumisaika ihmisellä on 10,8 tuntia ja vaihteluväli 9,1-14,4 tuntia. Muuttumattoman lääkkeen plasmapitoisuudet pysyvät alle 2 nanogrammassa/ml IMODIUM® (loperamidi hcl) 2 mg:n kapselin nauttimisen jälkeen. Plasman tasot ovat korkeimmillaan noin viisi tuntia kapselin annon jälkeen ja 2,5 tuntia nesteen antamisen jälkeen. Loperamidin huippupitoisuudet plasmassa olivat samanlaiset molemmilla formulaatioilla. Loperamidin eliminaatio tapahtuu pääasiassa oksidatiivisen N-demetyloinnin kautta. Sytokromi P450 (CYP450) isotsyymeillä CYP2C8 ja CYP3A4 uskotaan olevan tärkeä rooli loperamidin N-demetylaatioprosessissa, koska kversetiini (CYP2C8-estäjä) ja ketokonatsoli (CYP3A4-estäjä) estivät N-demetylaatioprosessia merkittävästi in vitro ja 40 %:lla %, vastaavasti. Lisäksi CYP2B6:lla ja CYP2D6:lla näyttää olevan vähäinen rooli loperamidin N-demetylaatiossa. Muuttumattomana loperamidin ja sen metaboliittien erittyminen tapahtuu pääasiassa ulosteiden kautta. Niillä potilailla, joiden biokemiallisia ja hematologisia parametreja seurattiin kliinisten kokeiden aikana, ei havaittu suuntauksia poikkeaviin IMODIUM® (loperamidi hcl) -hoidon aikana. Samoin virtsaanalyysit, EKG ja kliiniset oftalmologiset tutkimukset eivät osoittaneet suuntauksia kohti poikkeavuuksia.
POTILASTIEDOT
Potilaita tulee neuvoa ottamaan yhteyttä lääkäriin, jos heidän ripulinsa ei parane 48 tunnin kuluessa tai jos he havaitsevat verta ulosteessa, nousevat kuumetta tai vatsan turvotusta.
Väsymystä, huimausta tai uneliaisuutta voi esiintyä IMODIUMilla (loperamidi hcl) hoidettujen ripulioireyhtymien yhteydessä. Siksi on suositeltavaa olla varovainen autoa ajaessa tai koneita käytettäessä. (katso HAITTAVAIKUTUKSET ).
