Rhinocort 100mcg Budesonide Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Rhinocort Aqua on ja miten sitä käytetään?
Rhinocort Aqua (budesonidi) -nenäsumute on steroidi, jota käytetään kausiluonteisten tai ympärivuotisten allergioiden aiheuttamien nenäoireiden, kuten tukkoisuuden, aivastelun ja vuotavan nenän hoitoon. Rhinocort Aqua -nenäsumutetta käytetään myös estämään nenäpolyyppien uusiutuminen leikkauksen jälkeen.
Mitkä ovat Rhinocort 100mcg Aquan sivuvaikutukset?
Rhinocort Aqua -nenäsumutteen yleisiä sivuvaikutuksia ovat:
- nenän/kurkun kuivuus tai ärsytys,
- kipeä kurkku,
- yskä,
- aivastelu,
- nenäverenvuoto,
- epämiellyttävä maku/haju,
- haavaumia tai valkoisia läiskiä nenän sisällä tai ympärillä tai
- kipu, turvotus, polttaminen, kutina tai ärsytys nenäsi ympärillä.
Kerro lääkärillesi, jos sinulla on harvinaisia mutta vakavia Rhinocort Aqua -nenäsumutteen sivuvaikutuksia, mukaan lukien:
- maun tai hajun menetys tai
- kipua tai haavaumia nenässäsi.
KUVAUS
Budesonidi, RHINOCORT AQUA (budesonide) nenäsumutteen vaikuttava aine, on tulehdusta ehkäisevä synteettinen kortikosteroidi.
Se on kemiallisesti nimetty (RS)-11-beeta, 16-alfa, 17, 21-tetrahydroksipregna-l,4-dieeni-3,20-dioni sykliseksi 16,17-asetaaliksi butyraldehydin kanssa.
Budesonidia tarjotaan kahden epimeerin (22R ja 22S) seoksena.
Budesonidin empiirinen kaava on C25H34O6 ja sen molekyylipaino on 430,5.
Sen rakennekaava on:
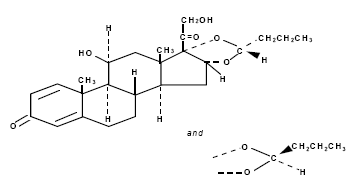
Budesonidi on valkoinen tai luonnonvalkoinen, hajuton jauhe, joka on käytännössä liukenematon veteen ja heptaaniin, liukenee niukasti etanoliin ja liukenee vapaasti kloroformiin.
Sen jakaantumiskerroin oktanolin ja veden välillä pH:ssa 5 on 1,6 x 103.
RHINOCORT AQUA (budesonidi) nenäsumute on hajustamaton, mitattu annos, manuaalinen pumppusuihkeformulaatio, joka sisältää budesonidin mikronisoidun suspension vesipitoisessa väliaineessa. Mikrokiteinen selluloosa ja karboksimetyyliselluloosanatrium, vedetön dekstroosi, polysorbaatti 80, dinatriumedetaatti, kaliumsorbaatti ja puhdistettu vesi sisältyvät tähän väliaineeseen; kloorivetyhappoa lisätään pH:n säätämiseksi tavoitearvoon 4,5.
RHINOCORT 100 mcg AQUA-nenäsumute antaa 32 mikrogrammaa budesonidia per suihke.
Jokainen pullo RHINOCORT 100mcg AQUA (budesonide) Nenäsumutetta 32 mcg sisältää 120 mitattua suihketta ensimmäisen esikäsittelyn jälkeen.
Ennen ensimmäistä käyttöä säiliötä on ravistettava kevyesti ja pumppu on täytettävä painamalla sitä kahdeksan kertaa. Päivittäin käytettäessä pumppua ei tarvitse täyttää uudelleen. Jos sitä ei käytetä kahteen peräkkäiseen päivään, esikäsittele uudelleen yhdellä suihkeella tai kunnes näkyviin tulee hieno suihke. Jos sitä ei ole käytetty yli 14 päivään, huuhtele applikaattori ja esittele kahdella suihkeella tai kunnes hienojakoinen suihke tulee näkyviin.
INDIKAATIOT
Kausiluonteisen tai ympärivuotisen allergisen nuhan hoito
RHINOCORT AQUA (budesonidi) -nenäsumute on tarkoitettu kausiluonteisen tai ympärivuotisen allergisen nuhan nenäoireiden hoitoon aikuisilla ja yli 6-vuotiailla lapsilla.
ANNOSTELU JA HALLINNOINTI
Suositeltu aloitusannos aikuisille ja 6-vuotiaille ja sitä vanhemmille lapsille on 64 mikrogrammaa päivässä annettuna yksi suihke per sieraimeen RHINOCORT AQUA (budesonidi) -nenäsumutetta 32 mikrog kerran päivässä. Jotkut potilaat, jotka eivät saavuta oireiden hallintaa suositellulla aloitusannoksella, voivat hyötyä suurennetusta annoksesta. Suurin suositeltu annos aikuisille (12-vuotiaat ja sitä vanhemmat) on 256 mikrog päivässä annettuna neljänä suihkeena sieraimeen kerran vuorokaudessa RHINOCORT AQUA (budesonidi) -nenäsumutetta 32 mikrog ja suurin suositeltu annos lapsipotilaille (6-
On aina toivottavaa titrata yksittäinen potilas pienimpään tehokkaaseen annokseen sivuvaikutusten mahdollisuuden vähentämiseksi. Nenäoireiden paranemista voidaan havaita potilailla 10 tunnin sisällä RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteen ensimmäisestä käytöstä, mutta kliininen paraneminen kestää yleensä 1–2 päivää ja maksimihyöty noin 2 viikossa. Kun suurin hyöty on saavutettu ja oireet ovat hallinnassa, annoksen pienentäminen voi olla tehokasta allergisen nuhan oireiden hallinnassa potilailla, jotka olivat alun perin hallinnassa suuremmilla annoksilla.
Ennen ensimmäistä käyttöä säiliötä on ravistettava kevyesti ja pumppu on täytettävä painamalla sitä kahdeksan kertaa. Päivittäin käytettäessä pumppua ei tarvitse täyttää uudelleen. Jos sitä ei käytetä kahteen peräkkäiseen päivään, esikäsittele uudelleen yhdellä suihkeella tai kunnes näkyviin tulee hieno suihke. Jos sitä ei ole käytetty yli 14 päivään, huuhtele applikaattori ja esittele kahdella suihkeella tai kunnes hienojakoinen suihke tulee näkyviin. Ravista säiliötä kevyesti ennen jokaista käyttöä.
Kuvitettu Potilaan käyttöohjeet jokaisen RHINOCORT AQUA (budesonidi) -nenäsuihkeen 32 mikrogramman mukana.
MITEN TOIMITETAAN
Annostusmuodot ja vahvuudet
RHINOCORT AQUA (budesonidi) nenäsumute on nenäsumutesuspensio. Jokainen suihke antaa 32 mikrogrammaa budesonidia. Jokainen pullo RHINOCORT 100mcg AQUA (budesonide) Nenäsumutetta 32 mcg sisältää 120 mitattua suihketta ensimmäisen esikäsittelyn jälkeen.
RHINOCORT 100mcg AQUA (budesonidi) nenäsumute 32mcg on saatavana kullanruskeassa lasipullossa, jossa on annospumppusuihke ja vihreä suojakorkki. RHINOCORT 100 mcg AQUA (budesonidi) nenäsumute 32 mcg ( NDC 0186-1070-08) tarjoaa 120 annosruiskua ensimmäisen esikäsittelyn jälkeen; netto täyttöpaino 8,6 g. RHINOCORT 100 mcg AQUA (budesonide) nenäsumute 32 mcg pullo on täytetty ylimäärällä pohjustusaktiivisuuden mahdollistamiseksi. Pullo tulee hävittää 120 suihkeen jälkeen ensimmäisen esikäsittelyn jälkeen, koska sen jälkeen annosteltu budesonidin määrä ruiskua kohden voi olla huomattavasti pienempi kuin etiketissä ilmoitettu annos. Jokainen suihke antaa potilaalle 32 mikrogrammaa budesonidia.
RHINOCORT 100 mcg AQUA (budesonidi) nenäsumutetta tulee säilyttää kontrolloidussa huoneenlämmössä, 20-25°C (68-77°F) venttiili ylhäällä. Ei saa jäätyä. Suojaa valolta. Ravista kevyesti ennen käyttöä. Älä suihkuta silmiin.
Jakelija: AstraZeneca LP, Wilmington, DE 19850. Tarkistettu: 12/2010
SIVUVAIKUTUKSET
Systeeminen ja intranasaalinen kortikosteroidien käyttö voi johtaa seuraaviin:
- Nenäverenvuoto, Candida albicans -infektio, nenän väliseinän perforaatio ja heikentynyt haavan paraneminen [ks. VAROITUKSET JA VAROTOIMET ].
- Yliherkkyys, mukaan lukien anafylaksia [katso VAROITUKSET JA VAROTOIMET ].
- Immunosuppressio [katso VAROITUKSET JA VAROTOIMET ].
- Hyperkortisismi ja lisämunuaisten vajaatoiminta [katso VAROITUKSET JA VAROTOIMET ].
- Kasvuvaikutus [katso VAROITUKSET JA VAROTOIMET ja Käyttö tietyissä populaatioissa ].
- Glaukooma ja kaihi [katso VAROITUKSET JA VAROTOIMET ].
Kokemus kliinisistä kokeista
Koska kliiniset tutkimukset suoritetaan hyvin vaihtelevissa olosuhteissa, lääkkeen kliinisissä tutkimuksissa havaittuja haittavaikutuksia ei voida suoraan verrata toisen lääkkeen kliinisissä tutkimuksissa havaittuihin nopeuksiin, eivätkä ne välttämättä kuvasta käytännössä havaittuja nopeuksia.
Taulukon 1 yleisten haittavaikutusten ilmaantuvuus perustuu kahteen Yhdysvalloissa ja viiteen muuhun kuin Yhdysvalloissa suoritettuun kliiniseen tutkimukseen, joihin osallistui 1 526 potilasta, joilla oli kausiluonteista tai ympärivuotista nuhaa aikuisilla ja ≥ 6-vuotiailla lapsilla, joita hoidettiin RHINOCORT AQUA (budesonidi) nenäsumuteella annoksilla enintään 400 mikrogrammaa kerran päivässä 3-6 viikon ajan. Tähän populaatioon kuului 745 naista ja 781 miestä, joiden keski-ikä oli 31 vuotta (6-85 vuotta, 349 oli 6
Samanlainen haittavaikutusprofiili havaittiin 6–12-vuotiaiden lapsipotilaiden alaryhmässä. Nämä potilaat sisältyvät taulukkoon 1.
Kliinisissä tutkimuksissa 2–3 prosenttia (2–3 %) potilaista keskeytti hoidon haittavaikutusten vuoksi. Systeemisiä kortikosteroidisivuvaikutuksia ei raportoitu kontrolloiduissa kliinisissä tutkimuksissa RHINOCORT AQUA (budesonidi) nenäsumuteella.
Jos suositellut annokset ylittyvät tai henkilöt ovat erityisen herkkiä, voi esiintyä hyperkortismin oireita, eli Gushingin oireyhtymää ja lisämunuaisten vajaatoimintaa.
Markkinoinnin jälkeinen kokemus
Seuraavia haittavaikutuksia on raportoitu RHINOCORT AQUA (budesonidi) -nenäsumutteen hyväksymisen jälkeisen käytön aikana. Koska nämä reaktiot on raportoitu vapaaehtoisesti epävarman kokoisesta populaatiosta, ei ole aina mahdollista luotettavasti arvioida niiden esiintymistiheyttä tai määrittää syy-yhteyttä lääkkeelle altistumiseen.
Immuunijärjestelmän häiriöt: välittömät ja viivästyneet yliherkkyysreaktiot (mukaan lukien anafylaktinen reaktio, nokkosihottuma, ihottuma, ihottuma, angioödeema ja kutina), [ks. VAROITUKSET JA VAROTOIMET ja VASTA-AIHEET ]
Silmäsairaudet: glaukooma, kohonnut silmänpaine, kaihi [katso VAROITUKSET JA VAROTOIMET ]
Hengityselimet, rintakehä ja välikarsina: nenän väliseinän perforaatio, anosmia, nieluhäiriöt (kurkun ärsytys, kurkun kipu, kurkun turvotus, polttava kurkku ja kutiseva kurkku) ja hengityksen vinkuminen
Sydämen häiriöt: sydämentykytys
Tuki- ja liikuntaelimistön ja sidekudoksen häiriöt: kasvun estäminen [katso VAROITUKSET JA VAROTOIMET ja Käyttö tietyissä populaatioissa ]
HUUMEIDEN VUOROVAIKUTUKSET
Sytokromi P450 3A4:n estäjät
Kortikosteroidien, mukaan lukien budesonidin, pääasiallinen metaboliareitti on sytokromi P450 (CYP) -isoentsyymi 3A4 (CYP3A4). Ketokonatsolin, voimakkaan CYP3A4:n estäjän, oraalisen annon jälkeen suun kautta annetun budesonidin keskimääräinen plasmapitoisuus nousi. CYP3A4:n samanaikainen anto voi estää budesonidin metaboliaa ja lisätä systeemistä altistusta budesonidille. Varovaisuutta tulee noudattaa harkittaessa RHINOCORT AQUA (budesonidi) nenäsumutteen antoa samanaikaisesti pitkäaikaisen ketokonatsolin ja muiden tunnettujen vahvojen CYP3A4:n estäjien (esim. ritonaviiri, atatsanaviiriklaritromysiini, indinaviiri-itrakonatsoli, nefatsodoni nelfinaviiri-satelitrokinaviiri) kanssa. VAROITUKSET JA VAROTOIMET ja KLIININEN FARMAKOLOGIA ].
VAROITUKSET
Mukana osana VAROTOIMENPITEET osio.
VAROTOIMENPITEET
Paikalliset nenävaikutukset
Nenäverenvuoto
Kliinisissä 3–52 viikkoa kestäneissä tutkimuksissa nenäverenvuotoa havaittiin useammin potilailla, joita hoidettiin RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumuteella kuin lumelääkettä saaneilla [ks. HAITTAVAIKUTUKSET ].
Candida-infektio
Kliinisissä tutkimuksissa, joissa budesonidia annettiin intranasaalisesti, on esiintynyt Candida albicansin aiheuttamia paikallisia infektioita nenään ja nieluun. Kun tällainen infektio kehittyy, se voi vaatia hoitoa sopivalla paikallisella tai systeemisellä hoidolla ja RHINOCORT AQUA (budesonidi) -nenäsumutehoidon lopettamista. Potilaat, jotka käyttävät RHINOCORT AQUA (budesonidi) -nenäsumutetta useiden kuukausien ajan tai pidempään, on tutkittava säännöllisesti Candida-infektion tai muiden nenän limakalvojen haittavaikutusten merkkien varalta.
Nenän väliseinän perforaatio
Nenän väliseinän perforaatiotapauksia on raportoitu kortikosteroidien, mukaan lukien budesonidin, intranasaalisen annon jälkeen [ks. HAITTAVAIKUTUKSET ].
Heikentynyt haavan paraneminen
Kortikosteroidien haavan paranemista estävän vaikutuksen vuoksi potilaiden, jotka ovat kokeneet äskettäin nenän väliseinän haavaumia, nenäleikkauksia tai nenävamman, ei tule käyttää nenän kortikosteroideja ennen kuin ne ovat parantuneet.
Yliherkkyysreaktiot, mukaan lukien anafylaksia
Yliherkkyysreaktioita, mukaan lukien anafylaktinen reaktio, nokkosihottuma, ihottuma, ihottuma, angioödeema ja kutina, saattaa esiintyä [ks. VASTA-AIHEET ja HAITTAVAIKUTUKSET, Markkinoinnin jälkeinen kokemus ].
Immunosuppressio
Potilaat, jotka käyttävät immuunijärjestelmää heikentäviä lääkkeitä, ovat alttiimpia infektioille kuin terveet henkilöt. Esimerkiksi vesirokko ja tuhkarokko voivat olla vakavampia tai jopa kuolemaan johtavia kortikosteroideja käyttävillä herkillä lapsilla tai aikuisilla. Tällaisilla lapsilla tai aikuisilla, joilla ei ole ollut näitä sairauksia tai jotka eivät ole asianmukaisesti rokotettuja, tulee olla erityisen varovaisia altistumisen välttämiseksi. Ei tiedetä, miten kortikosteroidien annos, reitti ja annon kesto vaikuttavat levinneen infektion kehittymisriskiin. Perussairauden ja/tai aiemman kortikosteroidihoidon osuutta riskiin ei myöskään tunneta. Jos altistut vesirokolle, hoito varicella zoster -immunoglobuliinilla (VZIG) tai yhdistetyllä suonensisäisellä immunoglobuliinilla (WIG) voi olla aiheellista. Jos altistuminen tuhkarokkolle, ehkäisy yhdistetyn intramuskulaarisen immunoglobuliinin (IG) avulla voi olla aiheellista. (Katso vastaavat pakkausselosteet täydelliset VZIG- ja IG-lääkemääräystiedot ). Jos vesirokko kehittyy, hoitoa viruslääkkeillä voidaan harkita.
Vesirokko- tai tuhkarokko-infektion kliinistä etenemistä intranasaalisia tai inhaloitavia kortikosteroideja käyttävillä potilailla ei ole tutkittu. Vaikka intranasaalisista kortikosteroideista ei ole tietoa, kliinisessä tutkimuksessa on tutkittu immuunivastetta vesirokkorokotteelle 12 kuukauden ja 8 vuoden ikäisillä astmapotilailla, joita hoidettiin budesonidin inhalaatiosuspensiolla.
Avoimessa, ei-satunnaistetussa kliinisessä tutkimuksessa tarkasteltiin immuunivastetta vesirokkorokotteelle 243:lla 12 kuukauden–8-vuotiaalla astmapotilaalla, joita hoidettiin budesonidin inhalaatiosuspensiolla 0,25–1 mg päivässä (n=151) tai ei-kortikosteroidihoidolla. (n = 92) (eli beeta-agonistit, leukotrieenireseptoriantagonistit tai kromonit). Niiden potilaiden prosenttiosuus, joille kehittyi seroprotektiivinen vasta-ainetiitteri ≥ 5,0 (gpELISA-arvo) vasteena rokotukseen, oli samanlainen potilailla, joita hoidettiin budesonidin inhalaatiosuspensiolla (85 %) kuin potilailla, joita hoidettiin ei-kortikosteroidihoitoa saaneilla astmahoidoilla (90 %). Yhdellekään budesonidin inhalaatiosuspensiolla hoidetulle potilaalle ei kehittynyt vesirokkoa rokotuksen seurauksena.
Kortikosteroideja tulee käyttää varoen, jos ollenkaan, potilailla, joilla on aktiivinen tai lepotilassa oleva tuberkuloosiinfektio, hoitamaton sieni-, bakteeri-, systeeminen virus- tai loisinfektio. tai silmän herpes simplex.
Hypotalamus-aivolisäke-lisämunuaisen akselin vaikutukset
Hyperkortisismi ja lisämunuaisten vajaatoiminta: Kun intranasaalisia steroideja käytetään suositeltua suurempina annoksina tai herkille henkilöille suositelluilla annoksilla, systeemisiä kortikosteroidivaikutuksia, kuten hyperkortismia ja lisämunuaisten vajaatoimintaa, saattaa ilmetä. Jos tällaisia muutoksia tapahtuu, RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutteen annostelu tulee lopettaa hitaasti, noudattaen hyväksyttyjä menettelyjä suun kautta otettavan kortikosteroidihoidon lopettamiseksi.
Systeemisen kortikosteroidin korvaamiseen paikallisella kortikosteroidilla voi liittyä merkkejä lisämunuaisten vajaatoiminnasta, ja lisäksi joillakin potilailla voi esiintyä kortikosteroidien vieroitusoireita, kuten nivel- ja/tai lihaskipua, väsymystä, heikkoutta, pahoinvointia, oksentelua, hypotensiota, väsymys ja masennus. Potilaat, joita on aiemmin hoidettu pitkiä aikoja systeemisillä kortikosteroideilla, tulee vieroittaa hitaasti, kun heidät siirretään paikallisiin kortikosteroideihin, ja niitä tulee tarkkailla huolellisesti akuutin lisämunuaisen vajaatoiminnan varalta vasteena stressiin. Potilailla, joilla on astma tai jokin muu kliininen sairaus, joka vaatii pitkäaikaista systeemistä kortikosteroidihoitoa, systeemisten kortikosteroidien annoksen liian nopea lasku voi aiheuttaa vakavan oireiden pahenemisen.
Vuorovaikutukset vahvojen sytokromi P450 3A4 -estäjien kanssa
Varovaisuutta tulee noudattaa harkittaessa RHINOCORT AQUA -nenäsumutteen antoa samanaikaisesti ketokonatsolin ja muiden tunnettujen vahvojen CYP3A4-estäjien (esim. ritonaviiri, atatsanaviiri, klaritromysiini, indinaviiri, itrakonatsoli, nefatsodoni, nelfinaviiri, sakinaviiri, telitromysiinin haittavaikutukset) kanssa. systeemistä altistumista budesonidille saattaa esiintyä [ks LÄÄKKEIDEN VUOROVAIKUTUKSET, KLIININEN FARMAKOLOGIA ].
Vaikutus kasvuun
Nenänsisäiset kortikosteroidit, mukaan lukien budesonidi, voivat hidastaa kasvunopeutta, kun niitä annetaan lapsipotilaille. Seuraa rutiininomaisesti niiden lapsipotilaiden kasvua, jotka saavat pitkäaikaista hoitoa RHINOCORT 100 mcg AQUA (budesonidi) nenäsumuteella. Intranasaalisten kortikosteroidien systeemisten vaikutusten minimoimiseksi, mukaan lukien RHINOCORT AQUA (budesonidi) -nenäsumute, titraa kunkin potilaan annos pienimpään annostukseen, joka hallitsee hänen oireitaan tehokkaasti [ks. Käyttö tietyissä populaatioissa, lasten käyttöön ].
Glaukooma ja kaihi
Glaukoomaa, kohonnutta silmänpainetta ja kaihia on raportoitu kortikosteroidien, mukaan lukien budesonidin, intranasaalisen annon jälkeen. Siksi tarkka seuranta on aiheellista potilailla, joilla on muutos näkökyvyssä tai joilla on aiemmin ollut kohonnut silmänpaine, glaukooma ja/tai kaihi [ks. HAITTAVAIKUTUKSET ].
Potilasneuvontatiedot
[Katso FDA:n hyväksymä potilasmerkintä ]
Potilaiden, joita hoidetaan RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteella, tulee saada seuraavat tiedot ja ohjeet. Näiden tietojen tarkoituksena on auttaa potilasta lääkkeen turvallisessa ja tehokkaassa käytössä. Se ei ole kaikkien mahdollisten haitallisten tai suunniteltujen vaikutusten paljastaminen. RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteen oikeaa käyttöä varten ja maksimaalisen parannuksen saavuttamiseksi potilaan tulee lukea ja noudattaa mukana tulevaa FDA:n hyväksymää potilasmerkintää.
Paikalliset nenävaikutukset
Potilaille tulee kertoa, että joillakin potilailla nenässä ja nielussa esiintyi nenäverenvuotoa ja paikallisia Candida albicans -infektioita. Jos kandidiaasi kehittyy, se tulee hoitaa sopivalla paikallisella tai systeemisellä hoidolla ja lopettaa hoito RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutteella. Lisäksi nenän kortikosteroideihin liittyy nenän väliseinän perforaatio ja heikentynyt haavan paraneminen. Potilaiden, joilla on ollut äskettäin nenähaavoja, nenäleikkauksia tai nenävammoja, ei tule käyttää RHINOCORT AQUA (budesonidi) -nenäsumutetta, ennen kuin parantunut on tapahtunut [ks. VAROITUKSET JA VAROTOIMET ].
Yliherkkyys, mukaan lukien anafylaksia
Potilaita tulee kertoa, että yliherkkyysreaktioita, mukaan lukien anafylaktinen reaktio, nokkosihottuma, ihottuma, ihottuma, angioedeeema ja kutina, on raportoitu käytettäessä RHINOCORT AQUA (budesonidi) -nenäsumutetta. Lopettaa
RHINOCORT AQUA (budesonidi) nenäsumutetta, jos tällaisia reaktioita esiintyy [katso VASTA-AIHEET, VAROITUKSET JA VAROTOIMET ja HAITTAVAIKUTUKSET ].
Immunosuppressio
Potilaita, jotka saavat immuunivastetta heikentäviä kortikosteroidiannoksia, tulee varoittaa välttämään altistumista vesirokolle tai tuhkarokkolle ja ottamaan yhteyttä lääkäriin välittömästi, jos he altistuvat. Potilaille on kerrottava olemassa olevan tuberkuloosin, sieni-, bakteeri-, virus- tai loisinfektion tai silmän herpes simplexin mahdollisesta pahenemisesta [ks. VAROITUKSET JA VAROTOIMET ].
Alennettu kasvunopeus
Potilaita tulee kertoa, että nenänsisäiset kortikosteroidit, mukaan lukien budesonidi, voivat hidastaa kasvunopeutta, kun niitä annetaan lapsipotilaille. Lääkäreiden tulee seurata tarkasti lasten ja nuorten kasvua, jotka käyttävät kortikosteroideja millä tahansa reitillä [ks. VAROITUKSET JA VAROTOIMET ].
Glaukooma ja kaihi
Potilaita tulee kertoa, että nenänsisäisten kortikosteroidien, mukaan lukien budesonidin, pitkäaikainen käyttö saattaa lisätä joidenkin silmäongelmien (kaihi ja glaukooma) riskiä. Potilaiden tulee ilmoittaa terveydenhuollon tarjoajalleen, jos näönmuutos havaitaan RHINOCORT AQUA (budesonidi) -nenäsumutteen käytön aikana [ks. VAROITUKSET JA VAROTOIMET ].
Käytä Päivittäin
Potilaiden tulee käyttää RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutetta säännöllisin väliajoin, koska sen tehokkuus riippuu sen säännöllisestä käytöstä. Potilaat voivat huomata nenäoireiden paranemisen 10 tunnin sisällä RHINOCORT AQUA (budesonidi) -nenäsumutteen ensimmäisestä käytöstä. Suurin hyöty voidaan saavuttaa vasta noin 2 viikon kuluttua hoidon aloittamisesta [katso ANNOSTELU JA HALLINNOINTI ].
Potilaiden tulee ottaa lääkitys ohjeiden mukaan, eivätkä ne saa ylittää määrättyä annosta. Potilaan tulee ottaa yhteyttä lääkäriin, jos oireet eivät parane kahden viikon kuluttua tai jos tila pahenee. Potilaiden, joilla on toistuvia nenäverenvuotoja (nenäverenvuotoa) tai epämukavuutta nenän väliseinässä tämän lääkkeen käytön aikana, tulee ottaa yhteyttä lääkäriin. RHINOCORT AQUA (budesonidi) -nenäsumutteen oikeaa käyttöä varten ja maksimaalisen parannuksen saavuttamiseksi potilaan tulee lukea mukana olevat potilastiedot huolellisesti ja seurata niitä. Älä käytä RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutetta sen jälkeen, kun merkitty määrä suihkeita on käytetty (ei sisällä pohjustusta) tai pakkauksessa tai pullon etiketissä olevan viimeisen käyttöpäivämäärän jälkeen.
Kuinka käyttää RHINOCORT 100mcg AQUA (budesonidi) nenäsumutetta
Potilaita on opastettava huolellisesti tämän lääkevalmisteen käytöstä optimaalisen annostelun varmistamiseksi [katso POTILASTIEDOT ].
Ei-kliininen toksikologia
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Sprague-Dawley-rotilla tehdyssä 104 viikkoa kestäneessä suun kautta annetussa tutkimuksessa glioomien esiintyvyyden lisääntyminen havaittiin tilastollisesti merkitsevästi urosrotilla, jotka saivat suun kautta budesonidia 50 mikrogrammaa/kg/vrk (noin kaksi kertaa nenänsisäiseen vuorokausiannokseen verrattuna). aikuiset ja lapset mcg/m2 perusteella). Tuumorigeenisyyttä ei havaittu urosrotilla oraalisilla annoksilla 25 mikrog/kg asti (suunnilleen sama kuin suurin suositeltu päivittäinen intranasaalinen annos aikuisille ja lapsille mikrog/m2:n perusteella, eikä naarasrotilla oraalisilla annoksilla 50 mcg/kg asti noin kaksi kertaa suurin suositeltu intranasaalinen päiväannos aikuisilla ja lapsilla mikrog/m2:n perusteella). Kahdessa kaksivuotisessa lisätutkimuksessa Fischer- ja Sprague-Dawley-urosrotilla budesonidi ei aiheuttanut glioomia suun kautta annetulla annoksella 50 mikrogrammaa/kg (noin kaksinkertainen aikuisten ja lasten suurin suositeltu intranasaalinen päivittäinen annos mikrog/m2:n perusteella). Sprague-Dawley-urosrotilla budesonidi kuitenkin lisäsi tilastollisesti merkitsevää maksasolukasvainten esiintyvyyttä oraalisella annoksella 50 mcg/kg (noin kaksinkertainen aikuisten ja lasten suurin suositeltu intranasaalinen päivittäinen annos mikrog/m2-pohjaisesti. ). Samanaikaiset vertailukortikosteroidit (prednisoloni ja triamsinoloniasetonidi) näissä kahdessa tutkimuksessa osoittivat samanlaisia tuloksia.
Ei ollut todisteita karsinogeenisestä vaikutuksesta, kun budesonidia annettiin suun kautta 91 viikon ajan hiirille annoksina 200 mikrogrammaa/kg/vrk (noin 3 kertaa suurin suositeltu intranasaalinen päiväannos aikuisille ja lapsille mikrog/m2:n perusteella). .
Budesonidi ei ollut mutageeninen tai klastogeeninen kuudessa eri testijärjestelmässä: Amesin salmonella/mikrosomilevytesti, hiiren mikrotumatesti, hiiren lymfoomatesti, kromosomipoikkeamatesti ihmisen lymfosyyteillä, sukupuoleen liittyvä resessiivinen letaalitesti Drosophila melanogasterissa ja DNA-korjausanalyysi rotalla. hepatosyyttiviljelmä.
Rotilla budesonidilla ei ollut vaikutusta hedelmällisyyteen ihonalaisilla annoksilla 80 mikrog/kg asti (noin 3 kertaa aikuisten suurin suositeltu intranasaalinen päiväannos mikrog/m2:n perusteella).
Ihonalainen annos 20 mcg/kg/vrk (pienempi kuin suurin suositeltu päivittäinen intranasaalinen annos aikuisille mikrog/m2:n perusteella laskettuna) vähentää äidin painonnousua, syntymää edeltävää elinkykyä ja poikien elinkykyä syntymän ja imetyksen aikana. havaittiin. Tällaisia vaikutuksia ei havaittu annoksella 5 mikrog/kg (pienempi kuin suurin suositeltu vuorokausiannos aikuisille mikrog/m2:n perusteella).
Käyttö tietyissä populaatioissa
Raskaus
Teratogeeniset vaikutukset: Raskausluokka B. Budesonidin vaikutus ihmisen raskauden tuloksiin on arvioitu syntymärekisterien arvioiden avulla, jotka liittyvät äidin inhaloitavan budesonidin (eli PULMICORT TURBUHALER) ja nenänsisäisesti annettavan budesonidin (eli RHINOCORT 100 mikrogrammaa) AQUA (budesonidi) käyttöön. Tulokset väestöpohjaisista prospektiivisistä kohorttiepidemiologisista tutkimuksista, joissa tarkasteltiin tietoja kolmesta ruotsalaisesta rekisteristä, jotka kattavat noin 99 % raskauksista vuosina 1995–2001 (eli Ruotsin lääketieteellinen syntymärekisteri; synnynnäisten epämuodostumien rekisteri; lasten kardiologian rekisteri), ei osoita lisääntynyttä riskiä kokonaisriskille. synnynnäiset epämuodostumat, jotka johtuvat inhaloitavan tai intranasaalisen budesonidin käytöstä raskauden alkuvaiheessa.
Synnynnäisiä epämuodostumia tutkittiin 2 014 lapsella, joiden äidit ilmoittivat käyttäneensä inhaloitavaa budesonidia astman hoitoon raskauden alkuvaiheessa (yleensä 10–12 viikkoa viimeisten kuukautisten jälkeen), jolloin esiintyy useimmat tärkeimmät elinten epämuodostumat.1 Synnynnäisten epämuodostumien yleisyys oli samanlainen verrattuna väestön yleiseen asteeseen (3,8 % vs. 3,5 %). Suu-kasvohalkeamilla ja sydänvioilla syntyneiden imeväisten määrä oli sama kuin väestön odotettu lukumäärä (4 lasta vs. 3,3 ja 18 lasta vs. 17-18). Jatkotutkimuksessa, jossa imeväisten kokonaismäärä nostettiin 2 534:ään, synnynnäisten epämuodostumien yleisyys pikkulapsilla, joiden äidit altistivat inhaloitavalle budesonidille raskauden alkuvaiheessa, ei eronnut kaikkien vastasyntyneiden määrästä samana ajanjaksona (3,6 %). ).2 Ruotsin lääketieteellisen syntymärekisterin kolmas tutkimus, jossa käsiteltiin 2 968 raskautta, jotka olivat altistuneet hengitetylle budesonidille. Suurin osa niistä oli ensimmäisen raskauskolmanneksen altistumista, raportoitu raskausikä, syntymäpaino, syntymän pituus, kuolleena syntyneet lapset ja moninkertaiset synnytykset, jotka olivat samanlaisia altistuneilla vauvoilla verrattuna altistumattomat pikkulapset.3
Synnynnäisiä epämuodostumia tutkittiin 2 113 lapsella, joiden äidit ilmoittivat käyttäneensä intranasaalista budesonidia raskauden alkuvaiheessa. Synnynnäisten epämuodostumien yleisyys oli samanlainen kuin väestössä (4,5 % vs. 3,5 %). Oikaistu kerroinsuhde (OR) oli 1,06 (95 % CI 0,86-1,31). Suu-kasvohalkiolla syntyneiden imeväisten määrä oli sama kuin väestön odotettu lukumäärä (3 lasta vs. 3, vastaavasti). Sydänvioista syntyneiden vauvojen määrä ylitti odotetun väestön (28 lasta vs. 17,8). Intranasaalisen budesonidin systeeminen altistuminen on 6 kertaa pienempi kuin inhaloitavan budesonidin, eikä sydänvaurioiden yhteyttä havaittu suuremman budesonidialtistuksen kanssa.
Eläinlöydöistä huolimatta näyttää siltä, että sikiövaurioiden mahdollisuus on vähäinen, jos lääkettä käytetään raskauden aikana. Koska ihmisillä tehdyt tutkimukset eivät kuitenkaan voi sulkea pois haittojen mahdollisuutta, RHINOCORT AQUA (budesonidi) -nenäsumutetta tulee käyttää raskauden aikana vain, jos se on selvästi tarpeen.
Budesonidi aiheutti sikiön menetystä, alensi poikasten painoa ja luuston poikkeavuuksia kaniineilla annetulla ihonalaisella annoksella, joka oli noin 2 kertaa suurin suositeltu päivittäinen intranasaalinen annos aikuisilla mikrog/m2:n perusteella laskettuna, ja ihonalaisella annoksella rotilla, joka oli noin 16 kertaa suurempi kuin Suurin suositeltu intranasaalinen päiväannos aikuisille mikrog/m2-pohjaisesti. Rotilla ei havaittu teratogeenisia tai alkioita tappavia vaikutuksia, kun budesonidia annettiin inhalaationa annoksina, jotka olivat enintään noin 8-kertaisia aikuisille suositeltuun maksimaaliseen intranasaaliseen vuorokausiannokseen mikrogrammaa/m2:n perusteella.
Oraalisista kortikosteroideista saadut kokemukset niiden käyttöönoton jälkeen farmakologisissa annoksissa, toisin kuin fysiologisissa annoksissa, viittaavat siihen, että jyrsijät ovat alttiimpia kortikosteroidien teratogeenisille vaikutuksille kuin ihmiset.
Ei-teratogeeniset vaikutukset: Hypoadrenalismia voi esiintyä imeväisillä, joiden äidit ovat saaneet kortikosteroideja raskauden aikana. Tällaisia lapsia tulee tarkkailla huolellisesti.
Imettävät äidit
Budesonidi erittyy äidinmaitoon. Kuivajauheinhalaattorilla annetusta budesonidia koskevat tiedot osoittavat, että rintamaidossa imeväiselle saatavilla oleva budesonidin päivittäinen kokonaisannos on noin 0,3–1 % äidin hengittämästä annoksesta [ks. KLIININEN FARMAKOLOGIA, Farmakokinetiikka, Erityisryhmät, Hoito ]. Imettävillä naisilla ei ole tehty tutkimuksia erityisesti RHINOCORT 100mcg AQUA -nenäsumuteella; Vauvan äidinmaidossa saatavilla olevan budesonidin annoksen prosenttiosuutena äidin annoksesta odotetaan kuitenkin olevan samanlainen. RHINOCORT AQUA (budesonidi) nenäsumutetta tulee käyttää imettäville naisille vain, jos se on kliinisesti tarkoituksenmukaista. Lääkkeen määrääjien tulee punnita imetyksen tunnetut hyödyt äidille ja lapselle ja imeväisen minimaalisen budesonidialtistuksen mahdollisia riskejä. Annostusnäkökohtiin kuuluvat lääkemääräys tai titraus pienimpään kliinisesti tehokkaaseen annokseen ja RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteen käyttö välittömästi imetyksen jälkeen annostelun ja imetyksen välisen ajan maksimoimiseksi imeväisen altistumisen minimoimiseksi.
Käyttö lapsille
Turvallisuutta ja tehoa alle 6-vuotiailla lapsipotilailla ei ole varmistettu.
Kontrolloidut kliiniset tutkimukset ovat osoittaneet, että intranasaaliset kortikosteroidit voivat hidastaa kasvunopeutta lapsipotilailla. Tämä vaikutus on havaittu hypotalamus-aivolisäke-lisämunuaisen (HPA)-akselin suppressiosta puuttuessa, mikä viittaa siihen, että kasvunopeus on herkempi indikaattori systeemiselle kortikosteroidialtistukselle lapsipotilailla kuin jotkut yleisesti käytetyt HPA-akselin toiminnan testit. . Tämän intranasaalisiin kortikosteroideihin liittyvän kasvunopeuden hidastumisen pitkän aikavälin vaikutuksia, mukaan lukien vaikutusta aikuisen lopulliseen pituuteen, ei tunneta. Nenänsisäisten kortikosteroidien hoidon lopettamisen jälkeistä "kiihtymiskasvun" mahdollisuutta ei ole tutkittu riittävästi.
Nenänsisäisiä kortikosteroideja, mukaan lukien RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutetta saavien lapsipotilaiden kasvua on seurattava rutiininomaisesti (esim. stadiometrisesti). Pitkäaikaisen hoidon mahdollisia kasvuvaikutuksia tulee punnita saavutettuihin kliinisiin hyötyihin ja vaihtoehtoisiin hoitoihin liittyviin riskeihin ja hyötyihin nähden. Intranasaalisten kortikosteroidien systeemisten vaikutusten minimoimiseksi, mukaan lukien RHINOCORT AQUA (budesonidi) -nenäsumute, jokainen potilas tulee titrata pienimpään annokseen, joka hallitsee hänen oireitaan tehokkaasti.
Vuoden mittainen lumekontrolloitu kliininen kasvututkimus tehtiin 229:llä lapsipotilaalla (4–8-vuotiaat) RHINOCORT AQUA (budesonidi) -nenäsumutteen (64 mikrogramman kerta-annos, suositeltu aloitusannos) tehon arvioimiseksi. 6-vuotiaille ja sitä vanhemmille lapsille) kasvunopeuden perusteella. Populaatiosta, jossa oli 141 potilasta, jotka saivat RHINOCORT 100 mcg AQUA (budesonidi) nenäsumutetta ja 67 lumelääkettä, kasvunopeuden pistearvio RHINOCORT AQUA (budesonidi) nenäsumuteella oli 0,25 cm/vuosi pienempi kuin lumelääke (95 %:n luottamusväli) vaihtelevat 0,59 cm/vuosi pienempi kuin lumelääke ja 0,08 cm/vuosi korkeampi kuin lumelääke).
Tutkimuksessa 5–12-vuotiailla astmaatikoilla lapsilla, jotka saivat budesonidia kuivajauheinhalaattorilla 200 mikrogrammaa kahdesti vuorokaudessa (n = 311), kasvu hidastui 1,1 senttimetriä lumelääkettä saaneisiin (0,433 tuumaa). n=418) vuoden lopussa; näiden kahden hoitoryhmän välinen ero ei kasvanut enempää kolmen vuoden lisähoidon aikana. Neljän vuoden loppuun mennessä budesonidikuivajauheinhalaattorilla hoidetuilla lapsilla ja lumelääkettä saavilla lapsilla oli samanlainen kasvunopeus. Tästä tutkimuksesta tehtyjä johtopäätöksiä saattaa hämmentää kortikosteroidien epätasainen käyttö hoitoryhmissä ja tutkimusten aikana murrosiän saavuttaneiden potilaiden tietojen sisällyttäminen.
Inhaloitavien kortikosteroidien systeemiset vaikutukset liittyvät systeemiseen altistumiseen tällaisille lääkkeille. Farmakokineettiset tutkimukset ovat osoittaneet, että sekä aikuisilla että lapsilla systeemisen altistuksen budesonidille RHINOCORT AQUA (budesonidi) -nenäsumutteen suurimmilla suositelluilla annoksilla ei odoteta olevan suurempi kuin altistuminen pienimmille suositelluilla annoksilla kuivajauheinhalaattorin kautta. Siksi RHINOCORT AQUA (budesonidi) -nenäsumutteesta toimitetun budesonidin systeemisten vaikutusten (HPA-akseli ja kasvu) ei odoteta olevan suurempia kuin inhaloitavan budesonidin raportoitu, kun sitä annetaan kuivajauheinhalaattorin kautta.
Ei voida sulkea pois mahdollisuutta, että RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumute aiheuttaa kasvun hidastumista herkillä potilailla tai kun sitä annetaan yli 64 mikrogramman vuorokaudessa. Suositeltu annosalue 6–11-vuotiaille potilaille on 64–128 mikrog päivässä [ks. ANNOSTELU JA HALLINNOINTI ].
Geriatrinen käyttö
RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutteen kliinisissä tutkimuksissa 2 461 potilaasta 5 % oli 60-vuotiaita tai vanhempia. Näiden koehenkilöiden ja nuorempien koehenkilöiden välillä ei havaittu yleisiä eroja turvallisuudessa tai tehokkuudessa, lukuun ottamatta haittavaikutuksia, jotka raportoivat nenäverenvuotoa, joka lisääntyi iän myötä. Muut raportoidut kliiniset kokemukset eivät myöskään ole osoittaneet muita eroja iäkkäiden ja nuorempien potilaiden vasteissa, mutta joidenkin iäkkäiden henkilöiden suurempaa herkkyyttä ei voida sulkea pois.
Maksan vajaatoiminta
Virallisia farmakokineettisiä tutkimuksia, joissa käytettiin RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutetta, ei ole tehty potilailla, joilla on maksan vajaatoiminta. Koska budesonidi kuitenkin eliminoituu pääasiassa maksametaboliassa, maksan toiminnan heikkeneminen voi johtaa budesonidin kertymiseen plasmaan. Siksi potilaita, joilla on maksasairaus, tulee seurata tarkasti.
YLIANNOSTUS
Akuutti yliannostus tällä annosmuodolla on epätodennäköistä, koska yksi 120 suihkepullo RHINOCORT 100 mcg AQUA (budesonide) nenäsumutetta 32 mcg sisältää vain noin 5,4 mg budesonidia. Krooninen yliannostus voi aiheuttaa hyperkortismin merkkejä/oireita [katso VAROITUKSET JA VAROTOIMET ].
VASTA-AIHEET
RHINOCORT AQUA (budesonidi) nenäsumute on vasta-aiheinen potilaille, jotka ovat yliherkkiä jollekin sen aineosista [ks. VAROITUKSET JA VAROTOIMET ].
KLIININEN FARMAKOLOGIA
Toimintamekanismi
Budesonidi on anti-inflammatorinen kortikosteroidi, jolla on voimakas glukokortikoidiaktiivisuus ja heikko mineralokortikoidiaktiivisuus. Tavallisissa in vitro ja eläinmalleissa budesonidilla on noin 200 kertaa suurempi affiniteetti glukokortikoidireseptoriin ja 1000 kertaa suurempi paikallisesti käytettävä tulehdusta ehkäisevä teho kuin kortisolilla (rotan krotoniöljykorvan ödeemamääritys). Systeemisen aktiivisuuden mittana budesonidi on 40 kertaa tehokkaampi kuin kortisoli ihonalaisesti annettuna ja 25 kertaa tehokkaampi oraalisesti annettuna rotan kateenkorvan involuutiotestissä. Tämän kliinistä merkitystä ei tunneta.
RHINOCORT 100 mcg AQUA-nenäsumutteen vaikutus johtuu alkuperäisestä lääkkeestä, budesonidista. Glukokortikoidireseptorin affiniteettitutkimuksissa 22R-muoto oli kaksi kertaa niin aktiivinen kuin 22S-epimeeri. In vitro -tutkimukset osoittivat, että budesonidin kaksi muotoa eivät muutu keskenään.
Kortikosteroidien tarkkaa mekanismia tulehdukseen kausittaisessa ja ympärivuotisessa allergisessa nuhassa ei tunneta hyvin. Tulehdus on tärkeä osa kausiluonteisen ja ympärivuotisen allergisen nuhan patogeneesiä. Kortikosteroideilla on laaja valikoima estäviä vaikutuksia useisiin solutyyppeihin (esim. syöttösolut, eosinofiilit, neutrofiilit, makrofagit ja lymfosyytit) ja välittäjiin (esim. histamiini, eikosanoidit, leukotrieenit ja sytokiinit), jotka ovat mukana allergisissa ja ei-allergisissa välitteissä. tulehdus. Nämä kortikosteroidien anti-inflammatoriset vaikutukset voivat edistää niiden tehoa kausiluonteisessa ja ympärivuotisessa allergisessa nuhassa.
Farmakodynamiikka
Kolmen viikon kliininen tutkimus kausiluonteisesta nuhasta, jossa verrattiin RHINOCORT 100 mikrogramman nenäinhalaattoria, suun kautta nautittua budesonidia ja lumelääkettä 98 potilaalla, joilla oli koivun siitepölyn aiheuttama allerginen nuha, osoitti, että RHINOCORT-nenäinhalaattorin terapeuttinen vaikutus voidaan katsoa johtuvan paikallisista vaikutuksista. budesonidi.

HPA Axis Effects
RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutteen vaikutuksia lisämunuaisten toimintaan on arvioitu useissa kliinisissä tutkimuksissa. Neljän viikon kliinisessä tutkimuksessa 61 aikuispotilaalla, jotka saivat 256 mikrogrammaa päivässä RHINOCORT AQUA (budesonidi) -nenäsumutetta, ei havaittu merkittäviä eroja lumelääkettä saaneista potilaista plasman kortisolitasoissa, jotka mitattiin ennen 0,25 mg:n intramuskulaarista kosyntropiinia ja 60 minuuttia sen jälkeen. Virtsan 24 tunnin kortisolimittauksissa ei ollut johdonmukaisia eroja potilailla, jotka saivat enintään 400 mikrogrammaa päivässä. Samanlaisia tuloksia havaittiin tutkimuksessa, johon osallistui 150 lasta ja nuorta, jotka olivat iältään 6–17-vuotiaita, sairastavat jatkuvaa nuhaa ja joita hoidettiin 256 mikrogrammalla päivässä 12 kuukauden ajan.
Kun RHINOCORT AQUA (budesonidi) -nenäsumutetta (256 mcg) oli hoidettu seitsemän päivän ajan suositellulla enimmäisvuorokausiannoksella, plasman kortisoliaikakäyrän alla oleva pinta-ala pieneni hieman, mutta tilastollisesti merkitsevästi 24 tunnin aikana (AUC0-24h). ) terveillä aikuisilla vapaaehtoisilla.
Annosriippuvainen 24 tunnin virtsan kortisolin erittymisen estyminen havaittiin RHINOCORT AQUA (budesonidi) -nenäsumutteen antamisen jälkeen, jotka vaihtelivat 100-800 mikrogrammaa päivässä enintään neljän päivän ajan 78 terveellä aikuisella vapaaehtoisella. Näiden tulosten kliinistä merkitystä ei tunneta.
Farmakokinetiikka
Imeytyminen
Kun RHINOCORT AQUA (budesonidi) -nenäsumutetta (128 mikrog) on annettu intranasaalisesti, plasman keskimääräinen huippupitoisuus, noin 0,3 nmol/l, saavutetaan noin 0,5 tunnin kuluttua annoksesta. Verrattuna suonensisäiseen annokseen noin 34 % nenänsisäisestä annoksesta pääsee systeemiseen verenkiertoon, josta suurin osa imeytyy nenän limakalvon kautta. Vaikka budesonidi imeytyy hyvin ruoansulatuskanavasta, budesonidin oraalinen hyötyosuus on alhainen (n. 10 %) ensisijaisesti maksassa tapahtuvan laajan ensikierron metabolian vuoksi.
Jakelu
Budesonidin jakautumistilavuus oli noin 2-3 l/kg. Se sitoutui 85-90 % plasman proteiineihin. 22R-epimeerin jakautumistilavuus on lähes kaksi kertaa 22S-epimeerin jakautumistilavuus. Proteiinisitoutuminen oli vakio pitoisuusalueella (1-100 nmol/L), joka saavutettiin suositelluilla RHINOCORT 100 mikrogramman AQUA-nenäsumutteen annoksilla ja ylitti ne. Budesonidi sitoutui vain vähän tai ei lainkaan kortikosteroideja sitovaan globuliiniin. Budesonidi tasapainottui nopeasti punasolujen kanssa pitoisuudesta riippumattomalla tavalla veri/plasma-suhteen ollessa noin 0,8.
Aineenvaihdunta
Ihmisen maksahomogenaateilla tehdyt in vitro -tutkimukset ovat osoittaneet, että budesonidi metaboloituu nopeasti ja laajasti. Kaksi tärkeintä metaboliittia, jotka muodostuvat sytokromi P450:n (CYP) isoentsyymi 3A4 (CYP3A4) katalysoiman biotransformaation kautta, on eristetty ja tunnistettu 16α-hydroksiprednisoloniksi ja 6p-hydroksibudesonidiksi. Kummankin näiden kahden metaboliitin kortikosteroidiaktiivisuus on alle 1 % alkuperäisen yhdisteen aktiivisuudesta. In vitro ja in vivo -metaboliakuvioiden välillä ei ole havaittu laadullisia eroja. Ihmisen keuhko- ja seerumivalmisteissa havaittiin vähäistä metabolista inaktivaatiota.
Erittyminen/eliminaatio
Budesonidin 22R-muoto poistui ensisijaisesti maksasta systeemisellä puhdistumalla 1,4 l/min vs. 1,0 l/min 22S-muodolla. Terminaalinen puoliintumisaika, 2–3 tuntia, oli sama molemmilla epimeereillä ja riippumaton annoksesta. Budesonidi erittyi virtsaan ja ulosteisiin metaboliittien muodossa. Noin 2/3 intranasaalisesta radioleimatusta annoksesta löydettiin virtsasta ja loput ulosteista. Virtsassa ei havaittu muuttumatonta budesonidia.
Tietyt populaatiot
Geriatric
RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteen farmakokinetiikkaa iäkkäillä potilailla ei ole erityisesti tutkittu.
Pediatriset
RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteen antamisen jälkeen aika huippupitoisuuksien saavuttamiseen ja plasman puoliintumisaika olivat samanlaiset lapsilla ja aikuisilla. Lapsilla plasman pitoisuudet olivat noin kaksi kertaa suuremmat kuin aikuisilla, mikä johtui pääasiassa lasten ja aikuisten painoeroista.
Sukupuoli
Mitään erityistä farmakokineettistä tutkimusta ei ole tehty sukupuolen vaikutuksen arvioimiseksi budesonidin farmakokinetiikkaan. Kuitenkin, kun farmakokineettisessä tutkimuksessa annettiin 400 mikrogrammaa RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutetta 7 mies- ja 8 naispuoliselle vapaaehtoiselle, ei havaittu merkittäviä sukupuolten välisiä eroja farmakokineettisissä parametreissa.
Rotu
Ei ole tehty erityistä tutkimusta rodun vaikutuksen arvioimiseksi budesonidin farmakokinetiikkaan.
Imettävät äidit
Budesonidin jakautumista annettaessa suun kautta hengitettynä kuivajauheinhalaattorista annoksina 200 tai 400 mikrogrammaa kahdesti päivässä vähintään 3 kuukauden ajan tutkittiin kahdeksalla imettävällä naisella, joilla oli astma 1-6 kuukautta synnytyksen jälkeen. Näiden naisten systeeminen altistuminen budesonidille näyttää olevan verrattavissa muiden tutkimusten mukaan astmaa sairastaviin naisiin, jotka eivät imetä. Kahdeksan tunnin aikana annoksen jälkeen saatu rintamaito paljasti, että budesonidin maksimipitoisuus 400 ja 800 mikrogramman annoksilla oli vastaavasti 0,39 ja 0,78 nmol/l, ja se ilmaantui 45 minuutin kuluessa annostelusta. Arvioitu budesonidin oraalinen päivittäinen annos äidinmaidosta lapselle oli noin 0,007 ja 0,014 mikrog/kg/vrk kahdella tässä tutkimuksessa käytetyllä annostusohjelmalla, mikä on noin 0,3–1 % äidin hengittämästä annoksesta. Budesonidipitoisuudet plasmanäytteissä, jotka otettiin viideltä lapselta noin 90 minuuttia imetyksen jälkeen (ja noin 140 minuuttia lääkkeen antamisen jälkeen äidille), olivat kvantitatiivisen tason alapuolella ( Käyttö tietyissä väestöryhmissä, imettävät äidit ].
Munuaisten tai maksan vajaatoiminta
Budesonidin farmakokinetiikkaa ei ole tutkittu potilailla, joilla on munuaisten vajaatoiminta. Maksan vajaatoiminta voi vaikuttaa kortikosteroidien eliminaatioon. Budesonidin farmakokinetiikkaan vaikutti maksan toiminnan heikkeneminen, mikä on osoituksena systeemisen saatavuuden kaksinkertaistumisesta oraalisen nauttimisen jälkeen. Tämän löydön merkitystä intranasaalisesti annettavalle budesonidille ei ole osoitettu.
Huumeiden väliset vuorovaikutukset
Sytokromi P450 -entsyymien estäjät
Ketokonatsoli: Ketokonatsoli, joka on kortikosteroidien pääasiallisen metabolisen entsyymin sytokromi P450 (CYP) isoentsyymin 3A4 (CYP3A4) estäjä, nosti suun kautta nautitun budesonidin pitoisuutta plasmassa [ks. VAROITUKSET JA VAROTOIMET ja HUUMEIDEN VUOROVAIKUTUKSET ].
Simetidiini: Suositelluilla annoksilla simetidiinillä, CYP-entsyymien epäspesifisellä estäjällä, oli lievä mutta kliinisesti merkityksetön vaikutus suun kautta otettavan budesonidin farmakokinetiikkaan.
Eläinten toksikologia ja/tai farmakologia
Budesonidi oli teratogeeninen ja alkioita tappava kaneilla ja rotilla. Budesonidi aiheutti sikiön menetystä, alensi pentujen painoa ja luuston poikkeavuuksia kaniineilla annetulla annoksella 25 mcg/kg (noin 2 kertaa suurin suositeltu päivittäinen intranasaalinen annos aikuisilla mikrog/m2:n perusteella) ja ihonalaisella annoksella 500 mikrogrammaa /kg rotilla (noin 16 kertaa suurin suositeltu intranasaalinen päiväannos aikuisilla mikrogrammaa/m2:n perusteella). Rotilla ei havaittu teratogeenisia tai alkioita tappavia vaikutuksia, kun budesonidia annettiin inhalaatioannoksina aina 250 mcg/kg asti (noin 8 kertaa aikuisten suurin suositeltu intranasaalinen päiväannos mikrog/m2:n perusteella).
Kliiniset tutkimukset
RHINOCORT AQUA (budesonidi) -nenäsumutteen terapeuttista tehoa on arvioitu lumekontrolloiduissa kliinisissä tutkimuksissa kausiluonteisesta ja ympärivuotisesta allergisesta nuhasta, jotka kestivät 3–6 viikkoa.
Näissä tutkimuksissa budesonidilla hoidettujen potilaiden määrä oli 90 miestä ja 51 naista iältään 6–12-vuotiaita ja 691 miestä ja 694 12-vuotiasta ja sitä vanhempia naisia. Potilaat olivat pääosin valkoihoisia.
Kaiken kaikkiaan näiden kliinisten tutkimusten tulokset osoittivat, että kerran päivässä annettu RHINOCORT AQUA (budesonidi) -nenäsumute vähentää tilastollisesti merkitsevästi kausiluonteisen ja ympärivuotisen allergisen nuhan nenäoireiden vakavuutta, mukaan lukien vuotava nenä, aivastelu ja nenän tukkoisuus.
Nenäoireiden paranemista voidaan havaita potilailla 10 tunnin kuluessa siitä, kun RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutetta on käytetty ensimmäistä kertaa. Tätä alkamisaikaa tukee ympäristöaltistusyksikkötutkimus kausiluonteisen allergisen nuhan potilailla, joka osoitti, että RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumute paransi nenäoireita tilastollisesti merkitsevästi lumelääkkeeseen verrattuna 10 tunnilla. Lisätukea antaa monivuotisesta allergisesta nuhasta kärsivillä potilailla tehty kliininen tutkimus, joka osoitti tilastollisesti merkitsevää parannusta nenäoireissa sekä RHINOCORT AQUA (budesonidi) nenäsumuteella että aktiivisella vertailuaineella (mometasonifuroaatti) lumelääkkeeseen verrattuna 8 tunnilla. Alkua arvioitiin myös tässä tutkimuksessa nenän sisäänhengitysvirtauksen huippunopeudella, eikä tämä päätepiste osoittanut tehoa kummallekaan aktiiviselle hoidolle. Vaikka näissä tutkimuksissa havaittiin tilastollisesti merkitseviä parannuksia nenäoireissa lumelääkkeeseen verrattuna 8-10 tunnin sisällä, noin puolet tai kaksi kolmasosaa lopullisesta kliinisestä paranemisesta RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumuteella tapahtuu ensimmäisten 1-2 päivän aikana. ja suurin hyöty voidaan saavuttaa vasta noin 2 viikon kuluttua hoidon aloittamisesta.
VIITTEET
Kallen B, Rydhstroem H, Aberg A. Synnynnäiset epämuodostumat inhaloitavan budesonidin käytön jälkeen raskauden alkuvaiheessa. Obstet Gynecol 1999; 93:392-395.
2 Ericson A, Kallen B. Lääkkeiden käyttö raskauden aikana: ainutlaatuinen ruotsalainen rekisteröintimenetelmä, jota voidaan parantaa. Ruotsin lääkevirasto 1999; 1:8-11.
3 Norjavaara E, Gerhardsson de Verdier M. Normaalit raskauden tulokset väestöpohjaisessa tutkimuksessa, johon osallistui 2968 budesonidille altistunutta raskaana olevaa naista. J Allergy Clin Immunol 2003;! 11:736-742.
POTILASTIEDOT
RHINOCORT 100 mcg AQUA (budesonidi) ® (RINE-o-cort AH-kwa) (budesonidi) Nenäsumute
Vain nenässä käytettäväksi
Lue RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutteen mukana tulevat potilastiedot ennen kuin aloitat sen käytön ja aina, kun saat täyttöä. Saattaa tulla uutta tietoa. Nämä tiedot eivät korvaa terveydenhuollon tarjoajan kanssa puhumista terveydentilastasi tai hoidostasi. Jos sinulla on kysyttävää RHINOCORT AQUA (budesonidi) -nenäsumutteesta, kysy terveydenhuollon tarjoajalta tai apteekista.
Mikä on RHINOCORT 100mcg AQUA (budesonidi) nenäsumute?
RHINOCORT AQUA (budesonidi) nenäsumute on reseptilääke, jota käytetään kausittaisten ja ympärivuotisten allergiaoireiden hoitoon aikuisilla ja 6-vuotiailla ja sitä vanhemmilla lapsilla.
RHINOCORT AQUA -nenäsumute sisältää budesonidia, joka on ihmisen valmistama (synteettinen) kortikosteroidi. Nenänsisäiset kortikosteroidit ovat elimistössä olevia luonnollisia hormoneja, jotka vähentävät nenän limakalvon turvotusta. Kun ruiskutat RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutetta nenään, se auttaa vähentämään allergisen nuhan (nenän limakalvon tulehduksen) nenäoireita, kuten nenän tukkoisuutta, vuotavaa nenää, kutinaa ja aivastelua.
RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutteen turvallisuutta ja tehokkuutta ei ole osoitettu alle 6-vuotiailla lapsilla.
Kuka ei saa käyttää RHINOCORT AQUA (budesonidi) nenäsumutetta?
Älä käytä RHINOCORT 100mcg AQUA (budesonidi) nenäsumutetta:
- jos olet allerginen budesonidille tai jollekin RHINOCORT AQUA -nenäsumutteen aineosalle. Katso tämän pakkausselosteen lopusta täydellinen luettelo RHINOCORT AQUA (budesonidi) -nenäsumutteen aineosista.
Mitä minun pitäisi kertoa terveydenhuollon tarjoajalleni ennen RHINOCORT 100mcg AQUA (budesonidi) -nenäsuihkeen käyttöä?
Ennen kuin käytät RHINOCORT AQUA (budesonidi) -nenäsumutetta, kerro terveydenhuollon tarjoajalle tai apteekkihenkilökunnalle, jos:
- ovat viime aikoina olleet lähellä ketään, jolla on vesirokko tai tuhkarokko
- sinulla on maksaongelmia
- sinulla on hoitamattomia infektioita
- on koskaan ollut tuberkuloosi-niminen infektio
- sinulla on silmätulehdus
- sinulla on äskettäin ollut leikkaus tai nenävamma
- sinulla on muita sairauksia
- olet raskaana tai suunnittelet raskautta. Ei tiedetä, vahingoittaako RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsumutetta sikiötäsi. Keskustele lääkärisi kanssa, jos olet raskaana tai suunnittelet raskautta.
- imetät tai aiot imettää. RHINOCORT 100mcg AQUA (budesonidi) nenäsumute voi kulkeutua rintamaitoon. Keskustele lääkärisi kanssa parhaasta tavasta ruokkia vauvasi, jos käytät RHINOCORT AQUA (budesonidi) -nenäsumutetta.
Kerro terveydenhuollon tarjoajallesi kaikista käyttämistäsi lääkkeistä, mukaan lukien reseptilääkkeet ja ilman reseptiä saatavat lääkkeet, vitamiinit ja yrttilisät.
RHINOCORT AQUA (budesonidi) -nenäsumute voi vaikuttaa muiden lääkkeiden tehoon, ja muut lääkkeet voivat vaikuttaa RHINOCORT 100 mikrogrammaa AQUA (budesonidi) -nenäsuihkeen toimintaan.
Tunne käyttämäsi lääkkeet. Pidä luettelo lääkkeistäsi mukanasi, jotta voit näyttää terveydenhuollon tarjoajalle ja apteekkihenkilökunnalle, kun saat uuden lääkkeen.
Kuinka minun pitäisi käyttää RHINOCORT 100mcg AQUA (budesonidi) nenäsumutetta?
- RHINOCORT 100mcg AQUA (budesonidi) nenäsumute on tarkoitettu käytettäväksi vain nenässäsi. Älä suihkuta sitä silmiin tai suuhusi.
- Käytä RHINOCORT AQUA (budesonidi) -nenäsumutetta juuri niin kuin terveydenhuollon tarjoajasi neuvoo sinua käyttämään sitä.
- On erittäin tärkeää, että käytät RHINOCORT AQUA (budesonidi) nenäsumutetta säännöllisesti. Älä lopeta RHINOCORT AQUA (budesonidi) nenäsumutteen käyttöä tai muuta annostasi keskustelematta terveydenhuollon tarjoajan kanssa, vaikka tuntisit olosi paremmaksi.
- Keskustele terveydenhuollon tarjoajan kanssa, jos oireesi eivät parane, kun olet ottanut RHINOCORT AQUA (budesonidi) -nenäsumutetta 2 viikon ajan tai jos oireesi pahenevat.
- Aikuisen tulee auttaa pientä lasta käyttämään tätä lääkettä.
- Katso tämän pakkausselosteen lopussa olevat potilasohjeet saadaksesi täydelliset tiedot RHINOCORT AQUA (budesonidi) -nenäsumutteen käytöstä.
Mitkä ovat RHINOCORT AQUA (budesonidi) nenäsumutteen mahdolliset sivuvaikutukset?
RHINOCORT 100mcg AQUA (budesonidi) nenäsumute voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- reikä rustossa nenän sisällä (nenän väliseinän perforaatio). Kerro terveydenhuollon tarjoajallesi, jos nenästäsi kuuluu viheltävää ääntä hengittäessäsi.
- hidas haavan paraneminen. Älä käytä RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutetta ennen kuin nenäsi on parantunut, jos sinulla on haava nenässä, jos sinulle on tehty nenäleikkaus tai jos nenäsi on vaurioitunut.
- sieni-infektio nenässäsi.
- allergiset reaktiot. Kerro terveydenhuollon tarjoajallesi tai hakeudu välittömästi lääkärin hoitoon, jos sinulla on:
- ihottuma, punoitus tai turvotus
- vaikea kutina
- kasvojen, suun ja kielen turvotus
- immuunijärjestelmäongelmia, jotka voivat lisätä infektioriskiäsi. Saat todennäköisemmin infektioita, jos käytät lääkkeitä, jotka heikentävät elimistösi kykyä torjua infektioita. Vältä kosketusta ihmisten kanssa, joilla on tarttuvia sairauksia, kuten vesirokko tai tuhkarokko, kun käytät RHINOCORT AQUA (budesonide) -nenäsumutetta. Infektion oireita voivat olla kuume, kipu, kivut, vilunväristykset, väsymys, pahoinvointi ja oksentelu.
- lisämunuaisen vajaatoiminta, Lisämunuaisten vajaatoiminta on tila, jossa lisämunuaiset eivät tuota tarpeeksi steroidihormoneja. Lisämunuaisten vajaatoiminnan oireita voivat olla väsymys, heikkous, pahoinvointi, oksentelu ja alhainen verenpaine.
- hidastunut tai viivästynyt kasvu lapsilla. Lapsen kasvua tulee tarkistaa säännöllisesti, kun käytät RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutetta.
- silmäongelmat, kuten glaukooma ja kaihi. Kerro terveydenhuollon tarjoajallesi, jos sinulla on näkömuutos tai sinulla on ollut kohonnut silmänpaine, glaukooma ja/tai kaihi.
Soita terveydenhuollon tarjoajalle tai hakeudu heti lääkärin hoitoon, jos sinulla on oireita joistakin yllä luetelluista vakavista sivuvaikutuksista.
RHINOCORT 100mcg AQUA (budesonide) nenäsumutteen yleisimmät sivuvaikutukset ovat:
- nenästä vuotaa verta
- kipeä kurkku
- hengitysvaikeudet, kuten hengityksen vinkuminen tai rintakehän kiristys
- yskä
- nenäsi ärsytystä
Kerro terveydenhuollon tarjoajallesi, jos sinulla on sivuvaikutuksia, jotka häiritsevät sinua tai eivät katoa.
Nämä eivät ole kaikki RHINOCORT 100mcg AQUA (budesonidi) nenäsuihkeen mahdollisista sivuvaikutuksista. Lisätietoja saat terveydenhuollon tarjoajalta tai apteekista.
Soita terveydenhuollon tarjoajallesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle osoitteessa 1-800-FDA-1088 tai www.fda.gov/medwatch.
Voit ilmoittaa sivuvaikutuksista AstraZenecalle numerossa 1-800-236-9933.
Mitä minun pitäisi tietää allergisesta nuhasta?
"Nuha" tarkoittaa nenän limakalvon tulehdusta. Sitä kutsutaan joskus "heinänuhaksi". Allerginen nuha voi johtua allergioista siitepölylle, eläinten hilseelle, pölypunkille ja homeitiöille. Jos sinulla on allerginen nuha, nenästäsi tulee tukkoinen, vuotava ja kutiava. Saatat myös aivastaa paljon. Sinulla voi olla punaisia, kutiavia ja vetisiä silmiä; kutiava kurkku; tai tukkeutuneet, kutisevat korvat.
RHINOCORT AQUA (budesonidi) -nenäsumute auttaa lievittämään nenän oireita.
Jos sinulla on myös kutisevia, vetisiä silmiä, kerro siitä terveydenhuollon tarjoajallesi. Hän voi määrätä lisälääkkeitä näiden oireiden hoitoon.
Kuinka minun pitäisi säilyttää RHINOCORT AQUA (budesonidi) nenäsumutetta?
- Säilytä RHINOCORT AQUA (budesonidi) nenäsumutetta 68 ° F - 77 ° F (20 ° C - 25 ° C) lämpötilassa.
- Älä jäädytä RHINOCORT AQUA (budesonidi) -nenäsumutetta.
- Suojaa RHINOCORT 100mcg AQUA (budesonidi) nenäsumutetta valolta.
- Älä käytä RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutetta sen jälkeen, kun merkitty määrä suihkeita on käytetty (ei sisällä pohjustusta) tai pakkauksessa tai pullon etiketissä olevan viimeisen käyttöpäivämäärän jälkeen.
- Pidä vihreä suojakorkki RHINOCORT AQUA (budesonidi) -nenäsumutteessa, kun sitä ei käytetä. (Ole hyvä ja katso Ennen käyttöä kääntöpuolella ).
- Pidä RHINOCORT 100mcg AQUA (budesonidi) nenäsumute ja kaikki lääkkeet poissa lasten ulottuvilta.
Yleistä tietoa RHINOCORT AQUA (budesonidi) nenäsumutteen turvallisesta ja tehokkaasta käytöstä:
Älä käytä RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutetta sairauteen, johon sitä ei ole määrätty. Älä anna RHINOCORT AQUA (budesonidi) -nenäsumutetta muille ihmisille, vaikka heillä olisi samat oireet kuin sinulla. Se voi vahingoittaa heitä.
Tämä potilastietolehtinen sisältää yhteenvedon tärkeimmistä tiedoista RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutteesta. Jos haluat lisätietoja, keskustele terveydenhuollon tarjoajasi kanssa. Voit kysyä apteekista tai terveydenhuollon tarjoajalta tietoja RHINOCORT 100mcg AQUA (budesonide) -nenäsumutteesta, joka on kirjoitettu terveydenhuollon ammattilaisille.
Lisätietoja saat osoitteesta www.astrazeneca-us.com tai soittamalla AstraZenecalle numeroon 1-800-236-9933.
Mitkä ovat RHINOCORT AQUA (budesonidi) nenäsumutteen ainesosat?
Aktiivinen ainesosa: budesonidi
Inaktiiviset ainesosat: Mikrokiteinen selluloosa ja karboksimetyyliselluloosanatrium, vedetön dekstroosi, polysorbaatti 80, dinatriumedetaatti, kaliumsorbaatti ja puhdistettu vesi sekä kloorivetyhappo.
Potilasohjeet
Vain nenässä käytettäväksi. Älä suihkuta silmiin tai suuhun.
Lue potilasohjeet huolellisesti ennen kuin alat käyttää RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutetta. Jos sinulla on kysyttävää, kysy terveydenhuollon tarjoajaltasi
Kuva A 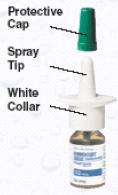
RHINOCORT AQUA (budesonidi) -nenäsuihkeen pohjustus
Ennen kuin käytät RHINOCORT AQUA (budesonidi) -nenäsumutetta, pullo on esivalmistettava. RHINOCORT 100mcg AQUA (budesonidi) nenäsuihkeen pohjustus:
1. Vedä poistaaksesi nenäsumuteyksikön vihreän suojakorkin.
2. Ravista pulloa kevyesti muutaman sekunnin ajan ennen jokaista käyttöä.
3. Pidä pulloa tukevasti kiinni kuvan B mukaisesti siten, että etu- ja keskisormesi ovat suihkekärjen kummallakin puolella ja peukalo pullon alla.
Kuva B 
4. Aktivoi pumppu painamalla nopeasti ja lujasti valkoista kaulusta samalla, kun pidät pullon pohjasta peukalollasi.
5. Ennen kuin käytät RHINOCORT AQUA (budesonidi) -nenäsumutetta ensimmäistä kertaa, ravista pulloa kevyesti. Pumppu tulee esitellä painamalla valkoista kaulusta 8 kertaa. Pumppu on nyt käyttövalmis. Päivittäin käytettäessä pumppua ei tarvitse täyttää uudelleen. Jos et käytä 2 päivää peräkkäin, pohjusta uudelleen 1 suihkeella tai kunnes hienojakoinen suihke ilmestyy. Jos sitä ei ole käytetty yli 14 päivään, huuhtele pumpun suihkekärki tämän pakkausselosteen lopussa lueteltujen puhdistusvaiheiden mukaisesti. Käsittele uudelleen puhdistuksen jälkeen kahdella suihkeella tai kunnes hienojakoinen suihke ilmestyy.
Jokainen RHINOCORT AQUA (budesonidi) -nenäsumutepullo sisältää tarpeeksi lääkettä, jotta voit ruiskuttaa lääkettä pullosta 120 kertaa pullon esikäsittelyn jälkeen.
Älä käytä RHINOCORT 100 mcg AQUA (budesonidi) -nenäsumutteen pulloa 120 suihkeen jälkeen. Lisäsuihkeet 120:n jälkeen eivät välttämättä sisällä oikeaa määrää lääkettä. Sinun tulee pitää kirjaa kustakin RHINOCORT 100mcg AQUA -nenäsumutepullosta käyttämiesi suihkeiden määrästä ja hävittää kaikki pulloon mahdollisesti jääneet lääkkeet. Täytä reseptisi kuukausittain.
Kuinka käyttää RHINOCORT 100mcg AQUA (budesonidi) -nenäsumutetta
Noudata näitä ohjeita RHINOCORT AQUA (budesonidi) nenäsumutteen päivittäisessä käytössä:
Kuva C 
4. Työnnä suihkekärki sieraimeen (kärki ei saa ulottua kauas nenään). Sulje toinen sieraimesi sormella ja kallista päätäsi hieman eteenpäin, jotta suihke suuntautuu nenäsi takaosaan (katso Kuva D ).
Kuva D 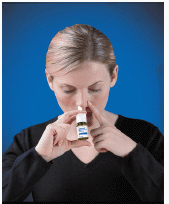
5. Aktivoi pumppu jokaisella suihkeella nopeasti ja lujasti painamalla valkoista kaulusta samalla kun pidät pullon pohjasta peukalollasi. Hengitä kevyesti sisäänpäin sieraimen kautta.
6. Kun olet ruiskuttanut sieraimeen, kallista päätäsi taaksepäin muutaman sekunnin ajan (katso Kuva E ).
Kuva E 
7. Jos tarvitaan toinen suihke samaan sieraimeen, toista vaiheet 3–6.
8. Toista vaiheet 3–7 toiselle sieraimellesi.
9. Vältä nenän puhaltamista 15 minuutin ajan RHINOCORT 100mcg AQUA (budesonide) -nenäsumutteen käytön jälkeen.
10. Pyyhi ruiskun kärki puhtaalla liinalla (katso Kuva F ) ja aseta vihreä suojakorkki paikalleen. Säilytä pullo pystyasennossa.
Kuva F 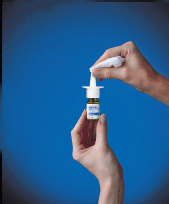
Kuinka puhdistaa RHINOCORT 100mcg AQUA (budesonidi) nenäsuihke
Kuva G 
Huuhtele vihreä suojakorkki ja suihkusuutin säännöllisesti. Tehdä tämä:
Lisätietoja RHINOCORT 100mcg AQUA (budesonide) ® -nenäsumutteesta saat soittamalla AstraZenecan tiedotuskeskukseen maanantaista perjantaihin klo 8–18 ET, lukuun ottamatta pyhäpäiviä klo. 1-800-236-9933.
