Micronase 2.5mg, 5mg Glyburide Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mikä Micronase on ja miten sitä käytetään?
Micronase (glyburide) -tabletit on reseptilääke, jota käytetään tyypin 2 diabeteksen oireiden hoitoon. Micronasea voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Mikronaasi kuuluu lääkkeiden luokkaan, jota kutsutaan diabeteslääkkeiksi, sulfonyyliureoiksi.
Ei tiedetä, onko Micronase turvallinen ja tehokas lapsille.
Mitkä ovat Micronasen mahdolliset sivuvaikutukset?
Micronase 5 mg voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- nokkosihottuma,
- vaikeuksia hengittää,
- kasvojen, huulten, kielen tai kurkun turvotus,
- kuume,
- kipeä kurkku,
- polttaa silmissäsi,
- ihokipu,
- punainen tai violetti ihottuma, joka leviää ja aiheuttaa rakkuloita ja hilseilyä,
- tumma virtsa,
- ihon tai silmien keltaisuus (keltatauti),
- vaikea ihottuma,
- punoitus,
- kutina,
- kalpea iho,
- helppo mustelma,
- epätavallinen verenvuoto,
- vilunväristykset,
- kipeä kurkku,
- suun haavaumat,
- päänsärky,
- hämmennystä,
- sammaltava puhe,
- vakava heikkous,
- oksentelua,
- koordinaation menetys ja
- epävakaa olo
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Micronasen yleisimmät sivuvaikutukset ovat:
- matala verensokeri,
- pahoinvointi,
- närästys,
- täynnä olo,
- lihas- tai nivelkipu,
- näön hämärtyminen,
- lievä ihottuma ja
- ihon punoitus
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Micronasen mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
MICRONASE 2,5 mg -tabletit sisältävät glyburidia, joka on oraalinen verensokeria alentava sulfonyyliurea-luokan lääke. Glyburidi on valkoinen, kiteinen yhdiste, joka on formuloitu MICRONASE-tableteiksi, joiden vahvuudet ovat 1,25, 2,5 ja 5 mg oraalista antoa varten. Ei-aktiiviset aineet: kolloidinen piidioksidi, kaksiemäksinen kalsiumfosfaatti, magnesiumstearaatti, mikrokiteinen selluloosa, natriumalginaatti, talkki. Lisäksi 2,5 mg sisältää alumiinioksidia ja FD&C Red No. 40 ja 5 mg sisältää alumiinioksidia ja FD&C Blue No. 1:tä. Glyburidin kemiallinen nimi on 1-[[p-[2-(5-kloori-o-anisamido)-etyyli]fenyyli]-sulfonyyli]-3-sykloheksyyliurea ja molekyylipaino on 493,99. Rakennekaava on esitetty alla.
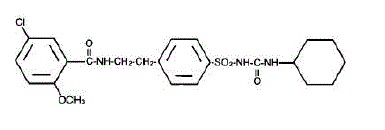
INDIKAATIOT
MICRONASE 2,5 mg on tarkoitettu tyypin 2 diabetes mellitusta sairastavien aikuisten glukoositasapainon parantamiseen ruokavalion ja liikunnan lisänä.
ANNOSTELU JA HALLINNOINTI
Diabetes mellituksen hoitoon MICRONASE-tableteilla ei ole kiinteää annostusohjelmaa. Virtsan glukoosin tavanomaisen seurannan lisäksi potilaan verensokeria on seurattava määräajoin, jotta voidaan määrittää potilaalle pienin tehokas annos. primaarisen epäonnistumisen havaitsemiseksi, eli riittämättömän verensokerin alenemisen suurimmalla suositellulla lääkeannoksella; ja havaita sekundaarinen epäonnistuminen, eli riittävän verensokeria alentavan vasteen menetys ensimmäisen tehojakson jälkeen. Glykosyloituneen hemoglobiinin tasot voivat myös olla arvokkaita potilaan hoitovasteen seurannassa.
Lyhytaikainen MICRONASE 5 mg:n antaminen voi olla riittävä jaksojen aikana, jolloin hallinta on menetetty ohimenevästi, jos potilas pysyy hallinnassa hyvin ruokavaliolla.
Tavallinen aloitusannos
MICRONASE 5 mg -tablettien tavallinen aloitusannos on 2,5–5 mg vuorokaudessa aamiaisen tai ensimmäisen pääaterian yhteydessä. Potilaille, jotka saattavat olla herkempiä hypoglykeemisille lääkkeille, aloitusannos on 1,25 mg päivässä. (Katso VAROTOIMENPITEET kohta potilaille, joilla on lisääntynyt riski.) Asianmukaisen annostusohjelman noudattamatta jättäminen voi aiheuttaa hypoglykemiaa. Potilaat, jotka eivät noudata heille määrättyä ruokavaliota ja lääkehoitoa, ovat alttiimpia saamaan epätyydyttävän vasteen hoitoon.
Siirto muista hypoglykeemisistä terapiapotilaista, jotka saavat muuta suun kautta annettavaa diabeteslääkehoitoa
Potilaiden siirtyminen muista suun kautta otetuista diabeteslääkkeistä MICRONASE-hoitoon tulee tehdä konservatiivisesti ja aloitusvuorokausiannoksen tulee olla 2,5–5 mg. Siirrettäessä potilaita muista suun kautta otetuista hypoglykeemisistä aineista kuin klooripropamidista MICRONASE 2,5 mg:aan, siirtymäaikaa ei tarvita eikä aloitus- tai esiannosta tarvita. Potilaita siirrettäessä klooripropamidista on noudatettava erityistä varovaisuutta kahden ensimmäisen viikon aikana, koska klooripropamidin pitkittynyt pysyminen kehossa ja myöhemmät päällekkäiset lääkevaikutukset voivat aiheuttaa hypoglykemian.
Potilaat, jotka saavat insuliinia
Jotkut tyypin II diabeetikoista, joita hoidetaan insuliinilla, voivat reagoida tyydyttävästi MICRONASE-hoitoon. Jos insuliiniannos on alle 20 yksikköä vuorokaudessa, voidaan yrittää korvata MICRONASE 2,5 mg -tabletit 2,5–5 mg kerta-annoksena. Jos insuliiniannos on 20–40 yksikköä vuorokaudessa, potilas voidaan asettaa suoraan MICRONASE 2,5 mg -tablettien 5 mg vuorokaudessa kerta-annoksena. Jos insuliiniannos on yli 40 yksikköä vuorokaudessa, MICRONASE-hoitoon siirtyminen edellyttää siirtymäaikaa. Näillä potilailla insuliiniannosta pienennetään 50 % ja MICRONASE 5 mg tabletit 5 mg päivässä aloitetaan. Katso lisätietoja kohdasta Titraus ylläpitoannokseen.
Potilaat, jotka saavat kolesevelaamia
Kun kolesevelaamia annetaan samanaikaisesti glyburidin kanssa, plasman maksimipitoisuus ja kokonaisaltistus glyburidille vähenevät. Siksi MICRONASE tulee antaa vähintään 4 tuntia ennen kolesevelaamia.
Titraus ylläpitoannokseen
Tavallinen ylläpitoannos on 1,25-20 mg vuorokaudessa, joka voidaan antaa yhtenä annoksena tai jaettuina annoksina (ks. Annosteluväli jakso). Annosta tulee suurentaa enintään 2,5 mg:n välein viikoittain potilaan verensokerivasteen perusteella.
MICRONASE 5 mg:n ja muiden oraalisten hypoglykeemisten aineiden välillä ei ole tarkkaa annossuhdetta. Vaikka potilaat voidaan siirtää muiden sulfonyyliureoiden enimmäisannoksesta, MICRONASE 2,5 mg -tablettien enimmäisaloitusannosta on noudatettava. Ylläpitoannos 5 mg MICRONASE 2,5 mg -tabletteja varmistaa suunnilleen saman verran verensokerin hallintaa kuin 250 - 375 mg klooripropamidia, 250 - 375 mg tolatsamidia, 500 - 750 mg asetoheksamidia tai 1 000 - 1500 mg tolbutamidia.
Siirrettäessä potilaita, jotka saavat yli 40 yksikköä insuliinia vuorokaudessa, heidän hoitonsa voidaan aloittaa 5 mg:n MICRONASE-tablettien päivittäisellä annoksella samanaikaisesti, kun insuliiniannosta pienennetään 50 %. Insuliinin asteittainen lopettaminen ja MICRONASE-arvon nostaminen 1,25–2,5 mg:lla 2–10 päivän välein suoritetaan sitten. Tämän muuntojakson aikana, kun käytetään sekä insuliinia että MICRONASEa, voi esiintyä hypoglykemiaa. Insuliinin poistamisen aikana potilaiden tulee testata virtsaan glukoosi- ja asetonipitoisuus vähintään kolme kertaa päivässä ja raportoida tuloksista lääkärilleen. Jatkuva asetonuria ja glykosuria osoittavat, että potilas on tyypin I diabeetikko, joka tarvitsee insuliinihoitoa.
Samanaikainen MICRONASE 5 mg ja metformiinihoito
MICRONASE-tabletit tulee lisätä vähitellen niiden potilaiden annostusohjelmaan, jotka eivät ole reagoineet metformiinimonoterapian enimmäisannokseen neljän viikon kuluttua (ks. Tavallinen aloitusannos ja ylläpitoannoksen titraus). Katso metformiinin pakkausseloste.
Samanaikaisella glyburidi- ja metformiinihoidolla haluttu verensokerin hallinta voidaan saavuttaa säätämällä kunkin lääkkeen annosta. Jokaisen lääkkeen optimaalinen annos tulisi kuitenkin yrittää tunnistaa tämän tavoitteen saavuttamiseksi. Glyburidin ja metformiinin samanaikainen käyttö sulfonyyliureahoitoon liittyvän hypoglykemian riski jatkuu ja saattaa lisääntyä. Asianmukaisiin varotoimiin on ryhdyttävä (katso VAROTOIMENPITEET ).
Suurin annos
Yli 20 mg:n päivittäisiä annoksia ei suositella.
Annosteluväli
Kerran päivässä annettava hoito on yleensä tyydyttävää. Joillakin potilailla, erityisesti yli 10 mg vuorokaudessa saavilla potilailla, voi olla tyydyttävämpi vaste kahdesti vuorokaudessa annettavalla annoksella.
Tietyt potilasryhmät
MICRONASEa ei suositella käytettäväksi raskauden aikana tai lapsille.
Iäkkäillä potilailla, heikentyneellä tai aliravituilla potilailla sekä potilailla, joilla on munuaisten tai maksan vajaatoiminta, aloitus- ja ylläpitoannostuksen tulee olla konservatiivisia hypoglykeemisten reaktioiden välttämiseksi. (Katso VAROTOIMENPITEET .)
MITEN TOIMITETAAN
MICRONASE Tabletit toimitetaan seuraavasti:
MICRONASE 5 mg tabletit 1,25 mg (Valkoinen, pyöreä, pisteytetty, painettu MICRONASE 1.25)
Pullot 100 NDC 0009-0131-01
MICRONASE Tabletit 2,5 mg (Tummanpunainen, pyöreä, pisteytetty, painettu MICRONASE 2.5)
Pullot 100 NDC 0009-0141-01 1000 pullot NDC 0009-0141-03 Yksikköannos Pkg 100 NDC 0009-0141-02
MICRONASE 2,5 mg Tabletit 5 mg (Sininen, pyöreä, uurrettu painettu MICRONASE 5)
Pullot 30 NDC 0009-0171-11 60 pulloa NDC 0009-0171-12 100 pulloa NDC 0009-0171-05 500 pullot NDC 0009-0171-06 1000 pullot NDC 0009-0171-07 Yksikköannos Pkg 100 NDC 0009-0171-03
Säilytä kontrolloidussa huoneenlämmössä 20–25 °C (68–77 °F) [katso USP]. Annosteltu hyvin suljetuissa säiliöissä, joissa on turvasulkimet. Pidä säiliö tiiviisti suljettuna.
Jakelija: Pfizer, Pharmacia ja Upjohn, pfizer Inc:n osasto, NY 10017. Tarkistettu: heinäkuu 2016.
SIVUVAIKUTUKSET
Hypoglykemia
Katso VAROTOIMENPITEET ja YLIANNOSTUS Osat.
Ruoansulatuskanavan reaktiot
Kolestaattista keltaisuutta ja hepatiittia voi esiintyä harvoin, mikä voi edetä maksan vajaatoiminnaksi; MICRONASE 2,5 mg -tablettien käyttö tulee lopettaa, jos näin tapahtuu.
Maksan toiminnan poikkeavuuksia, mukaan lukien yksittäisiä transaminaasitason nousuja, on raportoitu.
Ruoansulatuskanavan häiriöt, kuten pahoinvointi, ylävatsan täyteläisyys ja närästys, ovat yleisimmät reaktiot, joita esiintyi kliinisten tutkimusten aikana 1,8 %:lla hoidetuista potilaista. Ne ovat yleensä annoksesta riippuvia ja voivat hävitä, kun annosta pienennetään.
Dermatologiset reaktiot
Allergisia ihoreaktioita, kuten kutinaa, punoitusta, urtikariaa ja morbilliformisia tai makulopapulaarisia ihottumia, esiintyi kliinisissä tutkimuksissa 1,5 %:lla hoidetuista potilaista. Nämä voivat olla ohimeneviä ja hävitä huolimatta MICRONASEn jatkuvasta käytöstä; jos ihoreaktiot jatkuvat, lääke on lopetettava.
Porphyria cutanea tardaa ja valoherkkyysreaktioita on raportoitu sulfonyyliureoiden käytön yhteydessä.
Hematologiset reaktiot
Leukopenia, agranulosytoosi, trombosytopenia, hemolyyttinen anemia (ks. VAROTOIMENPITEET ), aplastista anemiaa ja pansytopeniaa on raportoitu sulfonyyliureoiden käytön yhteydessä.

Metaboliset reaktiot
Maksan porfyriaa ja disulfiraamin kaltaisia reaktioita on raportoitu sulfonyyliureoiden käytön yhteydessä; Maksaporfyriaa ei kuitenkaan ole raportoitu MICRONASE-hoidon yhteydessä, ja disulfiraamin kaltaisia reaktioita on raportoitu hyvin harvoin.
Hyponatremiatapauksia on raportoitu glyburidin ja kaikkien muiden sulfonyyliureoiden yhteydessä, useimmiten potilailla, jotka käyttävät muita lääkkeitä tai joilla on sairaus, jonka tiedetään aiheuttavan hyponatremiaa tai lisäävän antidiureettisen hormonin vapautumista. Epäasianmukaisen antidiureettisen hormonin (SIADH) erityksen oireyhtymää on raportoitu tiettyjen muiden sulfonyyliureoiden yhteydessä, ja on ehdotettu, että nämä sulfonyyliureat voivat lisätä ADH:n perifeeristä (antidiureettista) vaikutusta ja/tai lisätä ADH:n vapautumista.
Muut reaktiot
Muutoksia akkomodaatiossa ja/tai näön hämärtymistä on raportoitu glyburidin ja muiden sulfonyyliureoiden käytön yhteydessä. Näiden uskotaan liittyvän glukoositasojen vaihteluun.
Dermatologisten reaktioiden lisäksi on raportoitu allergisia reaktioita, kuten angioedeemaa, nivelkipua, lihaskipua ja vaskuliittia.
HUUMEIDEN VUOROVAIKUTUKSET
Sulfonyyliureoiden hypoglykeemistä vaikutusta voivat tehostaa tietyt lääkkeet, mukaan lukien ei-steroidiset tulehduskipulääkkeet ja muut voimakkaasti proteiineihin sitoutuvat lääkkeet, salisylaatit, sulfonamidit, kloramfenikoli, probenesidi, kumariinit, monoamiinioksidaasin estäjät ja beeta-adrenergiset salpaajat. Kun tällaisia lääkkeitä annetaan potilaalle, joka saa MICRONASE 5 mg, potilasta on tarkkailtava huolellisesti hypoglykemian varalta. Kun tällaiset lääkkeet poistetaan potilaalta, joka saa MICRONASE 5 mg, potilasta on tarkkailtava tarkasti hallinnan menettämisen varalta.
Maksaentsyymien nousun riski havaittiin potilailla, jotka saivat glyburidia samanaikaisesti bosentaanin kanssa. Siksi MICRONASE-valmisteen ja bosentaanin samanaikainen anto on vasta-aiheista.
Tietyt lääkkeet aiheuttavat yleensä hyperglykemiaa ja voivat johtaa hallinnan menettämiseen. Näitä lääkkeitä ovat tiatsidit ja muut diureetit, kortikosteroidit, fenotiatsiinit, kilpirauhasvalmisteet, estrogeenit, oraaliset ehkäisyvalmisteet, fenytoiini, nikotiinihappo, sympatomimeetit, kalsiumkanavaa salpaavat lääkkeet ja isoniatsidi. Kun tällaisia lääkkeitä annetaan MICRONASE-hoitoa saavalle potilaalle, potilasta on tarkkailtava tarkasti hallinnan menettämisen varalta. Kun tällaiset lääkkeet poistetaan MICRONASEa saavalta potilaalta, potilasta tulee tarkkailla huolellisesti hypoglykemian varalta.
Glyburidin ja siprofloksasiinin, fluorokinoloniantibiootin, välillä on raportoitu mahdollista yhteisvaikutusta, mikä voimistaa glyburidin hypoglykeemistä vaikutusta. Tämän yhteisvaikutuksen mekanismia ei tunneta.
Suun kautta otettavan mikonatsolin ja oraalisten hypoglykeemisten aineiden välillä on raportoitu mahdollista yhteisvaikutusta, joka johtaa vakavaan hypoglykemiaan. Ei tiedetä, esiintyykö tätä yhteisvaikutusta myös suonensisäisten, paikallisesti tai emättimeen annettavien mikonatsolivalmisteiden kanssa.
VAROITUKSET
Oraalisten hypoglykeemisten lääkkeiden antamisen on raportoitu liittyvän lisääntyneeseen kardiovaskulaariseen kuolleisuuteen verrattuna hoitoon pelkällä ruokavaliolla tai ruokavaliolla ja insuliinilla. Tämä varoitus perustuu University Group Diabetes Programin (UGDP) tutkimukseen, joka on pitkäaikainen prospektiivinen kliininen tutkimus, jonka tarkoituksena on arvioida glukoosia alentavien lääkkeiden tehokkuutta verisuonikomplikaatioiden ehkäisyssä tai viivästyksessä potilailla, joilla on insuliinista riippumaton diabetes. . Tutkimukseen osallistui 823 potilasta, jotka jaettiin satunnaisesti yhteen neljästä hoitoryhmästä
UGDP raportoi, että potilailla, joita hoidettiin 5–8 vuoden ajan ruokavaliolla ja kiinteällä tolbutamidiannoksella (1,5 grammaa päivässä), kardiovaskulaarinen kuolleisuusaste oli noin 2½ kertaa suurempi kuin pelkällä ruokavaliolla hoidetuilla potilailla. Merkittävää lisääntymistä kokonaiskuolleisuudessa ei havaittu, mutta tolbutamidin käyttö lopetettiin sydän- ja verisuoniperäisen kuolleisuuden lisääntymisen vuoksi, mikä rajoitti tutkimuksen mahdollisuutta osoittaa kokonaiskuolleisuuden lisääntyminen. Huolimatta näiden tulosten tulkintaa koskevasta kiistasta, UGDP-tutkimuksen tulokset tarjoavat riittävän perustan tälle varoitukselle. Potilaalle tulee kertoa MICRONASE 5 mg:n mahdollisista riskeistä ja eduista sekä vaihtoehtoisista hoitomuodoista.
Vaikka tähän tutkimukseen sisältyi vain yksi sulfonyyliurea-luokan lääke (tolbutamidi), on turvallisuuden kannalta järkevää ottaa huomioon, että tämä varoitus voi koskea myös muita tämän luokan suun kautta otettavia hypoglykeemisiä lääkkeitä, koska ne ovat samankaltaisia. toiminta ja kemiallinen rakenne.
VAROTOIMENPITEET
Kenraali
Makrovaskulaariset tulokset
Ei ole tehty kliinisiä tutkimuksia, jotka osoittaisivat lopullista näyttöä makrovaskulaarisen riskin vähentämisestä MICRONASElla tai muilla diabeteslääkkeillä.
Hypoglykemia
Kaikki sulfonyyliureat, mukaan lukien MICRONASE 2,5 mg, voivat aiheuttaa vaikean hypoglykemian. Oikea potilaan valinta, annostus ja ohjeet ovat tärkeitä hypoglykeemisten jaksojen välttämiseksi. Munuaisten tai maksan vajaatoiminta voi aiheuttaa kohonneita glyburidin lääkepitoisuuksia, ja jälkimmäinen voi myös heikentää glukoneogeenistä kapasiteettia, mikä molemmat lisää vakavien hypoglykeemisten reaktioiden riskiä. Iäkkäät, heikentyneet tai aliravitut potilaat sekä lisämunuaisen tai aivolisäkkeen vajaatoimintaa sairastavat potilaat ovat erityisen herkkiä glukoosia alentavien lääkkeiden hypoglykeemiselle vaikutukselle. Hypoglykemiaa voi olla vaikea tunnistaa vanhuksilla ja ihmisillä, jotka käyttävät beetasalpaavia lääkkeitä. Hypoglykemiaa esiintyy todennäköisemmin, kun kalorien saanti on puutteellista, raskaan tai pitkäaikaisen harjoituksen jälkeen, kun alkoholia nautitaan tai kun käytetään useampaa kuin yhtä glukoosia alentavaa lääkettä. Hypoglykemian riski voi lisääntyä yhdistelmähoidolla.
Verensokerin hallinnan menetys
Kun potilas, joka on vakiintunut jollakin diabeettisella hoito-ohjelmalla, altistuu stressille, kuten kuumeelle, traumalle, infektiolle tai leikkaukselle, hallinta voi menettää. Tällaisina aikoina voi olla tarpeen keskeyttää MICRONASE 2,5 mg -valmisteen käyttö ja antaa insuliinia.
Minkä tahansa hypoglykeemisen lääkkeen, mukaan lukien MICRONASE 5 mg, tehokkuus verensokerin alentamisessa halutulle tasolle heikkenee monilla potilailla tietyn ajan kuluessa, mikä voi johtua diabeteksen vaikeusasteesta tai heikentyneestä vasteesta lääkkeelle. Tätä ilmiötä kutsutaan toissijaiseksi epäonnistumiseksi, jotta se voidaan erottaa primaarisesta epäonnistumisesta, jossa lääke on tehoton yksittäisellä potilaalla, kun MICRONASE 5 mg annetaan ensimmäisen kerran. Annoksen riittävä säätö ja ruokavalion noudattaminen tulee arvioida ennen kuin potilas luokitellaan toissijaiseksi vajaatoiminnaksi.
Hemolyyttinen anemia
Potilaiden, joilla on glukoosi-6-fosfaattidehydrogenaasin (G6PD) puutos, hoito sulfonyyliurea-aineilla voi johtaa hemolyyttiseen anemiaan. Koska MICRONASE 5 mg b kuuluu sulfonyyliurealääkkeiden luokkaan, varovaisuutta on noudatettava potilailla, joilla on G6PD-puutos, ja harkittava vaihtoehtoa, joka ei ole sulfonyyliurea. Markkinoille tulon jälkeisissä raporteissa hemolyyttistä anemiaa on raportoitu myös potilailla, joilla ei ollut tiedossa G6PD:n puutetta.
Lääkärin neuvontatietoja potilaille
Tyypin 2 diabeteksen hoitoa aloitettaessa tulee painottaa ruokavaliota ensisijaisena hoitomuotona. Kalorirajoitus ja painonpudotus ovat tärkeitä lihaville diabeetikoille. Pelkästään asianmukainen ruokavalion hallinta voi olla tehokas verensokerin ja hyperglykemian oireiden hallinnassa. Säännöllisen liikunnan tärkeyttä tulee myös korostaa, sydän- ja verisuonisairauksien riskitekijät tulee tunnistaa ja korjaavia toimia mahdollisuuksien mukaan. Sekä lääkärin että potilaan tulee nähdä MICRONASE tai muiden diabeteslääkkeiden käyttö ruokavalion lisäksi hoitona, ei korvauksena tai kätevänä mekanismina ruokavalion rajoittamisen välttämiseksi. Lisäksi verensokerin hallinnan menetys pelkällä ruokavaliolla voi olla ohimenevää, mikä edellyttää vain lyhytaikaista MICRONASE- tai muiden diabeteslääkkeiden antamista. MICRONASE 2,5 mg:n tai muiden diabeteslääkkeiden käytön jatkamisen tai lopettamisen tulee perustua kliiniseen harkintaan käyttämällä säännöllisiä kliinisiä ja laboratoriotutkimuksia.
Laboratoriotestit
MICRONASE 5 mg -tablettien terapeuttista vastetta tulee seurata säännöllisillä virtsan glukoosimittauksilla ja säännöllisillä verensokerimittauksilla. Glykosyloituneen hemoglobiinin mittaamisesta voi olla apua joillekin potilaille.
Metformiini
NIDDM-potilailla tehdyssä kerta-annoksen yhteisvaikutustutkimuksessa havaittiin glyburidin AUC- ja Cmax-arvojen laskua, mutta ne vaihtelivat suuresti. Tämän tutkimuksen kerta-annosluonne ja korrelaation puute veren glyburiditasojen ja farmakodynaamisten vaikutusten välillä tekee tämän vuorovaikutuksen kliinisestä merkityksestä epävarman. Glyburidin ja metformiinin samanaikainen anto ei aiheuttanut muutoksia metformiinin farmakokinetiikkaan tai farmakodynamiikkaan.
Colesevelam
Kolesevelamin ja glyburidin samanaikainen anto pienensi glyburidin AUC-arvoa 32 % ja Cmax 47 %. Glyburidin AUC:n ja Cmax:n pieneneminen oli 20 % ja Cmax 15 %, kun se annettiin 1 tunti ennen, eivätkä ne muuttuneet merkitsevästi (-7 % ja vastaavasti 4 %), kun se annettiin 4 tuntia ennen kolesevelaamia.
Topiramaatti
Tyypin 2 diabetespotilailla tehdyssä lääkkeiden yhteisvaikutustutkimuksessa arvioitiin glyburidin (5 mg/vrk) vakaan tilan farmakokinetiikka yksinään ja samanaikaisesti topiramaatin (150 mg/vrk) kanssa. Glyburidin C-arvo laski 22 % ja AUC 25 % topiramaatin annon aikana. Aktiivisten metaboliittien 4-trans-hydroksiglyburidin (M1) ja 3-cis-hydroksiglyburidin (M2) systeeminen altistuminen (AUC) väheni myös 13 % ja 15 % ja C-pitoisuus 18 % ja 25 %. , vastaavasti. Glyburidin samanaikainen anto ei vaikuttanut topiramaatin vakaan tilan farmakokinetiikkaan.
Karsinogeneesi, mutageneesi ja hedelmällisyyden heikkeneminen
Rotilla tehdyt tutkimukset annoksilla 300 mg/kg/vrk 18 kuukauden ajan eivät osoittaneet karsinogeenisia vaikutuksia. Glyburidi ei ole mutageeninen, kun sitä tutkitaan Salmonella-mikrosomitestillä (Ames-testi) ja DNA-vaurio/emäksisen eluutiomäärityksellä. Mitään lääkkeisiin liittyviä vaikutuksia ei havaittu missään kriteereissä, jotka arvioitiin glyburidin kaksivuotisessa onkogeenisuustutkimuksessa hiirillä.
Raskaus
Teratogeeniset vaikutukset
Lisääntymistutkimuksia on suoritettu rotilla ja kaniineilla annoksilla, jotka ovat jopa 500-kertaisia ihmisen annokseen verrattuna, eivätkä ne ole osoittaneet näyttöä glyburidin aiheuttamasta hedelmällisyyden heikkenemisestä tai haitoista sikiölle. Ei kuitenkaan ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia raskaana olevilla naisilla. Koska eläinten lisääntymistutkimukset eivät aina ennusta ihmisen vastetta, tätä lääkettä tulee käyttää raskauden aikana vain, jos se on selvästi tarpeen.
Koska viimeaikaiset tiedot viittaavat siihen, että epänormaalit verensokeritasot raskauden aikana liittyvät lisääntyneeseen synnynnäisten epämuodostumien ilmaantumiseen, monet asiantuntijat suosittelevat insuliinin käyttöä raskauden aikana verensokerin pitämiseksi mahdollisimman lähellä normaalia.
Ei-teratogeeniset vaikutukset
Pitkittynyttä vaikeaa hypoglykemiaa (4–10 päivää) on raportoitu vastasyntyneillä, joiden äidit ovat saaneet sulfonyyliurealääkettä synnytyksen aikana. Tätä on raportoitu useammin käytettäessä aineita, joilla on pidentynyt puoliintumisaika. Jos MICRONASEa käytetään raskauden aikana, se tulee lopettaa vähintään kaksi viikkoa ennen odotettua toimituspäivää.
Imettävät äidit
Vaikka ei tiedetä, erittyykö glyburidi äidinmaitoon, joidenkin sulfonyyliurealääkkeiden tiedetään erittyvän äidinmaitoon. Koska imettävien imeväisten hypoglykemian mahdollisuus on olemassa, on tehtävä päätös, lopetetaanko imetys vai lopetetaanko lääkkeen käyttö ottaen huomioon lääkkeen merkitys äidille. Jos lääkkeen käyttö lopetetaan ja jos ruokavalio yksinään ei riitä verensokerin hallintaan, insuliinihoitoa tulee harkita.
Käyttö lapsille
Turvallisuutta ja tehokkuutta lapsipotilailla ei ole osoitettu.
Geriatrinen käyttö
Iäkkäät potilaat ovat erityisen herkkiä glukoosia alentavien lääkkeiden hypoglykeemiselle vaikutukselle. Hypoglykemiaa voi olla vaikea tunnistaa vanhuksilla (ks VAROTOIMENPITEET ). Aloitus- ja ylläpitoannostuksen tulee olla varovainen hypoglykeemisten reaktioiden välttämiseksi (ks ANNOSTELU JA HALLINNOINTI ).
Iäkkäät potilaat ovat alttiita kehittymään munuaisten vajaatoiminnalle, mikä saattaa vaarantaa hypoglykemian. Annoksen valintaan tulee sisältyä munuaisten toiminnan arviointi.
YLIANNOSTUS
Sulfonyyliureoiden, mukaan lukien MICRONASE 5 mg -tabletit, yliannostus voi aiheuttaa hypoglykemian. Lieviä hypoglykeemisiä oireita, ilman tajunnan menetystä tai neurologisia löydöksiä, tulee hoitaa aggressiivisesti suun kautta otettavalla glukoosilla ja lääkkeen annostuksen ja/tai ruokailun muutoksilla. Tarkkaa seurantaa tulee jatkaa, kunnes lääkäri on varma, että potilas on poissa vaarasta. Vakavia hypoglykeemisiä reaktioita, joihin liittyy kooma, kouristuksia tai muu neurologinen häiriö, esiintyy harvoin, mutta ne ovat lääketieteellisiä hätätilanteita, jotka vaativat välitöntä sairaalahoitoa. Jos hypoglykeeminen kooma diagnosoidaan tai sitä epäillään, potilaalle tulee antaa nopea suonensisäinen injektio tiivistettyä (50 %) glukoosiliuosta. Tämän jälkeen tulee antaa jatkuva infuusio laimeampaa (10 %) glukoosiliuosta nopeudella, joka pitää verensokerin yli 100 mg/dl:n tasolla. Potilaita tulee seurata tarkasti vähintään 24–48 tunnin ajan, koska hypoglykemia voi uusiutua ilmeisen kliinisen toipumisen jälkeen.
VASTA-AIHEET
MICRONASE 5 mg -tabletit ovat vasta-aiheisia potilaille, joilla on:
KLIININEN FARMAKOLOGIA
Toiminnot
Glyburidi näyttää alentavan verensokeria akuutisti stimuloimalla insuliinin vapautumista haimasta. Tämä vaikutus riippuu toimivista beetasoluista haiman saarekkeissa. Mekanismia, jolla glyburidi alentaa verensokeria pitkäaikaisen annon aikana, ei ole selkeästi osoitettu. Kroonisessa käytössä tyypin II diabeetikoilla verensokeria alentava vaikutus säilyy huolimatta lääkkeen insuliinin eritysvasteen asteittaisesta heikkenemisestä. Haiman ulkopuoliset vaikutukset voivat olla osallisena suun kautta otettavien sulfonyyliurean hypoglykeemisten lääkkeiden vaikutusmekanismissa. Glyburidin ja metformiinin yhdistelmällä voi olla synergistinen vaikutus, koska molemmat aineet parantavat glukoosinsietokykyä erilaisilla mutta toisiaan täydentävillä mekanismeilla.
Jotkut potilaat, jotka alun perin reagoivat suun kautta otettaviin hypoglykeemisiin lääkkeisiin, mukaan lukien MICRONASE, voivat jäädä vastetta tai reagoida huonosti ajan myötä. Vaihtoehtoisesti MICRONASE-tabletit voivat olla tehokkaita joillakin potilailla, jotka eivät ole reagoineet yhdelle tai useammalle muulle sulfonyyliurealääkkeelle.
Verensokeria alentavan vaikutuksensa lisäksi glyburidi aiheuttaa lievää diureesia lisäämällä munuaisten vapaan veden puhdistumaa. Disulfiraamin kaltaisia reaktioita on raportoitu hyvin harvoin potilailla, joita on hoidettu MICRONASE 2,5 mg -tableteilla.
Farmakokinetiikka
MICRONASE 2,5 mg -tableteilla tehdyt kerta-annostutkimukset normaaleilla koehenkilöillä osoittavat glyburidin merkittävän imeytymisen tunnissa, lääkkeen huippupitoisuudet noin neljässä tunnissa ja alhaiset, mutta havaittavissa olevat tasot 24 tunnin kuluttua. Glyburidin keskimääräiset seerumipitoisuudet, kuten seerumin pitoisuus-aikakäyrän alla näkyvät alueet, kasvavat suhteessa vastaaviin annoksen lisäyksiin. MICRONASE 2,5 mg:n useiden annosten tutkimukset diabeetikoilla osoittavat lääketason pitoisuus-aikakäyrät, jotka ovat samankaltaisia kuin kerta-annostutkimukset, mikä osoittaa, ettei lääkettä kertynyt kudosvarastoihin. Glyburidin väheneminen normaalien terveiden yksilöiden seerumissa on kaksivaiheista; terminaalinen puoliintumisaika on noin 10 tuntia. Yksittäisannostutkimuksissa normaaleilla paastopotilailla verensokerin laskun aste ja kesto on verrannollinen annettuun annokseen ja lääketason pitoisuus-aikakäyrän alle. Verensokeria alentava vaikutus säilyy 24 tunnin ajan kerta-aamuannoksen jälkeen ei-paastoamattomilla diabeetikoilla. Toistuvan annostelun olosuhteissa diabeetikoilla ei kuitenkaan ole luotettavaa korrelaatiota veren lääketasojen ja paastoveren glukoositasojen välillä. Yhden vuoden tutkimus MICRONASE-hoitoa saaneilla diabeetikoilla ei osoittanut luotettavaa korrelaatiota annetun annoksen ja seerumin lääketason välillä.
Glyburidin tärkein metaboliitti on 4-transhydroksijohdannainen. Myös toinen metaboliitti, 3-cishydroksijohdannainen, esiintyy. Näillä metaboliiteilla ei todennäköisesti ole merkittävää hypoglykeemistä vaikutusta ihmisillä, koska ne ovat vain heikosti aktiivisia (1/400 ja 1/40 aktiivisista glyburidina) kaneissa. Glyburidi erittyy metaboliitteina sappeen ja virtsaan, noin 50 % kumpaakin reittiä pitkin. Tämä kaksoiseritysreitti eroaa laadullisesti muista sulfonyyliureoista, jotka erittyvät pääasiassa virtsaan.
Sulfonyyliurealääkkeet sitoutuvat laajasti seerumin proteiineihin. Muiden lääkkeiden aiheuttama syrjäytyminen proteiineja sitovista kohdista voi johtaa hypoglykeemisen vaikutuksen lisääntymiseen. In vitro glyburidin sitoutuminen proteiineihin on pääasiassa ionitonta, kun taas muiden sulfonyyliureoiden (klooripropamidi, tolbutamidi, tolatsamidi) sitoutuminen proteiineihin on pääasiassa ionista. Happamat lääkkeet, kuten fenyylibutatsoni, varfariini ja salisylaatit, syrjäyttävät ioneja sitovat sulfonyyliureat seerumin proteiineista paljon suuremmassa määrin kuin ionittomia sitova glyburidi. Ei ole osoitettu, että tämä ero proteiineihin sitoutumisessa johtaisi vähemmän lääkeaineiden yhteisvaikutuksiin MICRONASE-tablettien kanssa kliinisessä käytössä.
POTILASTIEDOT
Potilaille tulee kertoa MICRONASE:n ja vaihtoehtoisten hoitomuotojen mahdollisista riskeistä ja eduista. Heille tulee myös kertoa ruokavalio-ohjeiden noudattamisen, säännöllisen harjoitteluohjelman ja säännöllisen virtsan ja/tai verensokerin mittaamisen tärkeydestä.
Potilaille ja vastuullisille perheenjäsenille tulee selittää hypoglykemian riskit, sen oireet ja hoito sekä sen kehittymiselle altistavat sairaudet. Ensisijainen ja toissijainen vika tulee myös selittää.
