Neoral 25mg, 100mg Cyclosporine Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Neoral 25mg on ja miten sitä käytetään?
Neoral 25mg on reseptilääke, jota käytetään estämään elinsiirron jälkeistä hylkimisreaktiota sekä hoitamaan nivelreuman ja psoriaasin oireita. Neoralia voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Neoral kuuluu lääkeluokkaan, jota kutsutaan DMARD:iksi, immunomodulaattoreiksi; Immunosuppressantit; Kalsineuriinin estäjät.
Ei tiedetä, onko Neoral 25mg turvallinen ja tehokas lapsille.
Mitkä ovat Neoralin mahdolliset sivuvaikutukset?
Neoral voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- nokkosihottuma,
- vaikeuksia hengittää,
- kasvojen, huulten, kielen tai kurkun turvotus,
- puheen, ajatusten, näön tai lihasten liikkeen ongelmia,
- kohtaus,
- kova päänsärky,
- näön hämärtyminen,
- hakkaa niskassasi tai korvissasi,
- kalpea iho,
- helppo mustelma,
- epätavallinen verenvuoto,
- pahoinvointi,
- heikkous,
- kihelmöivä tunne,
- rintakipu,
- epäsäännölliset sydämenlyönnit,
- liikkeen menetys,
- vähän tai ei ollenkaan virtsaamista,
- turvotus jaloissasi tai nilkoissasi,
- väsynyt olo,
- hengenahdistus,
- ruokahalun menetys,
- vatsakipu (oikea yläpuoli),
- ihon tai silmien keltaisuus,
- kuume,
- vilunväristykset,
- flunssan oireet,
- suun haavaumat,
- ihohaavat,
- kurkkukipu ja
- yskä
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Neoralin yleisimpiä sivuvaikutuksia ovat:
- vapina tai vapina,
- akne,
- kasvojen tai vartalon karvojen lisääntynyt kasvu,
- kohonnut verenpaine,
- pahoinvointi,
- ripuli ja
- turvonneet tai kipeät ikenet
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikki Neoralin mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
VAROITUS
Vain lääkärit, joilla on kokemusta systeemisen immunosuppressiivisen hoidon hoidosta indikoidussa sairaudessa, saavat määrätä Neoralia®. Kiinteiden elinsiirtojen yhteydessä käytettävillä annoksilla Neoralia® saavat määrätä vain immunosuppressiiviseen hoitoon ja elinsiirtopotilaiden hoitoon perehtyneet lääkärit. Lääkettä saavia potilaita tulee hoitaa tiloissa, joissa on riittävät laboratorio- ja tukiresurssit ja henkilöstö. Ylläpitohoidosta vastaavalla lääkärillä tulee olla täydelliset tiedot potilaan seurantaa varten. Neoral®, systeeminen immunosuppressantti, voi lisätä infektioherkkyyttä ja kasvainten kehittymistä. Munuaisen, maksan ja sydämensiirtopotilaille Neoral® voidaan antaa muiden immunosuppressiivisten aineiden kanssa. Lisääntynyt alttius infektioille ja mahdollinen lymfooman ja muiden kasvainten kehittyminen voi johtua immunosuppression asteen lisääntymisestä elinsiirtopotilailla.
Neoral®-pehmeät liivatekapselit (syklosporiinikapselit, USP) MODIFIED ja Neoral®-oraaliliuos (syklosporiinioraaliliuos, USP) MODIFIED ovat parantaneet biologista hyötyosuutta verrattuna Sandimmune®-pehmeisiin liivatekapseleihin (syklosporiinikapselit, USP) ja Sandimmune®-oraaliliuokseen (cyclosporine oral Solution) ratkaisu, USP). Neoral® ja Sandimmune® eivät ole bioekvivalentteja, eikä niitä voida käyttää keskenään ilman lääkärin valvontaa. Tietyllä vähimmäispitoisuudella syklosporiinialtistus on suurempi Neoral®:lla kuin Sandimmunella®. Erityistä varovaisuutta on noudatettava, jos potilas, joka saa poikkeuksellisen suuria Sandimmune®-annoksia, siirtyy Neoral®-hoitoon. Veren siklosporiinipitoisuuksia tulee seurata elinsiirto- ja nivelreumapotilailla, jotka käyttävät Neoralia®, jotta vältetään korkeista pitoisuuksista johtuva toksisuus. Annosta tulee muuttaa elinsiirtopotilailla matalista pitoisuuksista johtuvan mahdollisen elimen hylkimisen minimoimiseksi. Julkaistussa kirjallisuudessa esitettyjä veripitoisuuksia verrattaessa nykyisillä määrityksillä saatuihin pitoisuuksiin on tehtävä yksityiskohtaiset tiedot käytetyistä määritysmenetelmistä.
Psoriasispotilaille (katso myös yllä olevaa RAKKAUKSELLISET VAROITUKSET)
Psoriaasipotilailla, joita on aiemmin hoidettu PUVA:lla ja vähemmässä määrin metotreksaatilla tai muilla immunosuppressiivisilla aineilla, UVB-säteilyllä, kivihiilitervalla tai sädehoidolla, on lisääntynyt riski saada ihon pahanlaatuisia kasvaimia Neoral®-hoidon aikana.
Syklosporiini, Neoral®:n aktiivinen ainesosa, voi suositeltuina annoksina aiheuttaa systeemistä kohonnutta verenpainetta ja munuaistoksisuutta. Riski kasvaa siklosporiinihoidon annosta ja kestoa kasvaessa. Munuaisten toimintahäiriö, mukaan lukien rakenteellinen munuaisvaurio, on mahdollinen seuraus siklosporiinista, ja siksi munuaisten toimintaa on seurattava hoidon aikana.
KUVAUS
Neoral® on suun kautta otettava syklosporiiniformulaatio, joka muodostaa välittömästi mikroemulsion vesipitoisessa ympäristössä.
Syklosporiini, Neoral®:n aktiivinen ainesosa, on syklinen polypeptidi-immunosuppressiivinen aine, joka koostuu 11 aminohaposta. Sitä tuottaa aineenvaihduntatuotteena Beauveria nivea -sieni.
Kemiallisesti syklosporiinia kutsutaan [R-[R*,R*-(E)]]-sykliseksi (L-alanyyli-D-alanyyli-N-metyyli-L-leusyyli-N-metyyli-L-leusyyli-N-metyyli). -L-valyyli-3-hydroksi-N,4-dimetyyli-L-2-amino-6-oktenoyyli-L-a-aminobutyryyli-N-metyyliglysyyli-N-metyyli-L-leusyyli-L-valyyli-N-metyyli -L-leusyyli).
Neoral® pehmeät gelatiinikapselit (syklosporiinikapselit, USP) MODIFIED ovat saatavilla 25 mg ja 100 mg vahvuuksina.
Jokainen 25 mg:n kapseli sisältää:
siklosporiini………………………………25 mg alkoholia, USP dehydratoitu...................................11,9 % tilavuus/tilavuus (9,5 % paino/tilavuus)
Jokainen 100 mg:n kapseli sisältää:
siklosporiini………………………………100 mg alkoholia, USP dehydratoitu...................................11.9 % tilavuus/tilavuus (9,5 % paino/tilavuus)
Ei-aktiiviset ainesosat: Maissiöljy-mono-di-triglyseridit, polyoksyyli 40 hydrattu risiiniöljy NF, DL-αtokoferoli USP, gelatiini NF, glyseroli, rautaoksidimusta, propyleeniglykoli USP, titaanidioksidi USP, karmiini ja muut aineosat.
Neoral® Oral Solution (syklosporiinioraaliliuos, USP) MODIFIED on saatavana 50 ml:n pulloissa.
Jokainen ml sisältää:
siklosporiini…………………..................100 mg/ml alkoholia, USP dehydratoitu................ ...........11,9 % tilavuus/tilavuus (9,5 % paino/tilavuus)
Ei-aktiiviset ainesosat: Maissiöljy-mono-di-triglyseridit, polyoksyyli 40 hydrattu risiiniöljy NF, DL-α-tokoferoli USP, propyleeniglykoli USP.
Syklosporiinin (tunnetaan myös nimellä syklosporiini A) kemiallinen rakenne on:
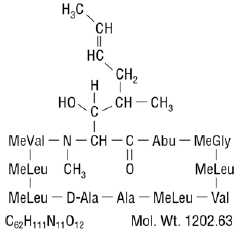
INDIKAATIOT
Munuaisten, maksan ja sydämen siirto
Neoral 25 mg on tarkoitettu elimen hylkimisreaktion ennaltaehkäisyyn munuais-, maksa- ja sydämen allogeenisissa siirroissa. Neoral 100 mg:aa on käytetty yhdessä atsatiopriinin ja kortikosteroidien kanssa.
Nivelreuma
Neoral on tarkoitettu vaikean aktiivisen nivelreuman hoitoon potilaille, joilla tauti ei ole reagoinut riittävästi metotreksaatilla. Neoralia voidaan käyttää yhdessä metotreksaatin kanssa nivelreumapotilailla, jotka eivät anna riittävää vastetta metotreksaatille yksin.
Psoriasis
Neoral on tarkoitettu aikuisten, ei-immuunipuutteisten potilaiden hoitoon, joilla on vakava (eli laaja-alainen ja/tai vammauttava), vastahakoinen läiskäpsoriaasi, jotka eivät ole reagoineet vähintään yhteen systeemiseen hoitoon (esim. PUVA, retinoidit tai metotreksaatti) tai potilaat, joille muut systeemiset hoidot ovat vasta-aiheisia tai joita ei voida sietää.
Vaikka reboundia esiintyy harvoin, useimmat potilaat kokevat uusiutumisen Neoral 100 mg -annoksella, kuten muillakin hoidoilla, kun hoito lopetetaan.
ANNOSTELU JA HALLINNOINTI
Neoral 25mg pehmeät gelatiinikapselit (syklosporiinikapselit, USP) MODIFIE ja Neoral oraaliliuos (syklosporiini oraaliliuos, USP) MODIFIE D
Neoral on parantanut biologista hyötyosuutta Sandimmuneen verrattuna. Neoral 25mg ja Sandimmune eivät ole biologisesti samanarvoisia, eikä niitä voida käyttää keskenään ilman lääkärin valvontaa.
Neoral 100 mg:n vuorokausiannos tulee aina jakaa kahteen annokseen (BID). On suositeltavaa, että Neoralia annetaan yhtenäisen aikataulun mukaisesti vuorokaudenajan ja aterioiden suhteen. Greippi ja greippimehu vaikuttavat aineenvaihduntaan ja lisäävät veren syklosporiinipitoisuutta, joten niitä tulee välttää.
Tietyt populaatiot
Munuaisten vajaatoiminta munuaisten, maksan ja sydämen siirroissa
Siklosporiini eliminoituu vain vähän munuaisten kautta, eikä sen farmakokinetiikka näytä muuttuvan merkittävästi potilailla, joilla on loppuvaiheen munuaissairaus ja jotka saavat rutiininomaista hemodialyysihoitoa (ks. KLIININEN FARMAKOLOGIA ). Kuitenkin sen nefrotoksisen potentiaalin vuoksi (ks VAROITUKSET ), munuaisten toiminnan huolellinen seuranta on suositeltavaa; Siklosporiinin annosta tulee pienentää tarvittaessa (ks VAROITUKSET ja VAROTOIMENPITEET ).
Munuaisten vajaatoiminta nivelreumassa ja psoriaasissa
Potilaiden, joiden munuaisten toiminta on heikentynyt, ei tule saada siklosporiinia (ks VASTA-AIHEET , VAROITUKSET ja VAROTOIMENPITEET ).
Maksan vajaatoiminta
Siklosporiinin puhdistuma voi heikentyä merkittävästi potilailla, joilla on vaikea maksasairaus (ks KLIININEN FARMAKOLOGIA ). Annoksen pienentäminen saattaa olla tarpeen potilailla, joilla on vaikea maksan vajaatoiminta, jotta veren pitoisuus pysyy suositellulla tavoitealueella (ks VAROITUKSET ja VAROTOIMENPITEET ).
Äskettäin siirretyt potilaat
Neoral 25 mg:n aloitusannos suun kautta voidaan antaa 4–12 tuntia ennen elinsiirtoa tai se voidaan antaa leikkauksen jälkeen. Neoral 25 mg:n aloitusannos vaihtelee siirretyn elimen ja muiden immunosuppressiiviseen protokollaan sisältyvien immunosuppressiivisten aineiden mukaan. Äskettäin siirretyillä potilailla Neoralin aloitusannos suun kautta on sama kuin Sandimmunen oraalinen aloitusannos. Ehdotetut aloitusannokset ovat saatavilla vuoden 1994 tutkimuksen tuloksista Sandimmunen käytöstä Yhdysvaltain elinsiirtokeskuksissa. Keskimääräiset ± SD aloitusannokset olivat 9 ± 3 mg/kg/vrk munuaisensiirtopotilaille (75 keskusta), 8 ± 4 mg/kg/vrk maksansiirtopotilaille (30 keskustaa) ja 7 ± 3 mg/kg/vrk. sydämensiirtopotilaille (24 keskusta). Päivittäiset kokonaisannokset jaettiin kahteen yhtä suureen päivittäiseen annokseen. Neoral-annosta säädetään myöhemmin ennalta määrätyn siklosporiinipitoisuuden saavuttamiseksi veressä (ks Veripitoisuuden seuranta elinsiirtopotilailla alla). Jos käytetään siklosporiinin pienimpiä veren pitoisuuksia, tavoitealue on sama Neoral 100 mg:lle kuin Sandimmunelle. Jos Neoral 100 mg:lle käytetään samaa minimipitoisuuden tavoitealuetta kuin Sandimmunelle, seurauksena on suurempi siklosporiinialtistus, kun Neoralia annetaan (ks. Farmakokinetiikka, Imeytyminen ). Annostus tulee titrata hylkimisreaktion ja siedettävyyden kliinisen arvioinnin perusteella. Pienemmät 100 mg Neoral-annokset voivat olla riittäviä ylläpitohoitona.
Lisähoitoa lisämunuaisen kortikosteroideilla suositellaan aluksi. Prednisonin erilaiset kapeneva annostusohjelmat näyttävät saavuttavan samanlaisia tuloksia. Potilaan painoon perustuva edustava annostusohjelma aloitettiin annoksella 2,0 mg/kg/vrk ensimmäisten 4 päivän ajan, ja sitä pienennettiin 1,0 mg/kg/vrk 1 viikon välein, 0,6 mg/kg/vrk 2 viikon kuluttua, 0,3 mg/kg/vrk. 1 kuukauden kuluttua ja 0,15 mg/kg/vrk 2 kuukauden kuluttua ja sen jälkeen ylläpitoannoksena. Steroidiannoksia voidaan pienentää edelleen yksilöllisesti riippuen potilaan tilasta ja siirteen toiminnasta. Prednisonin annosta on mukautettava kliinisen tilanteen mukaan.
Siirtyminen Sandimmunesta Neoral 25 mg:aan elinsiirtopotilailla
Elinsiirtopotilailla, joiden harkitaan siirtymistä Sandimmunesta Neoraliin, Neoral-hoito tulee aloittaa samalla päiväannoksella kuin aiemmin Sandimmunen kanssa (annoksen muuntaminen 1:1). Neoral-annosta tulee tämän jälkeen säätää, jotta saavutetaan konversiota edeltävä siklosporiinin alin pitoisuus veressä. Jos Neoral 100 mg:lle käytetään samaa minimipitoisuuden tavoitealuetta kuin Sandimmunelle, seurauksena on suurempi siklosporiinialtistus, kun Neoralia annetaan (ks. Farmakokinetiikka, Imeytyminen ). Potilaat, joilla epäillään Sandimmunen huonoa imeytymistä, tarvitsevat erilaisia annostusstrategioita (ks. Elinsiirtopotilaat, joilla Sandimmune imeytyy huonosti, alla). Joillakin potilailla veren pohjapitoisuuden nousu on selvempää ja sillä voi olla kliinistä merkitystä.
Kunnes veren alin pitoisuus saavuttaa konversiota edeltävän arvon, on erittäin suositeltavaa, että siklosporiinin veripitoisuutta seurataan 4–7 päivän välein Neoral-hoitoon siirtymisen jälkeen. Lisäksi kliinisiä turvallisuusparametreja, kuten seerumin kreatiniinia ja verenpainetta, on seurattava kahden viikon välein kahden ensimmäisen kuukauden aikana muutoksen jälkeen. Jos veren pohjapitoisuudet ovat halutun alueen ulkopuolella ja/tai kliiniset turvallisuusparametrit huononevat, Neoral 100mg:n annosta on muutettava vastaavasti.
Elinsiirtopotilaat, joiden Sandimmune imeytyy huonosti
Potilailla, joilla on odotettua alhaisemmat siklosporiinin pitoisuudet veressä suhteessa Sandimmunen oraaliseen annokseen, voi olla huono tai epäjohdonmukainen siklosporiinin imeytyminen Sandimmunesta. Neoral-hoitoon siirtymisen jälkeen potilaiden siklosporiinipitoisuudet ovat yleensä korkeammat. Syklosporiinin biologisen hyötyosuuden lisääntymisen vuoksi Neoral-valmisteeksi muuttamisen jälkeen siklosporiinin vähimmäispitoisuus veressä voi ylittää tavoitealueen. Erityistä varovaisuutta tulee noudattaa siirrettäessä potilaita Neoral 100 mg -annoksiin, jotka ovat suurempia kuin 10 mg/kg/vrk. Neoralin annos tulee titrata yksilöllisesti siklosporiinin pienimmän pitoisuuden, siedettävyyden ja kliinisen vasteen perusteella. Tässä populaatiossa siklosporiinin vähimmäispitoisuus veressä tulee mitata useammin, vähintään kahdesti viikossa (päivittäin, jos aloitusannos ylittää 10 mg/kg/vrk), kunnes pitoisuus vakiintuu halutulle alueelle.
Nivelreuma
Neoralin aloitusannos on 2,5 mg/kg/vrk, joka otetaan kahdesti päivässä jaettuna (BID) oraaliseen annokseen. Salisylaattien, tulehduskipulääkkeiden ja oraalisten kortikosteroidien käyttöä voidaan jatkaa (ks VAROITUKSET ja VAROTOIMENPITEET , HUUMEIDEN VUOROVAIKUTUKSET ). Vaikutus alkaa yleensä 4-8 viikon kuluttua. Jos kliininen hyöty ei ole riittävä ja siedettävyys on hyvä (mukaan lukien seerumin kreatiniini alle 30 % lähtötason yläpuolella), annosta voidaan suurentaa 0,5–0,75 mg/kg/vrk 8 viikon kuluttua ja uudelleen 12 viikon kuluttua enintään 4 mg:aan. /kg/päivä. Jos hyötyä ei ole havaittavissa 16 hoitoviikon kuluessa, Neoral 25 mg -hoito on lopetettava.
Annosta on pienennettävä 25–50 % milloin tahansa haittatapahtumien, esim. seerumin kreatiniinipitoisuuden nousun (30 % potilaan hoitoa edeltävän tason yläpuolella) tai kliinisesti merkittävien laboratorioarvojen poikkeavuuksien hallitsemiseksi (ks. VAROITUKSET ja VAROTOIMENPITEET ).
Jos annoksen pienentäminen ei ole tehokasta poikkeavuuksien hallinnassa tai jos haittatapahtuma tai poikkeavuus on vakava, Neoral 25 mg -valmisteen käyttö on lopetettava. Samaa aloitusannosta ja annosaluetta tulee käyttää, jos Neoral 25 mg yhdistetään suositeltuun metotreksaattiannokseen. Useimpia potilaita voidaan hoitaa Neoralin 25 mg:n annoksilla 3 mg/kg/vrk tai sitä pienemmillä annoksilla yhdistettynä metotreksaattiannoksiin, jotka ovat enintään 15 mg/viikko (ks. KLIININEN FARMAKOLOGIA , Kliiniset tutkimukset ).
Pitkäaikaisesta hoidosta on vain vähän tietoja. Nivelreuman aktiivisuuden uusiutuminen ilmenee yleensä 4 viikon kuluessa siklosporiinihoidon lopettamisesta.
Psoriasis
Neoral 100 mg:n aloitusannoksen tulee olla 2,5 mg/kg/vrk. Neoralia tulee ottaa kahdesti päivässä jaettuna (1,25 mg/kg kahdesti vuorokaudessa) suun kautta. Potilaita tulee pitää tällä annoksella vähintään 4 viikon ajan haittatapahtumia lukuun ottamatta. Jos merkittävää kliinistä paranemista ei ole tapahtunut siihen mennessä, potilaan annosta tulee suurentaa 2 viikon välein. Potilaan vasteen perusteella annosta tulee suurentaa noin 0,5 mg/kg/vrk enintään 4,0 mg/kg/vrk.
Annosta on pienennettävä 25–50 % milloin tahansa haittatapahtumien, esim. verenpainetaudin, seerumin kreatiniinipitoisuuden nousun (≥ 25 % yli potilaan hoitoa edeltävän tason) tai kliinisesti merkittävien laboratorioarvojen poikkeavuuksien hallitsemiseksi. Jos annoksen pienentäminen ei ole tehokasta poikkeavuuksien hallinnassa tai jos haittatapahtuma tai poikkeavuus on vakava, Neoral 25 mg -valmisteen käyttö on lopetettava (ks. Psoriasispotilaiden erityisseuranta ).
Potilaat osoittavat yleensä jonkin verran paranemista psoriaasin kliinisissä oireissa kahdessa viikossa. Taudin tyydyttävä hallinta ja vakauttaminen voi kestää 12–16 viikkoa. Neoral 25 mg:lla tehdyn annoksen titraustutkimuksen tulokset osoittavat, että psoriaasin paraneminen 75 % tai enemmän (PASI:n perusteella) saavutettiin 51 %:lla potilaista 8 viikon kuluttua ja 79 %:lla potilaista 16 viikon kuluttua. Hoito on lopetettava, jos tyydyttävää vastetta ei saada aikaan 6 viikon kuluttua annoksella 4 mg/kg/vrk tai potilaan suurimmalla siedetyllä annoksella. Kun potilas on riittävästi hallinnassa ja vaikuttaa vakaalta, Neoral 25 mg -annosta on pienennettävä ja potilasta hoidettava pienimmällä annoksella, joka ylläpitää riittävän vasteen (tämän ei välttämättä pitäisi olla potilaan täydellistä tyhjenemistä). Kliinisissä tutkimuksissa 60 %:lla potilaista siklosporiiniannokset suositellun annosalueen alemmilla rajoilla säilyttivät tehokkaasti tyydyttävän vasteen. Alle 2,5 mg/kg/vrk annokset voivat myös olla yhtä tehokkaita.
Kun siklosporiinihoito lopetetaan, uusiutuminen tapahtuu noin 6 viikon (50 % potilaista) - 16 viikon (75 % potilaista) kuluttua. Suurimmalla osalla potilaista palautumista ei tapahdu siklosporiinihoidon lopettamisen jälkeen. Kolmetoista tapausta kroonisen plakkipsoriaasin muuttumisesta vaikeammiksi psoriaasin muodoiksi on raportoitu. 9 pustulaarista ja 4 erytrodermista psoriaasia tapausta. Pitkäaikainen kokemus Neoralin käytöstä psoriaasipotilailla on rajallinen, eikä jatkuvaa yli vuoden pituista hoitoa suositella. Vuorottelua muiden hoitomuotojen kanssa tulee harkita tätä elinikäistä sairautta sairastavien potilaiden pitkäaikaishoidossa.
Neoral 25mg oraaliliuos (syklosporiini oraaliliuos, USP) MUUTETTU - Antosuositukset
Jotta Neoral 25 mg oraaliliuos (syklosporiini oraaliliuos, USP) MODIFED olisi maistuvampaa, se tulee laimentaa appelsiini- tai omenamehulla, joka on huoneenlämpöinen. Potilaiden tulee välttää laimentimien vaihtamista usein. Greippimehu vaikuttaa syklosporiinin aineenvaihduntaan ja sitä tulee välttää. Neoral-liuoksen yhdistelmä maidon kanssa voi olla epämiellyttävää. Maidon vaikutusta siklosporiinin biologiseen hyötyosuuteen, kun sitä annetaan Neoral 100 mg oraaliliuoksena, ei ole arvioitu.
Ota määrätty määrä Neoral 25 mg oraaliliuosta (syklosporiinioraaliliuos, USP) MODIFIED säiliöstä käyttämällä mukana toimitettua annosruiskua suojakannen poistamisen jälkeen ja siirrä liuos appelsiini- tai omenamehulasiin. Sekoita hyvin ja juo heti. Älä anna laimennetun oraaliliuoksen seistä ennen juomista. Käytä lasiastiaa (ei muovia). Huuhtele lasi lisää laimennusainetta varmistaaksesi, että koko annos kuluu. Kuivaa annosruiskun ulkopuoli käytön jälkeen puhtaalla pyyhkeellä ja aseta suojakansi takaisin paikalleen. Älä huuhtele annosruiskua vedellä tai muilla puhdistusaineilla. Jos ruisku vaatii puhdistusta, sen on oltava täysin kuiva ennen käytön jatkamista.
Veripitoisuuden seuranta elinsiirtopotilailla
Elinsiirtokeskukset ovat havainneet veren syklosporiinipitoisuuden seurannan olevan olennainen osa potilaan hoitoa. Veren konsentraatioanalyysin kannalta tärkeitä ovat käytetyn määrityksen tyyppi, siirretty elin ja muut annettavat immunosuppressiiviset aineet. Vaikka kiinteää yhteyttä ei ole vahvistettu, veren pitoisuuden seuranta voi auttaa hylkimisen ja toksisuuden kliinisessä arvioinnissa, annoksen säätämisessä ja hoitomyöntyvyyden arvioinnissa.
Syklosporiinin veren pitoisuuksien mittaamiseen on käytetty erilaisia määrityksiä. Vanhemmissa tutkimuksissa, joissa käytettiin epäspesifistä määritystä, viitattiin usein pitoisuuksiin, jotka olivat suunnilleen kaksi kertaa spesifisiin määrityksiin verrattuna. Siksi julkaistun kirjallisuuden pitoisuuksien ja yksittäisten potilaan pitoisuuksien vertailu nykyisiä määrityksiä käyttäen on tehtävä yksityiskohtaisten tietojen perusteella käytetyistä määritysmenetelmistä. Nykyiset määritystulokset eivät myöskään ole keskenään vaihdettavissa, ja niiden käyttöä tulee ohjata hyväksyttyjen merkintöjen mukaan. Keskustelu erilaisista määritysmenetelmistä on julkaisussa Annals of Clinical Biochemistry 1994; 31: 420-446. Vaikka useita määrityksiä ja määritysmatriiseja on saatavilla, vallitsee yksimielisyys siitä, että emoyhdistekohtaiset määritykset korreloivat parhaiten kliinisten tapahtumien kanssa. Näistä HPLC on vakiovertailu, mutta monoklonaalinen vasta-aine RIA ja monoklonaalinen vasta-aine FPIA tarjoavat herkkyyttä, toistettavuutta ja mukavuutta. Useimmat kliinikot perustavat seurantansa syklosporiinin pienimpään pitoisuuteen. Applied Pharmacokinetics, Principles of Therapeutic Drug Monitoring (1992) sisältää laajan keskustelun syklosporiinin farmakokinetiikasta ja lääkkeiden seurantatekniikoista. Veripitoisuuden seuranta ei korvaa munuaisten toiminnan seurantaa tai kudosbiopsioita.
MITEN TOIMITETAAN
Neoral® pehmeät gelatiinikapselit (syklosporiinikapselit, USP) MUUTETTU
25 mg
Soikea, siniharmaa, painettu punaisella, "Neoral" yli "25 mg".
Pakkauksissa 30 yksikköannoksen läpipainopakkausta ( NDC 0078-0246-15).
100 mg
Pitkät, siniharmaat, punaisella painettu "NEORAL" yli "100 mg".
Pakkauksissa 30 yksikköannoksen läpipainopakkausta ( NDC 0078-0248-15).
Säilytä Ja Annostele
Alkuperäisessä yksikköannospakkauksessa valvotussa huoneenlämpötilassa 68 °F - 77 °F (20 °C - 25 °C).
Neoral®-oraaliliuos (Cyclosporine Oral Solution, USP) MUUTETTU
Kirkas, keltainen neste, joka toimitetaan 50 ml:n pulloissa, jotka sisältävät 100 mg/ml ( NDC 0078-0274-22).
Säilytä Ja Annostele
Alkuperäisessä pakkauksessa valvotussa huoneenlämpötilassa 68°F - 77°F (20° - 25°C). Älä säilytä jääkaapissa. Avattu sisältö on käytettävä kahden kuukauden kuluessa. Alle 68 °F (20 °C) lämpötiloissa liuos voi geeliytyä; kevyttä flokkulaatiota tai kevyen sedimentin muodostumista voi myös esiintyä. Ei vaikuta tuotteen suorituskykyyn tai annostukseen käyttämällä mukana toimitettua ruiskua. Anna lämmetä huoneenlämpötilaan 25 °C (77 °F) näiden muutosten kumoamiseksi.
Neoral® pehmeät gelatiinikapselit (syklosporiinikapselit, USP) MUUTETTU
Neoral® Oral Solution (syklosporiinioraaliliuos, USP) MUUTETTU
Jakelija: Novartis Pharmaceuticals Corporation, East Hanover, New Jersey 07936. Tarkistettu kesäkuussa 2021.
SIVUVAIKUTUKSET
Munuaisten, maksan ja sydämen siirto
Siklosporiinihoidon tärkeimmät haittavaikutukset ovat munuaisten vajaatoiminta, vapina, hirsutismi, kohonnut verenpaine ja ikenien liikakasvu.
Hypertensio
Hypertensiota, joka on yleensä lievä tai kohtalainen, voi esiintyä noin 50 %:lla munuaisensiirron jälkeen potilaista ja useimmilla sydämensiirtopotilailla.
Glomerulaarinen kapillaaritromboosi
Glomerulaarista kapillaaritromboosia on havaittu potilailla, joita on hoidettu siklosporiinilla, ja se voi edetä siirteen vajaatoiminnaksi. Patologiset muutokset muistuttivat hemolyyttis-ureemisessa oireyhtymässä havaittuja muutoksia, ja niihin sisältyi munuaisten mikroverisuoniston tromboosi, jossa verihiutale-fibriinitrombi tukkii glomerulaarisia kapillaareja ja afferentteja arterioleja, mikroangiopaattinen hemolyyttinen anemia, trombosytopenia ja munuaisten toiminnan heikkeneminen. Samanlaisia löydöksiä on havaittu, kun muita immunosuppressiivisia aineita on käytetty transplantaation jälkeen.
Hypomagnesemia
Hypomagnesemiaa on raportoitu joillakin, mutta ei kaikilla, potilailla, joilla on esiintynyt kouristuksia siklosporiinihoidon aikana. Vaikka magnesiumvajausta koskevat tutkimukset normaaleilla koehenkilöillä viittaavat siihen, että hypomagnesemia liittyy neurologisiin häiriöihin, useat tekijät, mukaan lukien verenpainetauti, korkean annoksen metyyliprednisoloni, hypokolesterolemia ja suuriin plasman syklosporiinipitoisuuksiin liittyvä nefrotoksisuus näyttävät liittyvän siklosporiinitoksisuuden neurologisiin ilmenemismuotoihin.
HUUMEIDEN VUOROVAIKUTUKSET
Lääkkeiden ja muiden aineiden vaikutus syklosporiinin farmakokinetiikkaan ja/tai turvallisuuteen
Kaikki alla mainitut yksittäiset lääkkeet ovat hyvin perusteltuja vuorovaikutuksessa syklosporiinin kanssa. Lisäksi tulehduskipulääkkeiden samanaikainen käyttö siklosporiinin kanssa, erityisesti dehydraatiotilanteessa, voi voimistaa munuaisten vajaatoimintaa. Varovaisuutta tulee noudattaa käytettäessä muita lääkkeitä, joiden tiedetään heikentävän munuaisten toimintaa (ks VAROITUKSET , Nefrotoksisuus ).
Lääkkeet, jotka voivat tehostaa munuaisten vajaatoimintaa
Kun siklosporiinin kanssa käytetään samanaikaisesti lääkettä, joka voi aiheuttaa additiivista tai synergististä munuaisten vajaatoimintaa, munuaisten toimintaa (erityisesti seerumin kreatiniinia) on seurattava tarkasti. Jos merkittävää munuaisten vajaatoimintaa ilmenee, samanaikaisesti annettavan lääkkeen annosta tulee pienentää tai vaihtoehtoista hoitoa harkita.
Syklosporiini metaboloituu laajalti CYP3A-isoentsyymien, erityisesti CYP3A4:n, toimesta, ja se on usean lääkkeen ulosvirtauksen kuljettavan P-glykoproteiinin substraatti. Erilaisten aineiden tiedetään joko lisäävän tai vähentävän plasman tai kokoveren siklosporiinin pitoisuuksia, yleensä estämällä tai indusoimalla CYP3A4:n tai P-glykoproteiinin kuljettajaa tai molempia. Yhdisteitä, jotka vähentävät syklosporiinin imeytymistä, kuten orlistaattia, tulee välttää. Asianmukainen Neoral 100 mg annoksen säätö haluttujen siklosporiinipitoisuuksien saavuttamiseksi on välttämätöntä, kun samanaikaisesti käytetään lääkkeitä, jotka muuttavat merkittävästi siklosporiinipitoisuuksia (ks. B lood Pitoisuuden seuranta ).
1. Lääkkeet, jotka lisäävät syklosporiinipitoisuuksia
HIV-proteaasin estäjät
HIV-proteaasin estäjien (esim. indinaviirin, nelfinaviirin, ritonaviirin ja sakinaviirin) tiedetään inhiboivan sytokromi P-450 3A:ta ja siten mahdollisesti lisäävän siklosporiinin pitoisuuksia, mutta muodollisia yhteisvaikutustutkimuksia ei ole saatavilla. Varovaisuutta on noudatettava, kun näitä lääkkeitä annetaan samanaikaisesti.
Greippimehu
Greippi ja greippimehu vaikuttavat aineenvaihduntaan ja lisäävät veren syklosporiinipitoisuuksia, joten niitä tulee välttää.
2. Lääkkeet/ravintolisät, jotka vähentävät syklosporiinipitoisuuksia
Bosentaani
Bosentaanin (250 - 1000 mg 12 tunnin välein siedettävyyden perusteella) ja siklosporiinin (300 mg 12 tunnin välein 2 päivän ajan, sitten annostelu, jotta saavutettiin Cmax 200 - 250 ng/ml) samanaikainen anto 7 päivän ajan terveillä koehenkilöillä alensi siklosporiinin keskimääräinen annoksella normalisoitu AUC, Cmax ja pienin pitoisuus oli noin 50 %, 30 % ja 60 %, verrattuna siihen, kun siklosporiinia annettiin yksinään (ks. Syklosporiinin vaikutus muiden lääkkeiden tai aineiden farmakokinetiikkaan ja/tai turvallisuuteen ). Siklosporiinin samanaikaista antamista bosentaanin kanssa tulee välttää.
Boceprevir
Bosepreviirin (800 mg kolme kertaa vuorokaudessa 7 päivän ajan) ja siklosporiinin (100 mg kerta-annos) samanaikainen anto terveille koehenkilöille johti siklosporiinin keskimääräisen AUC:n nousuun noin 2,7-kertaiseksi ja Cmax:n 2-kertaiseksi verrattuna siklosporiinin käyttöön. annettiin yksin.
Telaprevir
Telapreviirin (750 mg joka 8. tunti 11 päivän ajan) ja siklosporiinin (10 mg päivänä 8) samanaikainen anto terveillä koehenkilöillä johti siklosporiinin keskimääräisen annoksen normalisoidun AUC:n nousuun noin 4,5-kertaiseksi ja Cmax:n 1,3-kertaiseksi. verrattuna siihen, kun siklosporiinia (100 mg kerta-annos) annettiin yksinään.
mäkikuisma
On raportoitu vakavasta lääkevuorovaikutuksesta siklosporiinin ja rohdosperäisen mäkikuisman välillä. Tämän yhteisvaikutuksen on raportoitu alentavan merkittävästi syklosporiinin pitoisuutta veressä, mikä johtaa subterapeuttisiin tasoihin, siirrettyjen elinten hylkimiseen ja siirteen menettämiseen.
Rifabutiini
Rifabutiinin tiedetään lisäävän muiden sytokromi P-450 -järjestelmän metaboloimien lääkkeiden metaboliaa. Rifabutiinin ja siklosporiinin välistä yhteisvaikutusta ei ole tutkittu. On noudatettava varovaisuutta, kun näitä kahta lääkettä annetaan samanaikaisesti.
Syklosporiinin vaikutus muiden lääkkeiden tai aineiden farmakokinetiikkaan ja/tai turvallisuuteen
Siklosporiini on CYP3A4:n ja useiden lääkkeiden ulosvirtauksen kuljettajien (esim. P-glykoproteiinin) estäjä ja voi lisätä sellaisten lääkevalmisteiden pitoisuuksia plasmassa, jotka ovat CYP3A4:n, P-glykoproteiinin tai orgaanisten anionien kuljettajaproteiinien substraatteja.
Siklosporiini voi vähentää digoksiinin, kolkisiinin, prednisolonin, HMG-CoA-reduktaasin estäjien (statiinien) ja aliskireenin, bosentaanin, dabigatraanin, repaglinidin, tulehduskipulääkkeiden, sirolimuusin, etoposidin ja muiden lääkkeiden puhdistumaa.
Katso toisen lääkkeen täydelliset reseptitiedot saadaksesi lisätietoja ja erityisiä suosituksia. Terveydenhuollon tarjoajan tulee tehdä päätös siklosporiinin samanaikaisesta antamisesta muiden lääkkeiden tai aineiden kanssa arvioituaan huolellisesti hyödyt ja riskit.
Digoksiini
Useilla digoksiinia käyttävillä potilailla on havaittu vakavaa digitalistoksisuutta muutaman päivän sisällä siklosporiinihoidon aloittamisesta. Jos digoksiinia käytetään samanaikaisesti siklosporiinin kanssa, seerumin digoksiinipitoisuutta on seurattava.
Kolkisiini
On raportoitu siklosporiinin mahdollisuudesta lisätä kolkisiinin toksisia vaikutuksia, kuten myopatiaa ja neuropatiaa, erityisesti potilailla, joilla on munuaisten vajaatoiminta. Syklosporiinin ja kolkisiinin samanaikainen anto johtaa merkittävään kolkisiinin plasmapitoisuuden nousuun. Jos kolkisiinia käytetään samanaikaisesti siklosporiinin kanssa, kolkisiinin annoksen pienentämistä suositellaan.
HMG-CoA-reduktaasin estäjät (statiinit)
Kirjallisuudessa ja markkinoille tulon jälkeen on raportoitu myotoksisuustapauksia, mukaan lukien lihaskipu ja -heikkous, myosiitti ja rabdomyolyysi, kun siklosporiinia on annettu samanaikaisesti lovastatiinin, simvastatiinin, atorvastatiinin, pravastatiinin ja harvoin fluvastatiinin kanssa. Kun näitä statiineja annetaan samanaikaisesti siklosporiinin kanssa, näiden statiinien annosta tulee pienentää etiketin suositusten mukaisesti. Statiinihoito on tilapäisesti keskeytettävä tai lopetettava potilailla, joilla on myopatian merkkejä ja oireita tai joilla on riskitekijöitä, jotka altistavat vakavalle munuaisvauriolle, mukaan lukien munuaisten vajaatoiminta, joka johtuu rabdomyolyysistä.
Repaglinidi
Siklosporiini voi suurentaa plasman repaglinidin pitoisuuksia ja siten lisätä hypoglykemian riskiä. 12 terveellä miespuolisella koehenkilöllä, jotka saivat kaksi annosta 100 mg:n siklosporiinikapselia suun kautta 12 tunnin välein ja kerta-annoksena 0,25 mg:n repagliniditabletti (puolet 0,5 mg:n tabletista) suun kautta 13 tuntia siklosporiinin aloitusannoksen jälkeen, repaglinidin keskimääräinen Cmax ja AUC nousi 1,8-kertaiseksi (vaihteluväli: 0,6-3,7-kertaiseksi) ja 2,4-kertaiseksi (vaihteluväli 1,2-5,3-kertaiseksi). Syklosporiinia ja repaglinidia samanaikaisesti käyttävien potilaiden verensokeripitoisuuden tarkka seuranta on suositeltavaa.
Ambrisentaani
Ambrisentaanin (5 mg vuorokaudessa) ja siklosporiinin (alkuvaiheessa 100-150 mg kahdesti vuorokaudessa, sitten annostelu Cmax 150-200 ng/ml:n saavuttamiseksi) samanaikainen antaminen 8 päivän ajan terveille koehenkilöille johti ambrisentaanin AUC- ja Cmax-arvojen keskimääräiseen nousuun noin 2 kertaiseksi ja 1,5-kertaiseksi verrattuna pelkkään ambrisentaaniin. Kun ambrisentaania annetaan samanaikaisesti siklosporiinin kanssa, ambrisentaaniannosta ei saa titrata suositeltuun enimmäisvuorokausiannokseen
Antrasykliiniantibiootit
Suuret siklosporiiniannokset (esim. laskimonsisäisellä aloitusannoksella 16 mg/kg/vrk) voivat lisätä altistumista antrasykliiniantibiooteille (esim. doksorubisiini, mitoksantroni, daunorubisiini) syöpäpotilailla.
Aliskiren
Siklosporiini muuttaa aliskireenin, P-glykoproteiinin ja CYP3A4:n substraatin, farmakokinetiikkaa. 14 terveellä koehenkilöllä, jotka saivat samanaikaisesti kerta-annoksia siklosporiinia (200 mg) ja pienempiä annoksia aliskireenia (75 mg), aliskireenin keskimääräinen Cmax nousi noin 2,5-kertaiseksi (90 % CI: 1,96-3,17) ja keskimääräinen AUC noin 4,3-kertainen (90 % luottamusväli: 3,52-5,21) verrattuna siihen, kun nämä koehenkilöt saivat pelkkää aliskireenia. Aliskireenin ja siklosporiinin samanaikainen anto pidensi aliskireenin eliminaation puoliintumisaikaa (26 tuntia vs. 43-45 tuntia) ja T-aikaa (0,5 tuntia vs. 1,5-2,0 tuntia). Siklosporiinin keskimääräiset AUC- ja Cmax-arvot olivat verrattavissa kirjallisuudessa ilmoitettuihin arvoihin. Syklosporiinin ja aliskireenin samanaikainen anto näillä koehenkilöillä johti myös haittatapahtumien, pääasiassa päänsäryn, kuuman aallon, pahoinvoinnin, oksentelun ja uneliaisuuden, lukumäärän ja/tai voimakkuuden lisääntymiseen. Siklosporiinin ja aliskireenin yhteiskäyttöä ei suositella.
Bosentaani
Terveillä koehenkilöillä bosentaanin ja siklosporiinin samanaikainen anto johti ajasta riippuvaiseen keskimääräiseen annoksen normalisoitumiseen.
bosentaanin pienimmät pitoisuudet (eli noin 21-kertaiset päivänä 1 ja 2-kertaiset päivänä 8 (tasapaino)) verrattuna siihen, kun bosentaania annettiin yksinään yhtenä annoksena päivänä 1 (ks. Lääkkeiden ja muiden aineiden vaikutus syklosporiinin farmakokinetiikkaan ja/tai turvallisuuteen ). Siklosporiinin samanaikaista antamista bosentaanin kanssa tulee välttää.
Dabigatran
Siklosporiinin vaikutusta dabigatraanipitoisuuksiin ei ollut virallisesti tutkittu. Dabigatraanin ja siklosporiinin samanaikainen anto saattaa suurentaa plasman dabigatraanipitoisuuksia siklosporiinin P-gp:tä estävän vaikutuksen vuoksi. Siklosporiinin yhteiskäyttöä dabigatraanin kanssa tulee välttää.
Kaliumia säästävät diureetit
Syklosporiinia ei tule käyttää kaliumia säästävien diureettien kanssa, koska hyperkalemiaa voi esiintyä. Varovaisuutta on noudatettava myös silloin, kun siklosporiinia annetaan samanaikaisesti kaliumia säästävien lääkkeiden (esim. angiotensiinikonvertaasin estäjien, angiotensiini II -reseptorin salpaajien), kaliumia sisältävien lääkkeiden kanssa sekä potilaille, jotka noudattavat runsaasti kaliumia sisältävää ruokavaliota. Kaliumpitoisuuden hallinta näissä tilanteissa on suositeltavaa.
Ei-steroidisten tulehduskipulääkkeiden (NSAID) yhteisvaikutukset
Kliinistä tilaa ja seerumin kreatiniiniarvoa on seurattava tarkasti, kun siklosporiinia käytetään yhdessä tulehduskipulääkkeiden kanssa nivelreumapotilailla (ks. VAROITUKSET ).
Farmakodynaamisia yhteisvaikutuksia on raportoitu esiintyvän syklosporiinin ja sekä naprokseenin että sulindaakin välillä, koska samanaikainen käyttö liittyy additiiviseen munuaisten toiminnan heikkenemiseen, mikä on määritetty 99mTc-dietyleenitriamiinipentaetikkahapon (DTPA) ja (p-aminohippurihapon) PAH-puhdistuman perusteella. Vaikka diklofenaakin samanaikainen anto ei vaikuta siklosporiinin pitoisuuksiin veressä, siihen on liittynyt diklofenaakkipitoisuuksien noin kaksinkertaistuminen veressä ja satunnaisia raportteja palautuvasta munuaisten toiminnan heikkenemisestä. Näin ollen diklofenaakkiannoksen tulee olla terapeuttisen alueen alimmalla tasolla.
Metotreksaatin yhteisvaikutus
Alustavat tiedot osoittavat, että kun metotreksaattia ja siklosporiinia annettiin samanaikaisesti nivelreumapotilaille (N = 20), metotreksaattipitoisuudet (AUC) nousivat noin 30 % ja sen metaboliitin, 7-hydroksimetotreksaatin, pitoisuudet (AUC:t) pienenivät noin 80 %. %. Tämän yhteisvaikutuksen kliinistä merkitystä ei tunneta. Syklosporiinipitoisuudet eivät näytä muuttuneen (N = 6).
Sirolimus
Seerumin kreatiniinipitoisuuden nousua havaittiin tutkimuksissa, joissa sirolimuusia käytettiin yhdessä täyden annoksen siklosporiinin kanssa. Tämä vaikutus on usein palautuva siklosporiinin annosta pienentämällä. Syklosporiinin samanaikainen käyttö lisää merkittävästi sirolimuusin pitoisuutta veressä. Sirolimuusipitoisuuksien nousun minimoimiseksi suositellaan, että sirolimuusi annetaan 4 tuntia siklosporiinin annon jälkeen.
Nifedipiini
Toistuvaa ienten liikakasvua on raportoitu, kun nifedipiiniä annetaan samanaikaisesti siklosporiinin kanssa. Nifedipiinin samanaikaista käyttöä tulee välttää potilailla, joille syklosporiinin sivuvaikutuksena kehittyy ikenen liikakasvu.
Metyyliprednisoloni
Kouristuksia, kun suuria annoksia metyyliprednisolonia annetaan samanaikaisesti siklosporiinin kanssa, on raportoitu.
Muut immunosuppressiiviset lääkkeet ja aineet
Psoriasispotilaat, jotka saavat muita immunosuppressiivisia aineita tai sädehoitoa (mukaan lukien PUVA ja UVB), eivät saa saada samanaikaisesti siklosporiinia liiallisen immunosuppression mahdollisuuden vuoksi.
Syklosporiinin vaikutus elävien rokotteiden tehokkuuteen
Siklosporiinihoidon aikana rokotus voi olla vähemmän tehokas. Elävien rokotteiden käyttöä tulee välttää.
Lisätietoja syklosporiinilääkkeiden yhteisvaikutuksista saat ottamalla yhteyttä Novartisin lääketieteellisten asioiden osastoon numeroon 1-888-NOW-NOVA [1-888-669-6682].
VAROITUKSET
(Katso myös LAATIKKO VAROITUS )
Kaikki potilaat
Syklosporiini, Neoral 25 mg:n vaikuttava aine, voi aiheuttaa munuaistoksisuutta ja hepatotoksisuutta. Riski kasvaa siklosporiiniannosten kasvaessa. Munuaisten vajaatoiminta, mukaan lukien rakenteellinen munuaisvaurio, on mahdollinen seuraus Neoral 100 mg:n käytöstä, ja siksi munuaisten toimintaa on seurattava hoidon aikana. On noudatettava varovaisuutta käytettäessä siklosporiinia nefrotoksisten lääkkeiden kanssa (katso VAROTOIMENPITEET ).
Neoralia saavat potilaat tarvitsevat seerumin kreatiniinin säännöllistä seurantaa (ks Erityinen seuranta alla ANNOSTELU JA HALLINNOINTI ). Iäkkäitä potilaita tulee seurata erityisen huolellisesti, koska myös munuaisten toiminta heikkenee iän myötä. Jos potilaita ei valvota kunnolla eikä annosta säädetä oikein, siklosporiinihoitoon voi liittyä rakenteellisia munuaisvaurioita ja jatkuvaa munuaisten vajaatoimintaa.
Seerumin kreatiniini- ja BUN-arvot voivat kohota Neoral-hoidon aikana ja heijastaa glomerulusten suodatusnopeuden vähenemistä. Munuaisten vajaatoiminta milloin tahansa vaatii tarkkaa seurantaa, ja annoksen tiheä muuttaminen voi olla aiheellista. Seerumin kreatiniinipitoisuuden nousun esiintymistiheys ja vakavuus lisääntyvät siklosporiinihoidon annoksen ja keston myötä. Nämä nousut tulevat todennäköisesti selvemmiksi ilman annoksen pienentämistä tai hoidon lopettamista.
Koska Neoral 100 mg ei ole bioekvivalentti Sandimmunen kanssa, Neoral-valmisteesta Sandimmuneksi muuttaminen suhteessa 1:1 (mg/kg/vrk) voi johtaa alhaisempiin siklosporiinipitoisuuksiin veressä. Siirtyminen Neoralista Sandimmuneen tulee suorittaa tehostetussa seurannassa mahdollisen aliannostuksen välttämiseksi.
Munuaisen, maksan ja sydämen siirto
Nefrotoksisuus
Syklosporiini, Neoralin vaikuttava aine, voi aiheuttaa munuaistoksisuutta ja maksatoksisuutta, kun sitä käytetään suurina annoksina. Ei ole epätavallista, että seerumin kreatiniini- ja BUN-tasot kohoavat siklosporiinihoidon aikana. Nämä nousut munuaisensiirtopotilailla eivät välttämättä tarkoita hylkimistä, ja jokainen potilas on arvioitava täysin ennen annoksen muuttamisen aloittamista.
Sandimmunen oraaliliuoksesta saadun historiallisen kokemuksen perusteella siklosporiiniin liittyvää munuaistoksisuutta on havaittu 25 %:ssa munuaisensiirtotapauksista, 38 %:ssa sydämensiirtotapauksista ja 37 %:ssa maksansiirtotapauksista. Lievä nefrotoksisuus havaittiin yleensä 2–3 kuukautta munuaisensiirron jälkeen, ja se koostui leikkausta edeltävän BUN- ja kreatiniinitason nousun pysähtymisestä syksyllä välillä 35–45 mg/dl ja 2,0–2,5 mg/dl. Nämä nousut johtuivat usein syklosporiinin annoksen pienentämisestä.
Selvempää nefrotoksisuutta havaittiin aikaisin siirron jälkeen, ja sille oli tunnusomaista nopeasti nouseva BUN ja kreatiniini. Koska nämä tapahtumat ovat samanlaisia kuin munuaisten hylkimisjaksot, on huolehdittava niiden erottamisesta. Tämä munuaistoksisuuden muoto reagoi yleensä syklosporiinin annoksen pienentämiseen.
Vaikka erityisiä diagnostisia kriteerejä, jotka luotettavasti erottaisivat munuaissiirteen hylkimisreaktion lääketoksisuudesta, ei ole löydetty, joukko parametrejä on liitetty merkittävästi jompaankumpaan. On kuitenkin huomattava, että jopa 20 %:lla potilaista voi esiintyä samanaikaisesti nefrotoksisuutta ja hylkimisreaktiota.
Syklosporiiniin liittyvän nefropatian muodolle on tunnusomaista jatkuva munuaisten toiminnan heikkeneminen ja morfologiset muutokset munuaisissa. 5–15 % siklosporiinia saaneista elinsiirron saajista ei pysty vähentämään seerumin kreatiniinin nousua huolimatta siklosporiinihoidon vähentämisestä tai lopettamisesta. Näiltä potilailta otetut munuaisbiopsiat osoittavat yhden tai useamman seuraavista muutoksista: tubulusvakuolisaatio, tubulaariset mikrokalkkeumat, peritubulaariset kapillaarit, arteriolopatia ja interstitiaalisen fibroosin raidallinen muoto, johon liittyy tubulusatrofiaa. Vaikka mikään näistä morfologisista muutoksista ei ole täysin spesifinen, syklosporiiniin liittyvän rakenteellisen nefrotoksisuuden diagnoosi vaatii todisteita näistä löydöistä.
Kun tarkastellaan syklosporiiniin liittyvän nefropatian kehittymistä, on huomionarvoista, että useat kirjoittajat ovat raportoineet yhteyden interstitiaalisen fibroosin ilmaantumisen ja suurempien kumulatiivisten annosten tai jatkuvasti korkeiden verenkierrossa olevien syklosporiinipitoisuuksien välillä. Tämä pätee erityisesti ensimmäisten kuuden elinsiirron jälkeisen kuukauden aikana, jolloin annos on yleensä suurin ja kun munuaisten vastaanottajilla elin näyttää olevan haavoittuvimmin syklosporiinin toksisille vaikutuksille. Muita interstitiaalisen fibroosin kehittymiseen vaikuttavia tekijöitä näillä potilailla ovat pitkittynyt perfuusioaika, lämmin iskemiaaika sekä akuutin toksisuuden jaksot sekä akuutti ja krooninen hylkimisreaktio. Interstitiaalisen fibroosin palautuvuutta ja sen korrelaatiota munuaisten toimintaan ei ole vielä määritetty. Arteriolopatian palautumista on raportoitu siklosporiinin käytön lopettamisen tai annoksen pienentämisen jälkeen.
Munuaisten vajaatoiminta milloin tahansa vaatii tarkkaa seurantaa, ja annoksen tiheä muuttaminen voi olla aiheellista.
Vakavan ja hellittämättömän hylkimisreaktion yhteydessä, kun pelastushoito pulssisteroideilla ja monoklonaalisilla vasta-aineilla ei pysty kumoamaan hyljintäjaksoa, saattaa olla parempi vaihtaa vaihtoehtoiseen immunosuppressiiviseen hoitoon sen sijaan, että nostaisi Neoral-annosta liiallisiin veren pitoisuuksiin.
Munuaisten toiminnan additiivisen tai synergistisen vajaatoiminnan mahdollisuuden vuoksi on noudatettava varovaisuutta, kun Neoralia annetaan samanaikaisesti muiden lääkkeiden kanssa, jotka voivat heikentää munuaisten toimintaa (ks. VAROTOIMENPITEET , HUUMEIDEN VUOROVAIKUTUKSET ).
Tromboottinen mikroangiopatia
Joskus potilaille on kehittynyt trombosytopenian ja mikroangiopaattisen hemolyyttisen anemian oireyhtymä, joka voi johtaa siirteen epäonnistumiseen. Vaskulopatia voi ilmaantua ilman hylkimistä, ja siihen liittyy innokas verihiutaleiden kulutus siirteen sisällä, kuten Indium 111 -leimatut verihiutaletutkimukset osoittavat. Tämän oireyhtymän patogeneesi tai hoito ei ole selvä. Vaikka parantuminen on tapahtunut syklosporiinin vähentämisen tai lopettamisen ja 1) streptokinaasin ja hepariinin antamisen tai 2) plasmafereesin jälkeen, tämä näyttää riippuvan varhaisesta havaitsemisesta Indium 111 -merkityillä verihiutalekuvauksilla (ks. HAITTAVAIKUTUKSET ).
Hyperkalemia
Merkittävää hyperkalemiaa (joskus liittyy hyperkloreemiseen metaboliseen asidoosiin) ja hyperurikemiaa on havaittu satunnaisesti yksittäisillä potilailla.
Maksatoksisuus
Syklosporiinilla hoidetuilla potilailla on raportoitu maksatoksisuutta ja maksavaurioita, mukaan lukien kolestaasi, keltaisuus, hepatiitti ja maksan vajaatoiminta. Useimmat ilmoitukset sisälsivät potilaita, joilla oli merkittäviä samanaikaisia sairauksia, perussairauksia ja muita hämmentäviä tekijöitä, mukaan lukien infektiokomplikaatiot ja maksatoksisia lääkkeitä. Joissakin tapauksissa, pääasiassa elinsiirtopotilailla, on raportoitu kuolemaan johtaneita tuloksia (ks HAITTAVAIKUTUKSET , Markkinoinnin jälkeinen kokemus, munuaisten, maksan ja sydämen siirto ).
Maksatoksisuutta, joka ilmenee yleensä maksaentsyymien ja bilirubiinin kohoamisena, raportoitiin kliinisissä tutkimuksissa syklosporiinilla hoidetuilla potilailla: 4 % munuaisensiirrossa, 7 % sydämensiirrossa ja 4 % maksansiirrossa. Tämä havaittiin yleensä ensimmäisen hoitokuukauden aikana, kun käytettiin suuria siklosporiiniannoksia. Kemian nousut yleensä vähenivät annosta pienentämällä.
Pahanlaatuiset kasvaimet
Kuten muitakin immunosuppressantteja saavilla potilailla, siklosporiinia saavilla potilailla on lisääntynyt lymfoomien ja muiden pahanlaatuisten kasvainten, erityisesti ihon, kehittymisen riski. Siklosporiinia käyttäviä potilaita tulee varoittaa välttämään liiallista altistumista ultraviolettivalolle. Suurentunut riski näyttää liittyvän pikemminkin immunosuppression voimakkuuteen ja kestoon kuin tiettyjen aineiden käyttöön. Koska on olemassa vaara, että immuunijärjestelmä heikkenee ja johtaa lisääntyneeseen infektio- tai pahanlaatuisuusriskiin, useita immunosuppressantteja sisältävää hoito-ohjelmaa tulee käyttää varoen. Jotkut pahanlaatuiset kasvaimet voivat olla kohtalokkaita. Elinsiirtopotilailla, jotka saavat siklosporiinia, on suurempi riski saada vakava infektio, joka johtaa kuolemaan.
Vakavat infektiot
Potilailla, jotka saavat immunosuppressantteja, mukaan lukien Neoral 100 mg, on lisääntynyt riski saada bakteeri-, virus-, sieni- ja alkueläininfektiot, mukaan lukien opportunistiset infektiot. Nämä infektiot voivat johtaa vakaviin, mukaan lukien kuolemaan johtaviin seurauksiin (ks LAATIKKO VAROITUS , ja HAITTAVAIKUTUKSET ).
Polyomavirusinfektiot
Potilailla, jotka saavat immunosuppressantteja, mukaan lukien Neoral 100 mg, on lisääntynyt riski saada opportunistisia infektioita, mukaan lukien polyoomavirusinfektiot. Polyomavirusinfektioilla elinsiirtopotilailla voi olla vakavia ja joskus kuolemaan johtavia seurauksia. Näitä ovat JC-virukseen liittyvä progressiivinen multifokaalinen leukoenkefalopatia (PML) ja polyoomavirukseen liittyvä nefropatia (PVAN), jotka johtuvat erityisesti BK-virusinfektiosta, joita on havaittu syklosporiinia saavilla potilailla. PVANiin liittyy vakavia seurauksia, mukaan lukien munuaisten toiminnan heikkeneminen ja munuaissiirteen menetys (ks. HAITTAVAIKUTUKSET , Markkinoinnin jälkeinen kokemus, munuaisten, maksan ja sydämen siirto ). Potilaiden seuranta voi auttaa havaitsemaan PVAN-riskissä olevat potilaat.
PML-tapauksia on raportoitu Neoral-hoitoa saaneilla potilailla. PML, joka on joskus kuolemaan johtava, ilmenee yleensä hemipareesina, apatiana, sekavina, kognitiivisina puutteina ja ataksiana. PML:n riskitekijöitä ovat hoito immunosuppressiivisilla hoidoilla ja immuunitoiminnan heikkeneminen. Immunosuppressoituneiden potilaiden lääkäreiden tulee ottaa huomioon PML erotusdiagnoosissa potilailla, jotka raportoivat neurologisista oireista, ja neurologin konsultaatiota tulee harkita kliinisen aiheen mukaan.
Kokonaisimmunosuppression vähentämistä on harkittava elinsiirtopotilailla, joille kehittyy PML tai PVAN. Vähentynyt immunosuppressio voi kuitenkin vaarantaa siirteen.
Neurotoksisuus
On raportoitu kouristuksia aikuisilla ja lapsipotilailla, jotka ovat saaneet siklosporiinia, erityisesti yhdessä suuriannoksisen metyyliprednisolonin kanssa.
Enkefalopatiaa, mukaan lukien posterior Reversible Encephalopathy Syndrome (PRES), on kuvattu sekä markkinoille tulon jälkeisissä raporteissa että kirjallisuudessa. Ilmeisiä oireita ovat tajunnan heikkeneminen, kouristukset, näköhäiriöt (mukaan lukien sokeus), motoristen toimintojen menetys, liikehäiriöt ja psykiatriset häiriöt. Monissa tapauksissa muutoksia valkoisessa aineessa on havaittu käyttämällä kuvantamistekniikoita ja patologisia näytteitä. Altistavat tekijät, kuten verenpainetauti, hypomagnesemia, hypokolesterolemia, suuriannoksiset kortikosteroidit, korkeat siklosporiinipitoisuudet veressä ja graft-versus-host -sairaus, on havaittu monissa, mutta ei kaikissa raportoiduissa tapauksissa. Muutokset ovat useimmissa tapauksissa olleet palautuvia siklosporiinin käytön lopettamisen jälkeen, ja joissakin tapauksissa havaittiin paranemista annoksen pienentämisen jälkeen. Vaikuttaa siltä, että maksansiirtopotilaat ovat alttiimpia enkefalopatialle kuin ne, jotka saavat munuaisensiirtoa. Toinen harvinainen siklosporiinin aiheuttaman neurotoksisuuden ilmentymä, jota esiintyy elinsiirtopotilailla useammin kuin muissa indikaatioissa, on optisen levyn turvotus, mukaan lukien papilloedeema, johon voi liittyä hyvänlaatuisen kallonsisäisen kohonneen verenpaineen aiheuttamaa näkövammaisuutta.
On noudatettava varovaisuutta käytettäessä siklosporiinia nefrotoksisten lääkkeiden kanssa (ks VAROTOIMENPITEET ).
Nivelreuma
Siklosporiininefropatia havaittiin munuaisbiopsiasta 6:sta 60:stä (10 %) nivelreumapotilaasta keskimääräisen 19 kuukauden hoidon keston jälkeen. Vain yhtä potilasta näistä kuudesta potilaasta hoidettiin annoksella ≤ 4 mg/kg/vrk. Seerumin kreatiniiniarvo parani kaikilla paitsi yhtä potilaalla siklosporiinihoidon lopettamisen jälkeen. "Maksimaalinen kreatiniinin nousu" näyttää olevan tekijä siklosporiininefropatian ennustamisessa.
Syklosporiinilla on mahdollisuus, kuten muidenkin immunosuppressiivisten aineiden kohdalla, lisätä pahanlaatuisten lymfoomien esiintymistä. Ei ole selvää, onko siklosporiinin riski suurempi kuin nivelreumapotilailla tai nivelreumapotilailla, jotka saavat sytotoksista hoitoa tähän käyttöaiheeseen. Viisi lymfoomatapausta havaittiin: neljä noin 2 300 nivelreuman hoitoon syklosporiinilla hoidetun potilaan tutkimuksessa ja toinen lymfoomatapaus raportoitiin kliinisessä tutkimuksessa. Vaikka tässä tutkimuksessa raportoitiin myös muita kasvaimia (12 ihosyöpää, 24 erityyppistä kiinteää kasvainta ja 1 multippeli myelooma), epidemiologiset analyysit eivät tukeneet yhteyttä siklosporiiniin muulla tavalla kuin pahanlaatuisten lymfoomien osalta.
Potilaat tulee arvioida perusteellisesti ennen Neoral 25 mg -hoitoa ja sen aikana pahanlaatuisten kasvainten kehittymisen varalta. Lisäksi Neoral 25 mg -hoidon käyttö muiden immunosuppressiivisten aineiden kanssa voi aiheuttaa liiallista immunosuppressiota, jonka tiedetään lisäävän pahanlaatuisten kasvainten riskiä.
Psoriasis
(Katso myös LAATIKKOINEN VAROITUS psoriaasista )
Koska siklosporiini on voimakas immunosuppressiivinen aine, jolla on useita mahdollisesti vakavia sivuvaikutuksia, Neoral 100 mg:n käytön riskit ja hyödyt tulee harkita ennen psoriaasipotilaiden hoitoa. Syklosporiini, Neoralin vaikuttava aine, voi aiheuttaa munuaistoksisuutta ja kohonnutta verenpainetta (ks VAROTOIMENPITEET ) ja riski kasvaa annoksen ja hoidon keston kasvaessa. Potilaiden, joilla saattaa olla suurentunut riski, kuten potilaiden, joilla on epänormaali munuaisten toiminta, hallitsematon verenpainetauti tai pahanlaatuisia kasvaimia, ei tule antaa Neoralia.
Munuaisten vajaatoiminta on Neoralin mahdollinen seuraus, joten munuaisten toimintaa on seurattava hoidon aikana.
Potilaat, jotka saavat Neoralia 100 mg, tarvitsevat seerumin kreatiniinin säännöllistä seurantaa (ks Erityinen seuranta alla ANNOSTELU JA HALLINNOINTI ). Iäkkäitä potilaita tulee seurata erityisen huolellisesti, koska myös munuaisten toiminta heikkenee iän myötä. Jos potilaita ei valvota kunnolla eikä annosta säädetä oikein, siklosporiinihoito voi aiheuttaa rakenteellisia munuaisvaurioita ja pysyviä munuaisten toimintahäiriöitä.
Seerumin kreatiniini- ja BUN-arvot voivat kohota Neoral 25 mg -hoidon aikana, mikä kuvastaa glomerulusten suodatusnopeuden vähenemistä.
Munuaisbiopsiat 86 psoriaasipotilaalta, joita hoidettiin keskimäärin 23 kuukauden ajan 1,2–7,6 mg/kg/vrk siklosporiinilla, osoittivat merkkejä siklosporiininefropatiasta 18/86:lla (21 %) potilaista. Patologia koostui munuaisten tubulusatrofiasta ja interstitiaalisesta fibroosista. Toistuvassa biopsiassa 13 näistä potilaasta, joita pidettiin eri annoksilla siklosporiinia keskimäärin 2 lisävuotta, syklosporiinin aiheuttamaa nefropatiaa sairastavien määrä nousi 26/86:een (30 %). Suurin osa potilaista (19/26) sai annoksen ≥ 5,0 mg/kg/vrk (suurin suositeltu annos on 4 mg/kg/vrk). Potilaat saivat myös syklosporiinia yli 15 kuukauden ajan (18/26) ja/tai heillä oli kliinisesti merkitsevä seerumin kreatiniinin nousu yli 1 kuukauden ajan (21/26). Kreatiniinitasot palasivat normaalille alueelle 7:llä 11 potilaasta, joilla siklosporiinihoito keskeytettiin.
Ihon ja lymfoproliferatiivisten pahanlaatuisten kasvainten kehittymisen riski on lisääntynyt syklosporiinilla hoidetuilla psoriaasipotilailla. Pahanlaatuisten kasvainten suhteellinen riski on verrattavissa muihin immunosuppressiivisilla aineilla hoidetuilla psoriaasipotilailla havaittuun riskiin.
Kasvaimia raportoitiin kliinisissä tutkimuksissa 32:lla (2,2 %) 1439 psoriaasipotilaasta, joita hoidettiin syklosporiinilla maailmanlaajuisesti. Lisää kasvaimia on raportoitu 7 potilaalla siklosporiinin markkinoille tulon jälkeen. Ihon pahanlaatuisia kasvaimia raportoitiin 16:lla (1,1 %) näistä potilaista; kaikki paitsi kaksi heistä olivat saaneet aiemmin PUVA-hoitoa. Metotreksaattia sai 7 potilasta.
UVB:tä ja kivihiilitervaa oli käyttänyt 2 potilasta ja 3 potilasta. Seitsemällä potilaalla oli joko aiemmin ollut ihosyöpä tai mahdollisesti altistava leesio ennen siklosporiinialtistusta. Ihosyöpää sairastavista 16 potilaasta 11 potilaalla oli 18 okasolusyöpää ja 7 potilaalla 10 tyvisolusyöpää.
Oli kaksi lymfoproliferatiivista pahanlaatuista kasvainta; yksi tapaus non-Hodgkinin lymfoomasta, joka vaati kemoterapiaa, ja yksi mycosis fungoides -tapaus, joka regressi spontaanisti syklosporiinin käytön lopettamisen jälkeen. Hyvänlaatuisia lymfosyyttisiä infiltraatiotapauksia oli neljä: 3 taantui spontaanisti syklosporiinin käytön lopettamisen jälkeen, kun taas neljäs regressi lääkkeen jatkamisesta huolimatta. Loput pahanlaatuisista kasvaimista, 13 tapausta (0,9 %), koskivat eri elimiä.
Potilaita ei tule hoitaa samanaikaisesti siklosporiinilla ja PUVA:lla tai UVB:llä, muulla sädehoidolla tai muilla immunosuppressiivisilla aineilla, koska on mahdollista liiallista immunosuppressiota ja siitä johtuvaa pahanlaatuisten kasvainten riskiä. (katso VASTA-AIHEET ). Potilaita tulee myös varoittaa suojaamaan itseään asianmukaisesti auringossa ollessaan ja välttämään liiallista altistumista auringolle. Potilaat tulee arvioida perusteellisesti ennen hoitoa ja sen aikana pahanlaatuisten kasvainten esiintymisen varalta. Muista, että psoriaattiset plakit voivat peittää pahanlaatuiset leesiot. Psoriaasille epätyypillisistä ihovaurioista tulee ottaa biopsia ennen hoidon aloittamista. Potilaita tulee hoitaa Neoralilla vasta, kun epäilyttävät leesiot ovat hävinneet kokonaan, ja vain, jos muita hoitovaihtoehtoja ei ole (ks. Psoriasispotilaiden erityinen seuranta ).
Erityiset apuaineet
Alkoholi (etanoli)
Alkoholipitoisuus (katso KUVAUS Neoral 100 mg tulee ottaa huomioon, kun sitä annetaan potilaille, joiden alkoholin käyttöä tulee välttää tai minimoida, esim. raskaana oleville tai imettäville naisille, potilaille, joilla on maksasairaus tai epilepsia, alkoholipotilaille tai lapsipotilaille. 70 kg painavalle aikuiselle suurin vuorokausiannos suun kautta antaisi noin 1 gramman alkoholia, mikä on noin 6 % normaalijuoman sisältämästä alkoholimäärästä.
VAROTOIMENPITEET
Kenraali
Hypertensio
Syklosporiini on Neoralin vaikuttava aine. Hypertensio on siklosporiinihoidon yleinen sivuvaikutus, joka voi jatkua (ks HAITTAVAIKUTUKSET ja ANNOSTELU JA HALLINNOINTI seurantasuosituksia varten). Lievää tai kohtalaista verenpainetautia kohdataan useammin kuin vaikeaa verenpainetautia, ja ilmaantuvuus vähenee ajan myötä. Syklosporiinilla hoidettujen munuais-, maksa- ja sydänsiirrännäisten vastaanottajat saattavat tarvita verenpainetta alentavaa hoitoa (ks. Nivelreuman erityisseuranta ja Psoriasispotilaat ). Koska siklosporiini voi kuitenkin aiheuttaa hyperkalemiaa, kaliumia säästäviä diureetteja ei tule käyttää. Vaikka kalsiumantagonistit voivat olla tehokkaita aineita siklosporiiniin liittyvän verenpaineen hoidossa, ne voivat häiritä siklosporiinin aineenvaihduntaa (ks. HUUMEIDEN VUOROVAIKUTUKSET ).
Rokotus
Siklosporiinihoidon aikana rokotus voi olla vähemmän tehokas; ja elävien heikennettyjen rokotteiden käyttöä tulee välttää.
Nivelreumapotilaiden erityisseuranta
Ennen hoidon aloittamista on suoritettava huolellinen fyysinen tutkimus, mukaan lukien verenpainemittaukset (vähintään kahdesti) ja kaksi kreatiniinitasoa lähtötilanteen arvioimiseksi. Verenpaine ja seerumin kreatiniini tulee arvioida 2 viikon välein ensimmäisten 3 kuukauden aikana ja sen jälkeen kuukausittain, jos potilas on vakaa. On suositeltavaa seurata seerumin kreatiniinia ja verenpainetta aina ei-steroidisten tulehduskipulääkkeiden (NSAID) annoksen nostamisen jälkeen ja uuden tulehduskipulääkkeen aloittamisen jälkeen Neoral 25 mg -hoidon aikana. Jos sitä annetaan samanaikaisesti metotreksaatin kanssa, CBC- ja maksan toimintakokeita suositellaan seurattavaksi kuukausittain (ks. VAROTOIMENPITEET , Yleistä, hypertensio ).
Potilailla, jotka saavat siklosporiinia, Neoralin annosta tulee pienentää 25–50 %, jos verenpainetautia ilmaantuu. Jos verenpainetauti jatkuu, Neoral 100 mg -annosta tulee edelleen pienentää tai verenpainetta pitää hallita verenpainetta alentavilla aineilla. Useimmissa tapauksissa verenpaine on palannut lähtötasolle, kun siklosporiinihoito lopetettiin.
Lumekontrolloiduissa nivelreumapotilailla tehdyissä tutkimuksissa systolista hypertensiota (määritelty kahden systolisen verenpainelukeman esiintymisenä > 140 mmHg) ja diastolista verenpainetta (määritelty kahdeksi diastoliseksi verenpainelukemaksi > 90 mmHg) esiintyi 33 %:lla ja 19 %:lla potilaista. siklosporiinilla hoidetuilla potilailla. Vastaavat lumelääkeluvut olivat 22 % ja 8 %.
Psoriasispotilaiden erityinen seuranta
Ennen hoidon aloittamista on suoritettava huolellinen dermatologinen ja fyysinen tutkimus, mukaan lukien verenpainemittaukset (vähintään kaksi kertaa). Koska Neoral on immunosuppressiivinen lääkeaine, potilaiden tulee arvioida piilevän infektion esiintymisen varalta ensimmäisessä fyysisessä tutkimuksessaan ja kasvainten esiintymisen varalta aluksi ja koko Neoral-hoidon ajan. Psoriaasille epätyypillisistä ihovaurioista tulee ottaa biopsia ennen Neoralin aloittamista. Potilaita, joilla on pahanlaatuisia tai pahanlaatuisia ihomuutoksia, tulee hoitaa Neoral 100 mg:lla vasta tällaisten leesioiden asianmukaisen hoidon jälkeen ja jos muuta hoitovaihtoehtoa ei ole.
Peruslaboratorioiden tulisi sisältää seerumin kreatiniini (kahdesti), BUN, CBC, seerumin magnesium, kalium, virtsahappo ja lipidit.
Siklosporiininefropatian riski pienenee, kun aloitusannos on pieni (2,5 mg/kg/vrk), enimmäisannos ei ylitä 4,0 mg/kg/vrk, seerumin kreatiniiniarvoa seurataan säännöllisesti siklosporiinin annon aikana ja Neoral-annos 25 mg:n annos pienenee, kun kreatiniinin nousu on suurempi tai yhtä suuri kuin 25 % potilaan hoitoa edeltävän tason yläpuolella. Kreatiniinin nousu on yleensä palautuvaa, kun Neoralin annosta pienennetään ajoissa tai sen käyttö lopetetaan.
Seerumin kreatiniini- ja BUN-arvot tulee arvioida 2 viikon välein ensimmäisten 3 kuukauden hoidon aikana ja sen jälkeen kuukausittain, jos potilas on vakaa. Jos seerumin kreatiniiniarvo on vähintään 25 % korkeampi kuin potilaan hoitoa edeltävä taso, seerumin kreatiniiniarvo tulee toistaa kahden viikon kuluessa. Jos seerumin kreatiniinin muutos on suurempi tai yhtä suuri kuin 25 % lähtötilanteen yläpuolella, Neoral 25 mg -annosta tulee vähentää 25-50 %. Jos klo milloin vain seerumin kreatiniini kohoaa vähintään 50 % hoitoa edeltävää tasoa korkeammalla, Neoral 25 mg:n annosta tulee vähentää 25-50 %. Neoral-hoito tulee lopettaa, jos seerumin kreatiniinin palautuminen (25 %:n sisällä lähtötasosta) ei ole saavutettavissa kahden annoksen muuttamisen jälkeen. On suositeltavaa seurata seerumin kreatiniinia ei-steroidisen tulehduskipulääkkeen annoksen suurentamisen jälkeen ja uuden ei-steroidisen tulehduskipulääkityksen aloittamisen jälkeen Neoral 25 mg -hoidon aikana.
Verenpaine tulee mitata 2 viikon välein ensimmäisten 3 kuukauden hoidon aikana ja sen jälkeen kuukausittain, jos potilas on vakaa, tai useammin, kun annosta muutetaan. Potilaiden, joilla ei ole aiempaa verenpainetautia ennen Neoral-hoidon aloittamista, lääkettä tulee vähentää 25–50 %, jos heillä todetaan jatkuva verenpaine. Jos potilas jatkaa kohonnutta verenpainetta huolimatta Neoralin 25 mg:n annoksen useista pienennyksistä, Neoral-hoito on lopetettava. Potilaiden, joilla on hoidettu verenpainetauti, ennen Neoral 100 mg -hoidon aloittamista heidän lääkityksensä tulee säätää verenpaineen hallintaan Neoral-hoidon aikana. Neoral 100 mg -hoito tulee lopettaa, jos muutos verenpainetaudin hoidossa ei ole tehokas tai siedettävä.
CBC-arvoja, virtsahappoa, kaliumia, lipidejä ja magnesiumia tulee myös seurata 2 viikon välein 3 ensimmäisen hoitokuukauden ajan ja sen jälkeen kuukausittain, jos potilas on vakaa, tai useammin, kun annosta muutetaan. Neoralin 25 mg:n annosta tulee pienentää 25–50 % kliinistä huolta aiheuttavien poikkeavuuksien varalta.
Kontrolloiduissa siklosporiinitutkimuksissa psoriaasipotilailla siklosporiinipitoisuudet veressä eivät korreloineet hyvin paranemisen tai sivuvaikutusten, kuten munuaisten toimintahäiriön, kanssa.
Laboratoriotestit
Kaikilla syklosporiinilla hoidetuilla potilailla munuaisten ja maksan toiminta on arvioitava toistuvasti mittaamalla seerumin kreatiniini, BUN, seerumin bilirubiini ja maksaentsyymit. Seerumin lipidejä, magnesiumia ja kaliumia tulee myös seurata.
Siklosporiinin veren pitoisuuksia tulee seurata rutiininomaisesti elinsiirtopotilailla (ks ANNOSTELU JA HALLINNOINTI , Veripitoisuuden seuranta elinsiirtopotilailla ), ja sitä seurataan säännöllisesti nivelreumapotilailla.
Karsinogeneesi, mutageneesi ja hedelmällisyyden heikkeneminen
Karsinogeenisuustutkimukset suoritettiin uros- ja naarasrotilla ja hiirillä. 78 viikkoa kestäneessä hiiritutkimuksessa todisteita tilastollisesti merkitsevästä trendistä havaittiin lymfosyyttisten lymfoomien osalta naarailla, ja maksasolukarsinoomien ilmaantuvuus keskiannoksen saaneilla miehillä ylitti merkittävästi kontrolliarvon. 24 kuukautta kestäneessä rottatutkimuksessa haiman saarekesoluadenoomat ylittivät merkittävästi kontrollimäärän pienellä annoksella. Hiirillä ja rotilla tehdyissä tutkimuksissa käytetyt annokset olivat 0,01-0,16 kertaa kliinisen ylläpitoannoksen (6 mg/kg) suuruiset. Maksasolukarsinoomat ja haiman saarekesoluadenoomat eivät olleet annoksesta riippuvaisia. Julkaistut raportit osoittavat, että karvattomien hiirten samanaikainen hoito UV-säteilyllä ja syklosporiinilla tai muilla immunosuppressiivisilla aineilla lyhentää ihokasvaimen muodostumiseen kuluvaa aikaa verrattuna pelkkään UV-säteilytykseen.
Syklosporiini ei ollut mutageeninen asianmukaisissa testijärjestelmissä. Syklosporiinin ei ole havaittu olevan mutageeninen/genotoksinen Ames-testissä, V79-HGPRT-testissä, hiirten ja kiinanhamstereiden mikrotumatestissä, kiinanhamsterin luuytimessä tehdyissä kromosomipoikkeavuustesteissä, hiiren dominanttiletaalimäärityksessä ja DNA-korjauskoe käsiteltyjen hiirten siittiöistä. Äskettäinen tutkimus, jossa analysoitiin sisarkromatidivaihdon (SCE) induktiota syklosporiinilla käyttäen ihmisen lymfosyyttejä in vitro, antoi viitteitä positiivisesta vaikutuksesta (eli SCE:n induktiosta) korkeilla pitoisuuksilla tässä järjestelmässä. Kahdessa julkaistussa tutkimuksessa kanit, jotka altistettiin syklosporiinille kohdussa (10 mg/kg/vrk ihonalaisesti), osoittivat vähentynyttä nefronien määrää, munuaisten hypertrofiaa, systeemistä kohonnutta verenpainetta ja progressiivista munuaisten vajaatoimintaa 35 viikon ikään asti. Raskaana olevilla rotilla, jotka saivat 12 mg/kg/vrk siklosporiinia suonensisäisesti (kaksi kertaa suositeltu suonensisäinen annos ihmiselle), oli sikiöitä, joilla oli lisääntynyt kammioväliseinävaurioiden ilmaantuvuus. Näitä löydöksiä ei ole osoitettu muilla lajeilla, eikä niiden merkitystä ihmisille tunneta.
Uros- ja naarasrotilla tehdyissä tutkimuksissa ei havaittu heikentynyttä hedelmällisyyttä.
Ihon laajalle levinnyt papillomatoosi havaittiin sen jälkeen, kun koiria oli hoidettu kroonisella syklosporiinilla 9-kertaisella psoriaasin alkuannoksella ihmisen 2,5 mg/kg, jolloin annokset ilmaistaan kehon pinta-alan perusteella. Tämä papillomatoosi osoitti spontaanin regression syklosporiinin käytön lopettamisen jälkeen.
Lisääntynyt pahanlaatuisten kasvainten ilmaantuvuus on tunnustettu immunosuppression komplikaatio elinsiirtojen vastaanottajilla ja potilailla, joilla on nivelreuma ja psoriaasi. Yleisimmät kasvaimien muodot ovat non-Hodgkinin lymfooma ja ihokarsinoomat. Pahanlaatuisten kasvainten riski siklosporiinin saajilla on suurempi kuin normaalilla terveellä väestöllä, mutta samanlainen kuin potilailla, jotka saavat muita immunosuppressiivisia hoitoja. Immunosuppression vähentäminen tai lopettaminen voi aiheuttaa leesioiden taantumista.
Psoriaasipotilailla, jotka käyttävät siklosporiinia, on raportoitu pahanlaatuisten kasvainten kehittymistä, erityisesti ihon kasvaimia (ks VAROITUKSET ). Psoriaasille epätyypillisistä ihovaurioista tulee ottaa biopsia ennen siklosporiinihoidon aloittamista. Potilaita, joilla on pahanlaatuisia tai pahanlaatuisia ihomuutoksia, tulee hoitaa siklosporiinilla vasta tällaisten leesioiden asianmukaisen hoidon jälkeen ja jos muuta hoitovaihtoehtoa ei ole.
Raskaus
Eläintutkimukset ovat osoittaneet lisääntymistoksisuutta rotilla ja kaniineilla. Syklosporiini ei antanut näyttöä mutageenisista tai teratogeenisista vaikutuksista tavanomaisissa testijärjestelmissä suun kautta annettuna (rotille enintään 17 mg/kg ja kaneille enintään 30 mg/kg päivässä suun kautta). Haittavaikutuksia havaittiin vain emoille myrkyllisillä annoksilla. lisääntymistutkimuksissa rotilla. Siklosporiinin on osoitettu olevan sikiö- ja sikiötoksinen rotilla ja kaniineilla suun kautta emolle toksisina annoksina. Sikiötoksisuutta havaittiin rotilla 0,8-kertaisella ja kaniineilla 5,4-kertaisella siirrännäisannoksella ihmisillä 6,0 mg/kg, jolloin annoskorjaukset perustuvat kehon pinta-alaan. Siklosporiini oli alkio- ja sikiötoksinen, minkä osoittavat lisääntynyt pre- ja postnataalinen kuolleisuus ja alentunut sikiön paino sekä siihen liittyvä luuston hidastuminen.
Raskaana olevilla naisilla ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia, joten Neoralia ei tule käyttää raskauden aikana, ellei mahdollinen hyöty äidille oikeuttaa sikiölle mahdollisesti aiheutuvaa riskiä.
Raskaana olevilla elinsiirron saajilla, joita hoidetaan immunosuppressiivisilla lääkkeillä, ennenaikaisen synnytyksen riski on suurentunut. Seuraavat tiedot edustavat raportoituja tuloksia 116 raskaudesta naisilla, jotka saivat siklosporiinia raskauden aikana, joista 90 % oli elinsiirtopotilaita ja joista suurin osa sai siklosporiinia koko raskausajan. Ainoat johdonmukaiset poikkeavuusmallit olivat ennenaikainen synnytys (raskausaika 28–36 viikkoa) ja alhainen syntymäpaino raskauden ikään nähden. Sikiön menetyksiä tapahtui kuusitoista. Suurin osa raskauksista (85/100) oli monimutkaista häiriöistä; mukaan lukien preeklampsia, eklampsia, ennenaikainen synnytys, abruptio placentae, oligohydramnion, Rh-yhteensopimattomuus ja sikiön toimintahäiriö. Ennenaikainen synnytys tapahtui 47 %:lla. Seitsemän epämuodostumaa raportoitiin viidellä elinkelpoisella lapsella ja kahdessa sikiön menetystapauksessa. 28 prosenttia vauvoista oli pieniä raskausikään nähden. Vastasyntyneiden komplikaatioita esiintyi 27 %:lla. Siksi Neoralin käytön riskit ja hyödyt raskauden aikana tulee punnita huolellisesti.
Saatavilla on rajoitettu määrä havaintoja kohdussa syklosporiinille altistuneista lapsista, noin 7-vuotiaille asti. Näillä lapsilla munuaisten toiminta ja verenpaine olivat normaaleja.
Äidin ja sikiön välisen vuorovaikutuksen mahdollisen katkeamisen vuoksi Neoralin käytön riski/hyötysuhdetta on punnittava huolellisesti raskauden aikana psoriaasipotilailla ja harkittava vakavasti Neoralin käytön lopettamista.
Neoral 100 mg -valmisteiden alkoholipitoisuus tulee myös ottaa huomioon raskaana olevilla naisilla (ks VAROITUKSET , Erityiset apuaineet ).
Imettävät äidit
Syklosporiinia on rintamaidossa. Koska Neoral 100 mg:n imeväisille saattaa aiheutua vakavia haittavaikutuksia, on päätettävä, lopetetaanko imetys vai lopetetaanko lääke, ottaen huomioon lääkkeen merkitys äidille. Neoral sisältää etanolia. Etanolia on äidinmaidossa samankaltaisina pitoisuuksina kuin äidin seerumissa, ja jos sitä on rintamaidossa, imeväinen imeytyy suun kautta (ks. VAROITUKSET ).
Käyttö lapsille
Vaikka riittäviä ja hyvin kontrolloituja tutkimuksia lapsilla ei ole saatettu päätökseen, alle vuoden ikäiset elinsiirron saajat ovat saaneet Neoralia ilman epätavallisia haittavaikutuksia. Neoral-hoidon turvallisuutta ja tehoa alle 18-vuotiailla lapsilla, joilla on juveniili nivelreuma tai psoriaasi, ei ole varmistettu.
Geriatrinen käyttö
Nivelreumaa koskevissa kliinisissä siklosporiinitutkimuksissa 17,5 % potilaista oli 65-vuotiaita tai vanhempia. Näille potilaille kehittyi todennäköisemmin systolinen hypertensio hoidon aikana, ja seerumin kreatiniinipitoisuus nousi todennäköisemmin ≥ 50 % lähtötason yläpuolelle 3–4 kuukauden hoidon jälkeen.
Neoral 100 mg:n kliinisissä tutkimuksissa elinsiirto- ja psoriaasipotilailla ei ollut riittävästi 65-vuotiaita ja sitä vanhempia koehenkilöitä sen määrittämiseksi, reagoivatko he eri tavalla kuin nuoremmat. Muut raportoidut kliiniset kokemukset eivät ole osoittaneet eroja iäkkäiden ja nuorempien potilaiden vasteessa. Yleensä iäkkään potilaan annoksen valinnassa tulee olla varovainen, yleensä alkaen annosalueen alimmasta päästä, mikä heijastaa maksan, munuaisten tai sydämen toiminnan heikkenemisen sekä samanaikaisen sairauden tai muun lääkehoidon yleisyyttä.
YLIANNOSTUS
Siklosporiinin yliannostuksesta on vähän kokemusta. Pakkooksentelu ja mahahuuhtelu voivat olla hyödyllisiä jopa 2 tuntia Neoralin annon jälkeen. Ohimenevää maksatoksisuutta ja munuaistoksisuutta voi esiintyä, minkä pitäisi hävitä lääkkeen lopettamisen jälkeen. Suun kautta annetut siklosporiiniannokset 10 g:aan asti (noin 150 mg/kg) on siedetty suhteellisen vähäisin kliinisin seurauksin, kuten oksentelun, uneliaisuuden, päänsäryn, takykardian ja muutamilla potilailla kohtalaisen vaikean, palautuvan munuaisten toiminnan heikkenemisen kanssa. Vakavia myrkytysoireita on kuitenkin raportoitu siklosporiinin vahingossa tapahtuneen parenteraalisen yliannostuksen jälkeen keskosilla. Yleisiä tukitoimenpiteitä ja oireenmukaista hoitoa tulee noudattaa kaikissa yliannostustapauksissa. Siklosporiini ei ole suuressa määrin dialysoitavissa, eikä se poistu hyvin hiiliverfuusiolla. Suun kautta otettava annos, jolla puolet koe-eläimistä kuolee, on 31-kertainen, 39-kertainen ja >54-kertainen ihmisen elinsiirtopotilaiden ylläpitoannos (6 mg/kg; korjaukset kehon pinta-alan perusteella) hiirillä, rotilla ja kaniineilla. .
VASTA-AIHEET
Kenraali
Neoral 100 mg on vasta-aiheinen potilaille, jotka ovat yliherkkiä siklosporiinille tai jollekin valmisteen aineosalle.
Nivelreuma
Nivelreumapotilaiden, joilla on epänormaali munuaisten toiminta, hallitsematon verenpainetauti tai pahanlaatuisia kasvaimia, ei tule käyttää Neoralia.
Psoriasis
Psoriaasipotilaat, joita hoidetaan Neoral 100 mg:lla, eivät saa saada samanaikaisesti PUVA- tai UVB-hoitoa, metotreksaattia tai muita immunosuppressiivisia aineita, kivihiilitervaa tai sädehoitoa. Psoriaasipotilaiden, joilla on epänormaali munuaisten toiminta, hallitsematon verenpainetauti tai pahanlaatuisia kasvaimia, ei tule käyttää Neoralia.
KLIININEN FARMAKOLOGIA
Syklosporiini on voimakas immunosuppressiivinen aine, joka pidentää eläimillä ihon, munuaisten, maksan, sydämen, haiman, luuytimen, ohutsuolen ja keuhkojen allogeenisten siirteiden selviytymistä. Syklosporiinin on osoitettu tukahduttavan tiettyä humoraalista immuniteettia ja suuremmassa määrin soluvälitteisiä immuunireaktioita, kuten allograftin hylkimistä, viivästynyttä yliherkkyyttä, kokeellista allergista enkefalomyeliittiä, Freundin adjuvanttiniveltulehdusta ja graft versus host -sairautta monissa eläinlajeissa useissa eri elimissä. .
Siklosporiinin tehokkuus johtuu immunokompetenttien lymfosyyttien spesifisestä ja palautuvasta estämisestä solusyklin G0- ja G1-vaiheessa. T-lymfosyytit estetään ensisijaisesti. T-auttajasolu on pääkohde, vaikka Tsuppressorisolu voidaan myös tukahduttaa. Syklosporiini estää myös lymfokiinien tuotantoa ja vapautumista, mukaan lukien interleukiini-2.
Eläimillä ei ole havaittu vaikutuksia fagosyyttitoimintoihin (muutoksia entsyymierityksessä, granulosyyttien kemotaktista migraatiota, makrofagien migraatiota, hiilen puhdistumaa in vivo). Siklosporiini ei aiheuta luuytimen suppressiota eläinmalleilla tai ihmisillä.
Farmakokinetiikka
Siklosporiinin immunosuppressiivinen vaikutus johtuu ensisijaisesti emolääkkeestä. Suun kautta annetun siklosporiinin imeytyminen on epätäydellistä. Siklosporiinin imeytymisaste riippuu yksittäisestä potilaasta, potilaspopulaatiosta ja formulaatiosta. Siklosporiinin eliminaatio tapahtuu pääasiassa sapen kautta, ja vain 6 % annoksesta (emolääke ja metaboliitit) erittyy virtsaan. Siklosporiinin jakautuminen verestä on yleensä kaksivaiheinen, ja sen terminaalinen puoliintumisaika on noin 8,4 tuntia (vaihteluväli 5-18 tuntia). Laskimonsisäisen annon jälkeen siklosporiinin verenpuhdistuma (määritys: HPLC) on noin 5-7 ml/min/kg aikuisilla munuais- tai maksasiirteen vastaanottajilla. Syklosporiinin puhdistuma veressä näyttää olevan hieman hitaampi sydämensiirtopotilailla.
Neoral Soft Gelatin Capsules (syklosporiinikapselit, USP) MODIFIED ja Neoral Oral Solution (syklosporiini oraaliliuos, USP) MODIFIED ovat bioekvivalentteja. Appelsiinimehulla tai omenamehulla laimennettu Neoral 25 mg oraaliliuos on bioekvivalentti vedellä laimennettua Neoral oraaliliuosta. Maidon vaikutusta siklosporiinin biologiseen hyötyosuuteen, kun sitä annetaan Neoral-oraaliliuoksena, ei ole arvioitu.
Annetun annoksen ja altistuksen välinen suhde (pitoisuus-aikakäyrän alla oleva pinta-ala, AUC) on lineaarinen terapeuttisella annosalueella. Siklosporiinialtistuksen (AUC) yksilöiden välinen vaihtelu (kokonais-, %CV) Neoralia tai Sandimmunea annettaessa vaihtelee noin 20–50 % munuaisensiirtopotilailla. Tämä yksilöiden välinen vaihtelu edistää osaltaan tarvetta yksilöidä annostusohjelma optimaalisen hoidon saavuttamiseksi (ks. ANNOSTELU JA HALLINNOINTI ).
AUC:n yksilönsisäinen vaihtelu munuaisensiirtopotilailla (%CV) oli 9-21 % Neoral-valmisteella ja 19-26 % Sandimmunella. Samoissa tutkimuksissa pienimpien pitoisuuksien (%CV) yksilöiden välinen vaihtelu oli 17-30 % Neoral-valmisteella ja 16-38 % Sandimmunella.
Imeytyminen
Neoral on parantanut biologista hyötyosuutta Sandimmuneen verrattuna. Sandimmunena annetun siklosporiinin absoluuttinen hyötyosuus riippuu potilaspopulaatiosta, ja sen arvioidaan olevan alle 10 % maksansiirtopotilailla ja jopa 89 % joillakin munuaisensiirtopotilailla. Neoralina annetun siklosporiinin absoluuttista biologista hyötyosuutta ei ole määritetty aikuisilla. Munuaisensiirto-, nivelreuma- ja psoriaasipotilailla tehdyissä tutkimuksissa siklosporiinin keskimääräinen AUC oli noin 20–50 % suurempi ja veren siklosporiinin huippupitoisuus Cmax oli noin 40–106 % suurempi Neoral 100 mg:n annon jälkeen verrattuna Sandimmunen annon jälkeen. . Annoksen normalisoitu AUC de novo maksansiirtopotilailla, joille annettiin Neoralia 28 päivää siirron jälkeen, oli 50 % suurempi ja Cmax oli 90 % suurempi kuin potilailla, joille annettiin Sandimmunea. AUC ja Cmax ovat myös suurentuneet (Neoral verrattuna Sandimmuneen) sydämensiirtopotilailla, mutta tiedot ovat hyvin rajalliset. Vaikka Neoral 100 mg:n AUC- ja Cmax-arvot ovat korkeammat verrattuna Sandimmuneen, annosta edeltävät alhaisimmat pitoisuudet (annosnormalisoitu) ovat samanlaiset molemmilla valmisteilla.
Neoralin oraalisen annon jälkeen aika veren siklosporiinin huippupitoisuuksien saavuttamiseen (Tmax) oli 1,5–2,0 tuntia. Ruoan antaminen Neoral 25 mg:n kanssa pienentää siklosporiinin AUC- ja Cmax-arvoja. Runsasrasvainen ateria (669 kcal, 45 grammaa rasvaa), joka nautittiin puolen tunnin sisällä ennen Neoralin 25 mg:n antoa, pienensi AUC-arvoa 13 % ja Cmax-arvoa 33 %. Vähärasvaisen aterian (667 kcal, 15 grammaa rasvaa) vaikutukset olivat samanlaiset.
Sappien T-putken ohjautumisen vaikutusta Neoral 25 mg:n syklosporiinin imeytymiseen tutkittiin 11 de novo maksansiirtopotilaalla. Kun potilaille annettiin Neoralia sapen T-putken ohjauksen kanssa ja ilman, havaittiin hyvin vähän eroa imeytymisessä mitattuna siklosporiinin maksimaalisten veren pitoisuuksien muutoksella ennen annostusta olevista arvoista T-letkun ollessa suljettuna verrattuna siihen, jolloin se oli suljettu. auki: 6,9 ± 41 % (vaihteluväli 55 % - 68 %).
PotilaspopulaatioJakelu
Siklosporiini jakautuu suurelta osin veritilavuuden ulkopuolelle. Vakaan tilan jakautumistilavuuden suonensisäisen annostelun aikana on raportoitu olevan 3–5 l/kg kiinteän elinsiirron saaneilla. Veressä jakautuminen on pitoisuudesta riippuvaista. Noin 33-47 % on plasmassa, 4-9 % lymfosyyteissä, 5-12 % granulosyyteissä ja 41-58 % erytrosyyteissä. Suurilla pitoisuuksilla leukosyyttien ja punasolujen sitoutumiskyky kyllästyy. Plasmassa noin 90 % sitoutuu proteiineihin, pääasiassa lipoproteiineihin. Siklosporiini erittyy äidinmaitoon (ks VAROTOIMENPITEET , Imettävät äidit ).
Aineenvaihdunta
Syklosporiini metaboloituu laajasti sytokromi P-450 3A -entsyymijärjestelmän toimesta maksassa ja vähäisemmässä määrin maha-suolikanavassa ja munuaisissa. Syklosporiinin metaboliaa voidaan muuttaa antamalla samanaikaisesti useita eri aineita (ks VAROTOIMENPITEET , HUUMEIDEN VUOROVAIKUTUKSET ). Ihmisen sapesta, ulosteesta, verestä ja virtsasta on tunnistettu ainakin 25 metaboliittia. Metaboliittien biologinen aktiivisuus ja niiden vaikutus toksisuuteen ovat huomattavasti pienemmät kuin emoyhdisteen. Tärkeimmät metaboliitit (M1, M9 ja M4N) syntyvät hapettumisesta 1-beeta-, 9-gamma- ja 4-N-demetyloituneissa asemissa. Vakaassa tilassa Sandimmunen oraalisen annon jälkeen veren M1-, M9- ja M4N-pitoisuuksien keskimääräiset AUC-arvot ovat noin 70 %, 21 % ja 7,5 % veren siklosporiinipitoisuuksien AUC-arvosta. Vakaiden munuaisensiirtopotilaiden (13 potilasta, joille annettiin Neoralia ja Sandimmunea crossover-tutkimuksessa) ja de novo maksansiirtopotilaiden (4 Neoralia 100 mg, 3 Sandimmunea) sappipitoisuuksiin perustuvat tiedot, annoksen prosenttiosuus M1-, M9- ja M4N-metaboliitit ovat samanlaisia käytettäessä joko Neoralia 25 mg tai Sandimmunea.
Erittyminen
Vain 0,1 % siklosporiiniannoksesta erittyy muuttumattomana virtsaan. Eliminaatio tapahtuu pääasiassa sapen kautta, ja vain 6 % annoksesta (emolääke ja metaboliitit) erittyy virtsaan. Dialyysi tai munuaisten vajaatoiminta eivät muuta siklosporiinin puhdistumaa merkittävästi.
Huumeiden vuorovaikutukset
(Katso VAROTOIMENPITEET , HUUMEIDEN VUOROVAIKUTUKSET ) Kun diklofenaakkia tai metotreksaattia annettiin samanaikaisesti siklosporiinin kanssa nivelreumapotilaille, kummankin diklofenaakin ja metotreksaatin AUC suureni merkittävästi (ks. VAROTOIMENPITEET , HUUMEIDEN VUOROVAIKUTUKSET ). Siklosporiinin ja aspiriinin, ketoprofeenin, piroksikaamin tai indometasiinin välillä ei esiintynyt kliinisesti merkittäviä farmakokineettisiä yhteisvaikutuksia.
Tietyt populaatiot
Munuaisten vajaatoiminta
Neljälle loppuvaiheen munuaissairaus (kreatiniinipuhdistuma
Maksan vajaatoiminta
Syklosporiini metaboloituu laajalti maksassa. Koska vaikea maksan vajaatoiminta voi suurentaa merkittävästi siklosporiinialtistusta, siklosporiinin annosta on ehkä pienennettävä näillä potilailla.
Lasten väestö
Neoralia tai Sandimmunea saaneiden lapsipotilaiden farmakokineettiset tiedot ovat hyvin rajallisia. 15 3–16-vuotiaalla munuaisensiirtopotilaalla siklosporiinin kokoveren puhdistuma Sandimmunen laskimonsisäisen annon jälkeen oli 10,6 ± 3,7 ml/min/kg (määritys: Cyclo-trac-spesifinen RIA). Tutkimuksessa, johon osallistui 7 2–16-vuotiasta munuaisensiirtopotilasta, siklosporiinin puhdistuma vaihteli välillä 9,8–15,5 ml/min/kg. Yhdeksällä 0,6–5,6-vuotiaalla maksansiirtopotilaalla puhdistuma oli 9,3 ± 5,4 ml/min/kg (määritys: HPLC).
Lapsiväestössä Neoralilla on myös parempi hyötyosuus Sandimmuneen verrattuna. Seitsemällä de novo maksansiirtopotilaalla, iältään 1,4–10 vuotta, Neoralin absoluuttinen hyötyosuus oli 43 % (vaihteluväli 30–68 %) ja Sandimmunen absoluuttinen hyötyosuus samoilla henkilöillä oli 28 % (vaihteluväli 17–42 %).
Geriatrinen väestö
Normaalien iäkkäiden vapaaehtoisten (N = 18, keski-ikä 69 vuotta) ja iäkkäiden nivelreumapotilaiden (N = 16, keski-ikä 68 vuotta) kerta-annostietojen vertailu nuorten aikuisten vapaaehtoisten kerta-annostietoihin (N = 16, keski-ikä) 26 vuotta) ei osoittanut merkitsevää eroa farmakokineettisissä parametreissa.
Kliiniset tutkimukset
Nivelreuma
Sandimmunen ja Neoral 100 mg:n tehokkuutta vaikean nivelreuman hoidossa arvioitiin viidessä kliinisessä tutkimuksessa, joihin osallistui yhteensä 728 siklosporiinilla hoidettua potilasta ja 273 lumelääkettä.
Yhteenveto tuloksista esitetään hoitoryhmäkohtaisista "vastevastaajista". Vastaaja määritellään potilaaksi, joka on suorittanut tutkimuksen 20 % parantuneella arkistossa ja turvonneiden nivelten määrässä ja 20 % parantuneessa kahdessa 4 tutkijan globaalista, potilaan globaalista, vammaisuudesta ja erytrosyyttien sedimentaatiosta (ESR) tutkimuksissa 651 ja 652 ja 3/5 tutkijan globaalista, potilaan globaalista, vammaisuudesta, visuaalista analogista kipua ja ESR:stä tutkimuksissa 2008, 654 ja 302.
Tutkimukseen 651 otettiin mukaan 264 aktiivista nivelreumaa sairastavaa potilasta, joilla oli vähintään 20 niveltä ja jotka eivät olleet tehonneet vähintään yhteen pääasialliseen nivelreumalääkkeeseen. Tutkimukseen otettiin 3:3:2 satunnaistaminen johonkin seuraavista kolmesta ryhmästä: (1) siklosporiinia 2,5 5 mg/kg/vrk, (2) metotreksaatti 7,5-15 mg/viikko tai (3) lumelääke. Hoidon kesto oli 24 viikkoa. Keskimääräinen siklosporiiniannos viimeisellä käynnillä oli 3,1 mg/kg/vrk. Katso alla oleva kaavio.
Tutkimukseen 652 otettiin mukaan 250 aktiivista nivelreumaa sairastavaa potilasta, joilla oli > 6 aktiivista kivuliasta tai arat niveltä ja jotka eivät olleet tehonneet vähintään yhden suuren nivelreumalääkkeen kanssa. Potilaat satunnaistettiin 3:3:2 satunnaistuksen avulla yhteen kolmesta hoitohaarasta: (1) 1,5 - 5 mg/kg/vrk siklosporiinia, (2) 2,5-5 mg/kg/vrk syklosporiinia ja (3) plasebo. Hoidon kesto oli 16 viikkoa. Keskimääräinen syklosporiiniannos ryhmälle 2 viimeisellä käynnillä oli 2,92 mg/kg/vrk. Katso alla oleva kaavio.
Tutkimukseen 2008 otettiin mukaan 144 potilasta, joilla oli aktiivinen nivelreuma ja > 6 aktiivista niveltä ja joiden aspiriini- ja kulta- tai penisillamiinihoitojaksot olivat epäonnistuneet. Potilaat satunnaistettiin yhteen kahdesta hoitoryhmästä (1) siklosporiini 2,5 - 5 mg/kg/vrk mukauttamalla ensimmäisen kuukauden jälkeen alimman tavoitetason saavuttamiseksi ja (2) lumelääkettä. Hoidon kesto oli 24 viikkoa. Keskimääräinen siklosporiiniannos viimeisellä käynnillä oli 3,63 mg/kg/vrk. Katso alla oleva kaavio.
Tutkimukseen 654 osallistui 148 potilasta, joiden aktiivisten nivelten määrä oli 6 tai enemmän huolimatta hoidosta maksimaalisilla siedetyillä metotreksaattiannoksilla vähintään kolmen kuukauden ajan. Potilaat jatkoivat nykyisen metotreksaattiannoksensa ottamista ja satunnaistettiin saamaan lisäksi jotakin seuraavista lääkkeistä: (1) siklosporiini 2,5 mg/kg/vrk, annosta nostettuna 0,5 mg/kg/vrk viikoilla 2 ja 4, jos ei ollut näyttöä toksisuudesta ja 0,5 mg/kg/vrk lisäys viikoilla 8 ja 16, jos aktiivisten nivelten määrä väheni
Tutkimukseen 302 otettiin mukaan 299 potilasta, joilla oli vaikea aktiivinen nivelreuma ja joista 99 % ei reagoinut tai eivät sietäneet vähintään yhtä aikaisempaa vakavaa nivelreumalääkettä. Potilaat satunnaistettiin yhteen kahdesta hoitoryhmästä (1) Neoral 25 mg ja (2) syklosporiini, jotka molemmat aloitettiin annoksella 2,5 mg/kg/vrk ja tehottomuutta nostettiin 4 viikon kuluttua 0,5 mg/kg/vrk lisäyksillä enintään 5 mg/kg/vrk ja alennetaan milloin tahansa toksisuuden vuoksi. Hoidon kesto oli 24 viikkoa. Keskimääräinen siklosporiiniannos viimeisellä käynnillä oli 2,91 mg/kg/vrk (vaihteluväli: 0,72-5,17) Neoral-valmisteella ja 3,27 mg/kg/vrk (vaihteluväli: 0,73-5,68) siklosporiinilla. Katso alla oleva kaavio.
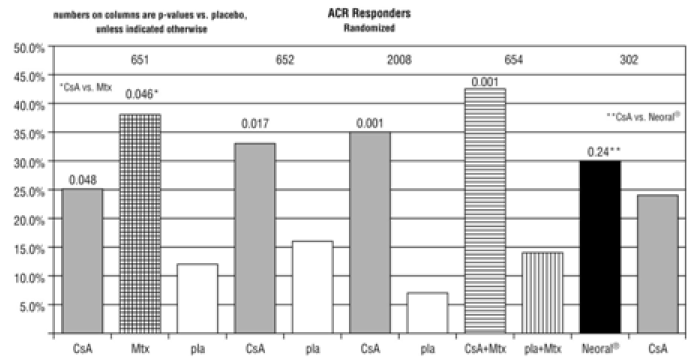
Kliiniset tutkimukset
Kontrolloiduissa tutkimuksissa 493 Neoral-hoitoa saaneella elinsiirtopotilaalla havaittujen haittavaikutusten luonne, vakavuus ja ilmaantuvuus olivat verrattavissa niihin, jotka havaittiin 208 elinsiirtopotilaalla, jotka saivat Sandimmunea näissä samoissa tutkimuksissa, kun näiden kahden lääkkeen annosta muutettiin. saavuttaakseen samat siklosporiinin vähimmäispitoisuudet veressä.
Sandimmunesta saadun historiallisen kokemuksen perusteella seuraavia reaktioita esiintyi vähintään 3 %:lla 892 potilaasta, jotka osallistuivat kliinisiin munuais-, sydän- ja maksansiirtotutkimuksiin.
Kliinisissä tutkimuksissa siklosporiinioraaliliuoksella (Sandimmune) hoidetuista 705 munuaisensiirtopotilaasta syy hoidon keskeyttämiseen oli munuaistoksisuus 5,4 %:lla, infektio 0,9 %:lla, tehon puute 1,4 %:lla, akuutti tubulusnekroosi 1,0 %:lla, lymfoproliferatiiviset häiriöt. 0,3 %:lla potilaista, kohonnut verenpaine 0,3 % ja muut syyt 0,7 %:lla potilaista.
Seuraavia reaktioita esiintyi korkeintaan 2 %:lla siklosporiinilla hoidetuista potilaista: allergiset reaktiot, anemia, anoreksia, sekavuus, sidekalvotulehdus, turvotus, kuume, hauraat kynnet, gastriitti, kuulon heikkeneminen, hikka, hyperglykemia, migreeni (Neoral), lihaskipu, peptinen haava, trombosytopenia, tinnitus.
Seuraavia reaktioita esiintyi harvoin: ahdistuneisuus, rintakipu, ummetus, masennus, hiusten katkeilu, hematuria, nivelkipu, uneliaisuus, suun haavaumat, sydäninfarkti, yöhikoilu, haimatulehdus, kutina, nielemisvaikeudet, pistely, ylemmän ruoansulatuskanavan verenvuoto, näköhäiriöt, heikkous, laihtuminen.
Potilailla, jotka saavat immunosuppressiivisia hoitoja, mukaan lukien siklosporiinia ja siklosporiinia sisältävät hoito-ohjelmat, on lisääntynyt infektioiden (virus-, bakteeri-, sieni-, lois-) riski. Sekä yleistyneitä että paikallisia infektioita voi esiintyä. Myös olemassa olevat infektiot voivat pahentua. Kuolemaan johtaneita seurauksia on raportoitu (ks VAROITUKSET ).
Markkinoinnin jälkeinen kokemus, munuaisten, maksan ja sydämen siirto
Maksatoksisuus
Maksatoksisuus ja maksavaurio, mukaan lukien kolestaasi, keltaisuus, hepatiitti ja maksan vajaatoiminta; vakavia ja/tai kuolemaan johtaneita seurauksia on raportoitu (ks VAROITUKSET , Maksatoksisuus ).
Lisääntynyt infektioriski
JC-virukseen liittyvän progressiivisen multifokaalisen leukoenkefalopatian (PML) tapaukset, joskus kuolemaan johtavat; ja polyoomavirukseen liittyvää nefropatiaa (PVAN), erityisesti BK-virusta, joka johtaa siirteen menettämiseen, on raportoitu (ks. VAROITUKSET , Polyomavirusinfektio ).
Päänsärky, mukaan lukien migreeni
Migreenitapauksia on raportoitu. Joissakin tapauksissa potilaat eivät ole pystyneet jatkamaan siklosporiinin käyttöä, mutta lopullisen päätöksen hoidon keskeyttämisestä tekee hoitava lääkäri arvioituaan huolellisesti hyödyt ja riskit.
Alaraajojen kipu
Yksittäisiä tapauksia alaraajojen kipuista on raportoitu syklosporiinin käytön yhteydessä. Alaraajojen kipua on myös havaittu osana kalsineuriini-inhibiittoreiden aiheuttamaa kipuoireyhtymää (CIPS), kuten kirjallisuudessa on kuvattu.
Nivelreuma
Tärkeimmät siklosporiinin käyttöön liittyvät haittavaikutukset nivelreumassa ovat munuaisten vajaatoiminta (ks. VAROITUKSET ), verenpainetauti (ks VAROTOIMENPITEET ), päänsärky, ruoansulatuskanavan häiriöt ja hirsutismi/hypertrichoosi.
Nivelreumapotilailla, joita hoidettiin kliinisissä tutkimuksissa suositellulla annosalueella, siklosporiinihoito keskeytettiin 5,3 %:lla potilaista kohonneen verenpaineen vuoksi ja 7 %:lla potilaista kohonneen kreatiniinin vuoksi. Nämä muutokset ovat yleensä palautuvia, kun annosta pienennetään ajoissa tai lääke lopetetaan. Seerumin kreatiniinipitoisuuden nousun esiintymistiheys ja vakavuus lisääntyvät siklosporiinihoidon annoksen ja keston myötä. Nämä nousut tulevat todennäköisesti selvemmiksi ilman annoksen pienentämistä tai hoidon lopettamista.
Seuraavia haittavaikutuksia esiintyi kontrolloiduissa kliinisissä tutkimuksissa:
Lisäksi seuraavia haittavaikutuksia on raportoitu kontrolloiduissa kliinisissä tutkimuksissa 1 % -
Autonominen hermosto: suun kuivuminen, lisääntynyt hikoilu
Keho kokonaisuutena: allergia, voimattomuus, kuumat aallot, huonovointisuus, yliannostus, toimenpide NOS*, kasvain NOS*, painon lasku, painon nousu
Sydän: epänormaalit sydämen äänet, sydämen vajaatoiminta, sydäninfarkti, perifeerinen iskemia
Keskus- ja ääreishermosto: hypoestesia, neuropatia, huimaus
Endokriiniset: struuma
Ruoansulatuskanava: ummetus, dysfagia, enanteema, eryktaatio, ruokatorven tulehdus, mahahaava, gastriitti, gastroenteriitti, ienverenvuoto, glossiitti, peptinen haava, sylkirauhasten suureneminen, kielen häiriö, hammassairaus
Infektio: paise, bakteeri-infektio, selluliitti, follikuliitti, sieni-infektio, herpes simplex, herpes zoster, munuaisten paise, moniliaasi, tonsilliitti, virusinfektio
Hematologinen: anemia, nenäverenvuoto, leukopenia, lymfadenopatia
Maksa ja sappijärjestelmä: bilirubinemia
Aineenvaihdunta ja ravitsemus: diabetes mellitus, hyperkalemia, hyperurikemia, hypoglykemia
Tuki- ja liikuntaelimistö: nivelsärky, luunmurtuma, bursiitti, nivelten sijoiltaanmeno, lihaskipu, jäykkyys, nivelkysta, jännehäiriö
Kasvaimet: rintojen fibroadenoosi, syöpä
Psykiatrinen: ahdistuneisuus, sekavuus, heikentynyt libido, emotionaalinen labilisuus, keskittymiskyvyn heikkeneminen, lisääntynyt libido, hermostuneisuus, paroniria, uneliaisuus
Lisääntyminen (naaras): rintakipu, kohdun verenvuoto
Hengitysjärjestelmä: epänormaalit rintaäänet, bronkospasmi
Iho ja lisäkkeet: epänormaali pigmentaatio, angioödeema, dermatiitti, kuiva iho, ekseema, kynsisairaus, kutina, ihosairaus, urtikaria
Erityiset aistit: epänormaali näkö, kaihi, sidekalvotulehdus, kuurous, silmäkipu, makuaistin vääristyminen, tinnitus, vestibulaarihäiriö
Virtsajärjestelmä: epänormaali virtsa, hematuria, lisääntynyt BUN, virtsaamispakko, nokturia, polyuria, pyelonefriitti, virtsankarkailu
*NOS = Ei muuten määritetty
Psoriasis
Tärkeimmät siklosporiinin käyttöön liittyvät haittavaikutukset psoriaasipotilailla ovat munuaisten vajaatoiminta, päänsärky, kohonnut verenpaine, hypertriglyseridemia, hirsutismi/hypertrichoosi, parestesia tai hyperestesia, influenssan kaltaiset oireet, pahoinvointi/oksentelu, ripuli, vatsakivut ja tuki- ja liikuntaelinten letargia, letargia tai nivelkipuja.
Psoriaasipotilailla, joita hoidettiin US-kontrolloiduissa kliinisissä tutkimuksissa suositellulla annosalueella, siklosporiinihoito keskeytettiin 1,0 %:lla potilaista kohonneen verenpaineen vuoksi ja 5,4 %:lla potilaista kohonneen kreatiniinin vuoksi. Useimmissa tapauksissa nämä muutokset olivat palautuvia siklosporiiniannoksen pienentämisen tai lopettamisen jälkeen.
Syklosporiinin käyttöön psoriaasissa on raportoitu yksi kuolema. 27-vuotiaalle miehelle kehittyi munuaisten vajaatoiminta, ja hänelle jatkettiin siklosporiinihoitoa. Hänellä oli progressiivinen munuaisten vajaatoiminta, joka johti kuolemaan.
Seerumin kreatiniinipitoisuuden esiintymistiheys ja vakavuus lisääntyvät siklosporiinihoidon annoksen ja keston myötä. Nämä nousut tulevat todennäköisesti voimakkaammiksi ja voivat johtaa peruuttamattomiin munuaisvaurioihin ilman annoksen pienentämistä tai hoidon lopettamista.
Seuraavia tapahtumia esiintyi 1 % - alle 3 %:lla siklosporiinilla hoidetuista psoriasispotilaista:
Keho kokonaisuutena: kuume, aallot, kuumat aallot
Sydän: rintakipu
Keskus- ja ääreishermosto: ruokahalun lisääntyminen, unettomuus, huimaus, hermostuneisuus, huimaus
Ruoansulatuskanava: vatsan turvotus, ummetus, ienverenvuoto
Maksa ja sappijärjestelmä: hyperbilirubinemia
Kasvaimet: ihon pahanlaatuiset kasvaimet [soumasolusyöpä (0,9 %) ja tyvisolusyöpä (0,4 %)]
Retikuloendoteliaalinen: verihiutaleiden, verenvuoto- ja hyytymishäiriöt, punasolujen häiriöt
Hengitys: infektiot, virus- ja muut infektiot
Iho ja lisäkkeet: akne, follikuliitti, keratoosi, kutina, ihottuma, kuiva iho
Virtsajärjestelmä: virtsaamistaajuus
Näkemys: epänormaali näkö
Lievää hypomagnesemiaa ja hyperkalemiaa saattaa esiintyä, mutta ne ovat oireettomia. Virtsahapon määrä voi lisääntyä, ja kihtikohtauksia on raportoitu harvoin. Lievä ja annoksesta riippuvainen hyperbilirubinemia on havaittu ilman hepatosellulaarisia vaurioita. Siklosporiinihoitoon saattaa liittyä seerumin triglyseridi- tai kolesterolipitoisuuden lievä nousu. Triglyseridien nousua (> 750 mg/dl) esiintyy noin 15 %:lla psoriaasipotilaista; kolesterolin nousua (> 300 mg/dl) havaitaan alle 3 %:lla psoriaasipotilaista. Yleensä nämä laboratorioarvojen poikkeamat palautuvat, kun annosta pienennetään tai siklosporiinihoito lopetetaan.
Markkinoinnin jälkeinen kokemus, psoriaasi
Potilailla, joilla on krooninen läiskäpsoriaasi, on raportoitu tapauksia, jotka muuttuvat erytrodermiseen psoriaasiksi tai yleistyneeksi märkärakkulaiseksi psoriaasiksi joko siklosporiinin lopettamisen tai vähentämisen jälkeen.
POTILASTIEDOT
Potilaita tulee neuvoa, että kaikki siklosporiinin valmisteen muuttaminen tulee tehdä varoen ja vain lääkärin valvonnassa, koska se voi johtaa annoksen muuttamisen tarpeeseen.
Potilaille tulee kertoa toistuvien laboratoriotutkimusten tarpeesta, kun he saavat siklosporiinia. Potilaita tulee kertoa mahdollisista riskeistä raskauden aikana ja neoplasian lisääntyneestä riskistä. Potilaille tulee myös kertoa kohonneen verenpaineen ja munuaisten vajaatoiminnan riskistä.
Potilaita tulee kertoa, että siklosporiinihoidon aikana rokotus voi olla vähemmän tehokas ja elävien heikennettyjen rokotteiden käyttöä tulee välttää.
Potilaille tulee antaa tarkat annostusohjeet. Neoral-oraaliliuos (syklosporiinioraaliliuos, USP) MODIFIED tulee laimentaa, mieluiten appelsiini- tai omenamehulla, joka on huoneenlämpötilassa. Neoral Oral Solution (syklosporiini oraaliliuos, USP) yhdistelmä maidon kanssa voi olla epämiellyttävää.
Potilaita tulee neuvoa ottamaan Neoral 100 mg johdonmukaisesti vuorokaudenajan ja aterioiden suhteen. Greippi ja greippimehu vaikuttavat aineenvaihduntaan ja lisäävät veren syklosporiinipitoisuutta, joten niitä tulee välttää.
