Elocon 5g Mometasone Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mikä Elocon 5g on ja miten sitä käytetään?
Elocon (mometasonifuroaatti) -voide, 0,1% on kortikosteroidivoide, voide tai voide, joka on tarkoitettu kortikosteroideihin reagoivien dermatoosien tulehduksellisten ja kutisevien ilmentymien lievittämiseen vähintään 2-vuotiailla potilailla.
Mitkä ovat Elocon 5g:n sivuvaikutukset?
Eloconin yleisiä sivuvaikutuksia ovat:
- ihottuma,
- kutina,
- palaa,
- punoitus,
- kuivuus,
- ihosi oheneminen tai pehmeneminen,
- ihottuma tai ärsytys suun ympärillä,
- turvonneet karvatupet,
- hämähäkkisuonet,
- tunnottomuus tai pistely,
- muutokset käsitellyn ihon värissä,
- rakkuloita,
- näppylöitä,
- käsitellyn ihon kuoriutuminen tai
- raskausarpia.
KUVAUS
ELOCON (mometasonifuroaatti) voide, 0,1% sisältää mometasonifuroaattia paikalliseen käyttöön. Mometasonifuroaatti on synteettinen kortikosteroidi, jolla on anti-inflammatorinen vaikutus.
Kemiallisesti mometasonifuroaatti on 9a,21-dikloori-11p,17-dihydroksi-16a-metyylipregna-1,4-dieeni3,20-dioni-17-(2-furoaatti), jonka empiirinen kaava on C27H30CI2O6, molekyylipaino 521. ja seuraava rakennekaava:
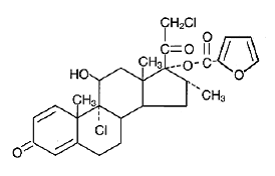
Mometasonifuroaatti on valkoinen tai luonnonvalkoinen jauhe, joka on käytännössä liukenematon veteen, liukenee heikosti oktanoliin ja kohtalaisesti etyylialkoholiin.
Yksi gramma ELOCON 5g Cream, 0,1 % sisältää 1 mg mometasonifuroaattia valkoisessa tai luonnonvalkoisessa kermapohjaisessa alumiinitärkkelysoktenyylisukkinaatissa (gammasäteilytetty), heksyleeniglykolia, hydrattua soijalesitiiniä, fosforihappoa, puhdistettua vettä, valkoista pehmeää titaanidioksidia. parafiini ja valkoinen vaha.
INDIKAATIOT
ELOCON® Cream on kortikosteroidi, joka on tarkoitettu lievittämään kortikosteroideihin reagoivien dermatoosien tulehduksellisia ja kutiavia ilmentymiä vähintään 2-vuotiailla potilailla.
ANNOSTELU JA HALLINNOINTI
Levitä ohut kalvo ELOCON Creamia vaurioituneille ihoalueille kerran päivässä. ELOCON Creamia voidaan käyttää vähintään 2-vuotiailla lapsipotilailla. Koska ELOCON Creamin turvallisuutta ja tehoa ei ole osoitettu alle 2-vuotiailla lapsipotilailla; käyttöä tässä ikäryhmässä ei suositella [katso VAROITUKSET JA VAROTOIMET ja Käyttö tietyissä populaatioissa ].
Hoito tulee lopettaa, kun hallinta on saavutettu. Jos paranemista ei havaita 2 viikon kuluessa, diagnoosin uudelleenarviointi saattaa olla tarpeen. ELOCON Creamin turvallisuutta ja tehoa lapsipotilailla yli 3 viikon käytön aikana ei ole osoitettu.
ELOCON Creamia ei saa käyttää okklusiivisten sidosten kanssa, ellei lääkäri ole määrännyt. ELOCON 5g Creamia ei tule levittää vaippa-alueelle, jos lapsi tarvitsee edelleen vaippoja tai muovihousuja, koska nämä vaatteet voivat muodostaa okklusiivisen sidoksen.
ELOCON Cream on tarkoitettu vain paikalliseen käyttöön. Sitä ei ole tarkoitettu oraaliseen, oftalmiseen tai intravaginaaliseen käyttöön.
Vältä käyttöä kasvoilla, nivusissa tai kainaloissa.
MITEN TOIMITETAAN
Annostusmuodot ja vahvuudet
Kerma, 0,1 %. Jokainen gramma ELOCON Creamia sisältää 1 mg mometasonifuroaattia valkoisen tai luonnonvalkoisen tasaisen ja homogeenisen voidepohjan muodossa.
Varastointi ja käsittely
ELOCON voide on väriltään valkoisesta luonnonvalkoiseen ja toimitetaan 15 gramman (NDC 0085-3149-01) ja 50 gramman ( NDC 0085-3149-03) putket.
Säilytä 25°C (77°F); retket sallitaan 15-30°C:een (59-86°F) [katso USP-ohjattu huonelämpötila ]. Vältä liiallista lämpöä.
Valmistettu: Merck Sharp & Dohme Corp., Merck & Co., Inc:n tytäryhtiö, Whitehouse Station, NJ 08889, USA. Valmistaja: Schering-Plough Labo NV Heist-op-den-Berg, Belgia. Tarkistettu: huhtikuuta 2013
SIVUVAIKUTUKSET
Koska kliiniset tutkimukset suoritetaan hyvin vaihtelevissa olosuhteissa, lääkkeen kliinisissä tutkimuksissa havaittuja haittavaikutuksia ei voida verrata suoraan toisen lääkkeen kliinisissä tutkimuksissa havaittuihin nopeuksiin, eivätkä ne välttämättä kuvasta kliinisissä käytännöissä havaittuja nopeuksia.
Kontrolloiduissa kliinisissä tutkimuksissa, joihin osallistui 319 henkilöä, ELOCON 5g Creamin käyttöön liittyvien haittavaikutusten ilmaantuvuus oli 1,6 %. Raportoituja reaktioita olivat polttaminen, kutina ja ihon surkastuminen. Myös ELOCON 5g Creamin käyttöön liittyvästä ruusufinnistä on saatu ilmoituksia. Kontrolloiduissa kliinisissä tutkimuksissa (n=74), joihin osallistui 2–12-vuotiaita lapsia, ELOCON 5g Creamin käyttöön liittyvien haittavaikutusten ilmaantuvuus oli noin 7 %. Raportoituja reaktioita olivat pistely, kutina ja furunkuloosi.
Seuraavien haittavaikutusten ilmoitettiin mahdollisesti tai todennäköisesti liittyvän ELOCON 5g Cream -hoitoon kliinisissä tutkimuksissa 4 %:lla 182:sta 6 kuukauden–2 vuoden ikäisestä lapsipotilasta: alentuneet glukokortikoidipitoisuudet, 2; parestesia, 2; follikuliitti, 1; moniliaasi, 1; bakteeri-infektio, 1; ihon depigmentaatio, 1. Seuraavia ihon surkastumisen merkkejä havaittiin myös kliinisessä tutkimuksessa ELOCON-voiteella hoidetuilla 97 koehenkilöllä: kiilto, 4; telangiektasia, 1; elastisuuden menetys, 4; normaalien ihomerkkien menetys, 4; ohuus, 1; ja mustelmat, 1.
Seuraavia muita paikallisia haittavaikutuksia on raportoitu paikallisesti käytettäessä kortikosteroideja, mutta niitä voi esiintyä useammin käytettäessä okklusiivisia sidoksia. Nämä reaktiot ovat: ärsytys, kuivuus, follikuliitti, hypertrichoosi, aknetyyppiset ihottumat, hypopigmentaatio, perioraalinen ihotulehdus, allerginen kosketusihottuma, sekundaarinen infektio, striae ja miliaria.
HUUMEIDEN VUOROVAIKUTUKSET
ELOCON Creamin kanssa ei ole tehty lääkkeiden yhteisvaikutustutkimuksia.
VAROITUKSET
Mukana osana VAROTOIMENPITEET osio.
VAROTOIMENPITEET
Vaikutukset endokriiniseen järjestelmään
Paikallisten kortikosteroidien systeeminen imeytyminen voi aiheuttaa palautuvaa hypotalamus-aivolisäke-lisämunuaisen (HPA) akselin suppressiota, mikä voi aiheuttaa glukokortikosteroidien vajaatoimintaa. Tämä voi tapahtua hoidon aikana tai hoidon lopettamisen jälkeen. Cushingin oireyhtymän, hyperglykemian ja glukosurian ilmenemismuodot voivat myös aiheuttaa joillakin potilailla paikallisten kortikosteroidien systeemisen imeytymisen hoidon aikana. Tekijöitä, jotka altistavat paikallista kortikosteroidia käyttävän potilaan HPA-akselin suppressioon, ovat voimakkaiden steroidien käyttö, suuret hoitopinta-alat, pitkäaikainen käyttö, okklusiivisten sidosten käyttö, muuttunut ihosuoja, maksan vajaatoiminta ja nuori ikä.
Koska systeeminen imeytyminen on mahdollista, paikallisten kortikosteroidien käyttö saattaa edellyttää, että potilaat on säännöllisesti arvioitava HPA-akselin suppression varalta. Tämä voidaan tehdä käyttämällä adrenokortikotrooppisen hormonin (ACTH) stimulaatiotestiä.
Tutkimuksessa, jossa arvioitiin mometasonifuroaattivoiteen vaikutuksia HPA-akseliin, 15 grammaa annosteltiin kahdesti päivässä 7 päivän ajan kuudelle aikuiselle, joilla oli psoriaasi tai atooppinen ihottuma. Tulokset osoittavat, että lääke vähensi hieman lisämunuaisen kortikosteroidieritystä.
Jos havaitaan HPA-akselin suppressiota, lääke on yritettävä poistaa vähitellen, vähentää annostelutiheyttä tai korvata tilalla vähemmän tehokas kortikosteroidi. HPA-akselin toiminta palautuu yleensä nopeasti, kun paikallisten kortikosteroidien käyttö lopetetaan. Harvoin voi ilmaantua merkkejä ja oireita glukokortikosteroidien vajaatoiminnasta, mikä vaatii täydentäviä systeemisiä kortikosteroideja.
Lapsipotilaat voivat olla alttiimpia systeemiselle myrkyllisyydelle vastaavilla annoksilla johtuen heidän suuremmasta ihon pinta-alasta ruumiinmassaan [ks. Käyttö tietyissä populaatioissa ].
Allerginen kontaktidermatiitti
Jos ärsytystä ilmenee, ELOCON Creamin käyttö on lopetettava ja asianmukainen hoito aloitettava. Kortikosteroidien aiheuttama allerginen kosketusihottuma diagnosoidaan yleensä havaitsemalla parantumisen epäonnistuminen sen sijaan, että havaitaan kliininen paheneminen, kuten useimpien kortikosteroideja sisältämättömien paikallisten tuotteiden kohdalla. Tällainen havainto on vahvistettava asianmukaisella diagnostisella laastaritestillä.
Samanaikaiset ihoinfektiot
Jos samanaikaisia ihoinfektioita esiintyy tai kehittyy, tulee käyttää asianmukaista sieni- tai antibakteerista ainetta. Jos myönteistä vastetta ei ilmene välittömästi, ELOCON 5g Creamin käyttö tulee lopettaa, kunnes infektio on saatu riittävästi hallintaan.

Ei-kliininen toksikologia
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Pitkäaikaisia eläinkokeita ei ole tehty ELOCON 5g Creamin karsinogeenisuuden arvioimiseksi. Mometasonifuroaatin pitkäaikaisia karsinogeenisuustutkimuksia tehtiin inhalaatioreitillä rotilla ja hiirillä. Sprague Dawley -rotilla tehdyssä 2 vuotta kestäneessä karsinogeenisuustutkimuksessa mometasonifuroaatti ei osoittanut tilastollisesti merkitsevää kasvainten lisääntymistä inhalaatioannoksilla 67 mikrog/kg asti (noin 0,04 kertaa ELOCON 5g Creamin arvioitu kliininen enimmäisannos mcg/m²:n perusteella. ). Sveitsiläisillä CD-1-hiirillä tehdyssä 19 kuukautta kestäneessä karsinogeenisuustutkimuksessa mometasonifuroaatti ei osoittanut tilastollisesti merkitsevää kasvainten ilmaantuvuuden lisääntymistä inhalaatioannoksilla 160 mcg/kg asti (noin 0,05 kertaa ELOCON Creamin arvioitu kliininen paikallisannos mcg/m² perusteella).
Mometasonifuroaatti lisäsi kromosomipoikkeavuuksia kiinanhamsterin munasarjasolutestissä in vitro, mutta ei lisännyt kromosomipoikkeavuuksia in vitro kiinanhamsterin keuhkosolutestissä. Mometasonifuroaatti ei ollut mutageeninen Amesin testissä tai hiiren lymfoomamäärityksessä, eikä se ollut klastogeeninen hiiren in vivo mikrotumatestissä, rotan luuytimen kromosomipoikkeavuusmäärityksessä tai hiiren uros-sukusolukromosomipoikkeavuusmäärityksessä. Mometasonifuroaatti ei myöskään indusoinut suunnittelematonta DNA-synteesiä in vivo rotan maksasoluissa.
Rotilla tehdyissä lisääntymistutkimuksissa uros- tai naarasrotilla ei havaittu hedelmällisyyden heikkenemistä 15 mikrog/kg:n ihonalaisilla annoksilla (noin 0,01 kertaa ELOCON 5g Creamin arvioitu kliininen paikallisannos mikrog/m²:n perusteella).
Käyttö tietyissä populaatioissa
Raskaus
Teratogeeniset vaikutukset - Raskausluokka C
Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia raskaana oleville naisille. Siksi ELOCON 5g Creamia tulee käyttää raskauden aikana vain, jos mahdollinen hyöty oikeuttaa mahdollisen riskin sikiölle.
Kortikosteroidien on osoitettu olevan teratogeenisiä koe-eläimissä, kun niitä annetaan systeemisesti suhteellisen pieninä annoksina. Joidenkin kortikosteroidien on osoitettu olevan teratogeenisiä koe-eläimillä ihon kautta levitettynä.
Kun mometasonifuroaattia annettiin raskaana oleville rotille, kaniineille ja hiirille, se lisäsi sikiön epämuodostumia. Epämuodostumia aiheuttaneet annokset vähensivät myös sikiön kasvua, mitattuna pienemmillä sikiön painoilla ja/tai viivästyneellä luustumisella. Mometasonifuroaatti aiheutti myös dystokiaa ja siihen liittyviä komplikaatioita, kun sitä annettiin rotille raskauden lopussa.
Hiirillä mometasonifuroaatti aiheutti suulakihalkeamaa ihonalaisilla annoksilla 60 mikrogrammaa/kg tai enemmän. Sikiön eloonjääminen väheni 180 mcg/kg. Myrkyllisyyttä ei havaittu annoksella 20 mcg/kg. (20, 60 ja 180 mikrog/kg annokset hiirellä ovat noin 0,01, 0,02 ja 0,05 kertaa ELOCON Creamin arvioitu kliininen enimmäisannos mcg/m²:n perusteella.)
Rotilla mometasonifuroaatti aiheutti napatyrä paikallisilla annoksilla 600 mcg/kg tai enemmän. Annos 300 mikrogrammaa/kg aiheutti viivästyksiä luustumisessa, mutta ei epämuodostumia. (300 ja 600 mcg/kg annokset rotilla ovat noin 0,2 ja 0,4 kertaa ELOCON 5g Creamin arvioitu kliininen enimmäisannos mcg/m²:n perusteella.)
Kaneissa mometasonifuroaatti aiheutti useita epämuodostumia (esim. taipuneita etukäpälöitä, sappirakon ageneesia, napatyrä, vesipää) paikallisilla annoksilla 150 mcg/kg tai enemmän (noin 0,2 kertaa ELOCON Creamin arvioitu kliininen paikallinen annos mcg/kg:lla). m² perusteella). Suun kautta annetussa tutkimuksessa mometasonifuroaatti lisäsi resorptiota ja aiheutti suulakihalkeamia ja/tai pään epämuodostumia (vesipää ja kupumainen pää) annoksella 700 mikrogrammaa/kg. 2800 mcg/kg useimmat pentueet keskeytettiin tai imeytyivät. Myrkyllisyyttä ei havaittu annoksella 140 mcg/kg. (Annokset 140, 700 ja 2800 mikrog/kg kanilla ovat noin 0,2, 0,9 ja 3,6 kertaa ELOCON 5g Creamin arvioidut kliiniset paikalliset annokset mikrog/m²:n perusteella.)
Kun rotat saivat ihonalaisia annoksia mometasonifuroaattia koko raskauden ajan tai raskauden myöhemmissä vaiheissa, 15 mikrogrammaa/kg aiheutti pitkittyneen ja vaikean synnytyksen ja vähensi elävien syntymien määrää, syntymäpainoa ja varhaista poikasten eloonjäämistä. Samanlaisia vaikutuksia ei havaittu annoksella 7,5 mcg/kg. (7,5 ja 15 mcg/kg annokset rotilla ovat noin 0,005 ja 0,01 kertaa ELOCON Creamin arvioitu kliininen enimmäisannos mcg/m²:n perusteella.)
Imettävät äidit
Systeemisesti annettavia kortikosteroideja erittyy äidinmaitoon ja ne voivat hidastaa kasvua, häiritä endogeenisten kortikosteroidien tuotantoa tai aiheuttaa muita epäsuotuisia vaikutuksia. Ei tiedetä, voisiko kortikosteroidien paikallinen anto johtaa riittävään systeemiseen imeytymiseen tuottamaan havaittavia määriä äidinmaitoon. Koska monet lääkkeet erittyvät äidinmaitoon, on noudatettava varovaisuutta, kun ELOCON 5g -voidetta annetaan imettävälle naiselle.
Käyttö lapsille
ELOCON Creamia voidaan käyttää varoen 2-vuotiaille tai sitä vanhemmille lapsipotilaille, vaikka yli 3 viikkoa kestävän lääkkeen käytön turvallisuutta ja tehoa ei ole osoitettu. Koska ELOCON 5g Creamin turvallisuutta ja tehoa ei ole osoitettu alle 2-vuotiailla lapsipotilailla, sen käyttöä tässä ikäryhmässä ei suositella.
Lapsitutkimuksessa 24 atooppisen ihottuman potilasta, joista 19 oli 2–12-vuotiaita, hoidettiin ELOCON Cream -voiteella kerran päivässä. Suurin osa koehenkilöistä parantui 3 viikossa. ELOCON 5g Cream aiheutti HPA-akselin suppression noin 16 %:lla 6–23 kuukauden ikäisistä lapsista, joiden lisämunuaisten toiminta oli normaalia Cortrosyn-testissä ennen hoidon aloittamista ja joita hoidettiin noin 3 viikon ajan. keskimääräinen kehon pinta-ala 41 % (vaihteluväli 15–94 %). Suppression kriteerit olivat: peruskortisolitaso ≤ 5 mcg/dl, 30 minuutin stimulaation jälkeinen taso ≤ 18 mcg/dl tai nousu KLIININEN FARMAKOLOGIA ].
Koska ihon pinta-alan suhde ruumiinmassaan on suurempi, lapsipotilailla on suurempi riski saada HPA-akselin suppressio ja Cushingin oireyhtymä, kun heitä hoidetaan paikallisilla kortikosteroideilla. Siksi heillä on myös suurempi riski saada lisämunuaisten vajaatoiminta hoidon aikana ja/tai sen jälkeen. Lapsipotilaat voivat olla aikuisia alttiimpia ihon surkastumiselle, mukaan lukien striat, kun heitä hoidetaan paikallisilla kortikosteroideilla. Lapsipotilailla, jotka käyttävät paikallisia kortikosteroideja yli 20 %:lle kehon pinnasta, on suurempi riski HPA-akselin suppressiosta.
HPA-akselin suppressiota, Cushingin oireyhtymää, lineaarista kasvun hidastumista, viivästynyttä painonnousua ja kallonsisäistä hypertensiota on raportoitu paikallisia kortikosteroideja saavilla lapsipotilailla. Lisämunuaisen suppression ilmenemismuotoja lapsilla ovat alhaiset plasman kortisolitasot ja vasteen puuttuminen ACTH-stimulaatiosta. Kallonsisäisen kohonneen verenpaineen ilmenemismuotoja ovat pullistuneet fontanellit, päänsärky ja molemminpuolinen papillideema.
ELOCON Creamia ei tule käyttää vaippaihottuman hoidossa.
Geriatrinen käyttö
ELOCON 5g Creamin kliinisissä tutkimuksissa oli mukana 190 henkilöä, jotka olivat vähintään 65-vuotiaita, ja 39 henkilöä, jotka olivat vähintään 75-vuotiaita. Näiden ja nuorempien koehenkilöiden välillä ei havaittu yleisiä eroja turvallisuudessa tai tehokkuudessa, ja muut raportoidut kliiniset kokemukset eivät ole osoittaneet eroja iäkkäiden ja nuorempien potilaiden vasteissa. Joidenkin iäkkäiden henkilöiden suurempaa herkkyyttä ei kuitenkaan voida sulkea pois.
YLIANNOSTUS
Paikallisesti levitetty ELOCON Cream voi imeytyä riittävinä määrinä systeemisten vaikutusten aikaansaamiseksi [katso VAROITUKSET JA VAROTOIMET ].
VASTA-AIHEET
Ei mitään.
KLIININEN FARMAKOLOGIA
Toimintamekanismi
Muiden paikallisten kortikosteroidien tapaan mometasonifuroaatilla on anti-inflammatorisia, kutinaa estäviä ja verisuonia supistavia ominaisuuksia. Paikallisten steroidien anti-inflammatorisen vaikutuksen mekanismi on yleensä epäselvä. Kortikosteroidien uskotaan kuitenkin toimivan indusoimalla fosfolipaasi A2:ta estäviä proteiineja, joita kutsutaan yhteisesti lipokortiineiksi. Oletetaan, että nämä proteiinit säätelevät voimakkaiden tulehduksen välittäjien, kuten prostaglandiinien ja leukotrieenien, biosynteesiä estämällä niiden yhteisen esiasteen arakidonihapon vapautumista. Fosfolipaasi A2 vapauttaa arakidonihappoa kalvon fosfolipideistä.
Farmakodynamiikka
ELOCON 5g Creamilla tehdyt tutkimukset osoittavat, että sen teho on keskitasoa verrattuna muihin paikallisiin kortikosteroideihin.
Tutkimuksessa, jossa arvioitiin mometasonifuroaattivoiteen vaikutuksia HPA-akseliin, 15 grammaa annosteltiin kahdesti päivässä 7 päivän ajan kuudelle aikuiselle, joilla oli psoriaasi tai atooppinen ihottuma. Voidetta levitettiin ilman okkluusiota vähintään 30 %:lle kehon pinnasta. Tulokset osoittivat, että lääke aiheutti lievää lisämunuaisen kortikosteroidierityksen laskua [katso VAROITUKSET JA VAROTOIMET ].
Avoimeen HPA-akselin turvallisuustutkimukseen otettiin mukaan yhdeksänkymmentäseitsemän atooppista ihottumaa sairastavaa 6–23 kuukauden ikäistä lapsipotilasta. ELOCON Creamia levitettiin kerran päivässä noin 3 viikon ajan keskimääräiselle kehon pinta-alalle 41 % (vaihteluväli 15–94 %). Noin 16 %:lla potilaista, joiden lisämunuaisten toiminta oli normaalia Cortrosyn-testissä ennen hoidon aloittamista, lisämunuaisten vajaatoimintaa havaittiin ELOCON 5g Cream -hoidon lopussa. Suppression kriteerit olivat: peruskortisolitaso ≤ 5 mcg/dl, 30 minuutin stimulaation jälkeinen taso ≤ 18 mcg/dl tai nousu Käyttö tietyissä populaatioissa ].
Farmakokinetiikka
Paikallisten kortikosteroidien ihon kautta tapahtuvan imeytymisen laajuus määräytyy monien tekijöiden mukaan, mukaan lukien vehikkeli ja epidermaalisen esteen eheys. Ihmisillä tehdyt tutkimukset osoittavat, että noin 0,4 % levitetystä ELOCON 5g Creamin annoksesta pääsee verenkiertoon 8 tunnin kosketuksen jälkeen normaalilla iholla ilman tukkeumaa. Ihon tulehdus ja/tai muut sairausprosessit voivat lisätä ihon kautta tapahtuvaa imeytymistä.
Kliiniset tutkimukset
ELOCON 5g Creamin turvallisuutta ja tehoa kortikosteroideihin reagoivien ihottumien hoidossa arvioitiin kahdessa satunnaistetussa, kaksoissokkoutetussa, vehikkeleillä kontrolloidussa kliinisessä tutkimuksessa, joista toisessa psoriaasissa ja toisessa atooppisessa dermatiitissa. Näissä kokeissa arvioitiin yhteensä 366 henkilöä (12-81-vuotiaita), joista 177 sai ELOCON-voidetta ja 181 koehenkilöä vehikkelivoidetta. ELOCON-voidetta tai ajoneuvovoidetta levitettiin kerran päivässä 21 päivän ajan.
Kaksi tutkimusta osoittivat, että ELOCON 5g Cream on tehokas psoriaasin ja atooppisen ihottuman hoidossa.
POTILASTIEDOT
Kerro potilaille seuraavista:
- Käytä ELOCON 5g Creamia lääkärin ohjeiden mukaan. Se on tarkoitettu vain ulkoiseen käyttöön.
- Vältä kosketusta silmiin.
- Älä käytä ELOCON Creamia kasvoille, kainaloihin tai nivusiin, ellei lääkäri ole niin määrännyt.
- Älä käytä ELOCON 5g Creamia muihin sairauksiin kuin siihen, johon se on määrätty.
- Käsiteltyä ihoaluetta ei saa sitoa tai muuten peittää tai kääriä tukkimaan, ellei lääkäri niin määrää.
- Ilmoita lääkärille kaikista paikallisten haittavaikutusten merkeistä.
- Neuvo potilaita olemaan käyttämättä ELOCON 5g -voidetta vaippaihottuman hoidossa. Älä käytä ELOCON Creamia vaippa-alueelle, sillä vaipat tai muovihousut voivat muodostaa okklusiivisen sidoksen.
- Lopeta hoito, kun hallinta on saavutettu. Jos parannusta ei näy 2 viikon kuluessa, ota yhteys lääkäriin.
- Älä käytä muita kortikosteroideja sisältäviä tuotteita ELOCON Creamin kanssa neuvottelematta ensin lääkärin kanssa.
