Brand Temovate 15g Clobetasol Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Temovate on ja miten sitä käytetään?
Temovate on reseptilääke, jota käytetään plakki- ja päänahan psoriaasin sekä kortikosteroideihin reagoivien dermatoosien oireiden hoitoon. Temovatea voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Temovate kuuluu lääkeryhmään nimeltä kortikosteroidit, paikalliset.
Ei tiedetä, onko Temovate turvallinen ja tehokas alle 12-vuotiaille lapsille.
Mitkä ovat Temovate-valmisteen mahdolliset sivuvaikutukset?
Temovate voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- ihosi tilan heikkeneminen,
- minkä tahansa käsitellyn ihon punoitus, lämpö, turvotus, vuoto tai voimakas ärsytys,
- näön hämärtyminen,
- putkinäkö,
- silmäkipu,
- nähdä haloja valojen ympärillä,
- lisääntynyt jano,
- kuiva suu,
- hedelmäinen hengityksen tuoksu,
- painonnousu kasvoissasi ja hartioissasi,
- hidas haavan paraneminen,
- ihon värjäytymistä,
- ihon oheneminen,
- lisääntynyt vartalon karva,
- väsymys,
- mielialan muutoksia,
- kuukautiskierron muutokset ja
- seksuaalisia muutoksia
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Temovate-valmisteen yleisimpiä sivuvaikutuksia ovat:
- käsitellyn ihon polttaminen, kutina, turvotus tai ärsytys,
- kuiva tai halkeileva iho,
- punoitusta tai hilseilyä karvatuppien ympärillä,
- hämähäkkisuonet,
- raskausarpia,
- ihon oheneminen,
- ihottuma tai nokkosihottuma,
- akne ja
- tilapäinen hiustenlähtö
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikki Temovaten mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
TEMOVATE® (klobetasolipropionaattivoide ja -voide) Cream and Ointment, 0,05 % sisältää vaikuttavana aineena klobetasolipropionaattia, synteettistä kortikosteroidia, paikalliseen dermatologiseen käyttöön. Klobetasolilla, prednisolonin analogilla, on korkea glukokortikoidiaktiivisuus ja vähäinen mineralokortikoidiaktiivisuus.
Klobetasolipropionaatti on kemiallisesti (11ß,16ß)-21-kloori-9-fluori-11-hydroksi-16-metyyli-17-(1-oksopropoksi)pregna-1,4-dieeni-3,20-dioni ja sillä on seuraava rakennekaava:
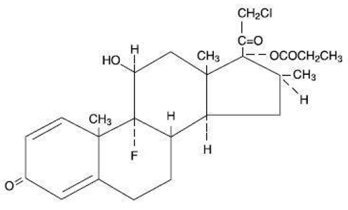
Klobetasolipropionaatin molekyylikaava on C25H32CIFO5 ja molekyylipaino 467. Se on valkoinen tai kermanvärinen kiteinen jauhe, joka ei liukene veteen.
TEMOVATE® Cream sisältää klobetasolipropionaattia 0,5 mg/g propyleeniglykolia, glyseryylimonostearaattia, setostearyylialkoholia, glyseryylistearaattia, PEG 100 stearaattia, valkoista vahaa, kloorikresolia, natriumsitraattia, sitruunahappomonohydraattia ja puhdistettua vettä sisältävässä voidepohjassa.
TEMOVATE® Ointment sisältää klobetasolipropionaattia 0,5 mg/g propyleeniglykolin, sorbitaaniseskvioleaatin ja valkoisen vaseliinin pohjana.
INDIKAATIOT
TEMOVATE® Cream and Ointment ovat erittäin tehokkaita kortikosteroidivalmisteita, jotka on tarkoitettu lievittämään kortikosteroideihin reagoivien dermatoosien tulehduksellisia ja kutinaa. Yli 2 peräkkäistä viikkoa kestävää hoitoa ei suositella, ja kokonaisannos ei saa ylittää 50 g/viikko, koska lääke voi suppressoida hypotalamus-aivolisäke-lisämunuainen (HPA) -akselia. Käyttöä alle 12-vuotiaille lapsipotilaille ei suositella.
Kuten muidenkin erittäin aktiivisten kortikosteroidien kohdalla, hoito tulee lopettaa, kun hallinta on saavutettu. Jos paranemista ei havaita 2 viikon kuluessa, diagnoosin uudelleenarviointi voi olla tarpeen.
ANNOSTELU JA HALLINNOINTI
Levitä ohut kerros TEMOVATE®-voidetta tai -voidetta sairastuneille ihoalueille kahdesti päivässä ja hiero hellästi ja kokonaan (katso KÄYTTÖAIHEET JA KÄYTTÖ ).
TEMOVATE® Cream ja Ointment ovat erittäin tehokkaita paikallisia kortikosteroideja; siksi, hoito tulee rajoittaa kahteen peräkkäiseen viikkoon, eikä yli 50 g/viikko saa käyttää.
Kuten muidenkin erittäin aktiivisten kortikosteroidien kohdalla, hoito tulee lopettaa, kun hallinta on saavutettu. Jos paranemista ei havaita 2 viikon kuluessa, diagnoosin uudelleenarviointi saattaa olla tarpeen.
TEMOVATE®-voidetta ja -voidetta ei tule käyttää okklusiivisten sidosten kanssa.
Geriatrinen käyttö
Tutkimuksissa, joissa geriatriset potilaat (65-vuotiaat tai vanhemmat, katso VAROTOIMENPITEET on hoidettu TEMOVATE®-voiteella tai -voiteella, turvallisuus ei eronnut nuorempien potilaiden turvallisuudesta; siksi annoksen muuttamista ei suositella.
MITEN TOIMITETAAN
TEMOVATE® (klobetasolipropionaattivoide) kerma, 0,05 % toimitetaan:
30 g putket ( NDC 10337-163-30) ja 60 g putket ( NDC 10337-163-60).
TEMOVATE® (klobetasolipropionaattivoide) voide, 0,05 %, toimitetaan:
15 g putket ( NDC 10337-162-15) ja 30 g putket ( NDC 10337-162-30).
Säilytä 15–30 °C (59–86 °F). TEMOVATE®-voidetta ei saa säilyttää jääkaapissa. PharmaDerm
Fougera Pharmaceuticals Inc:n osasto, Melville, NY 11747 USA. Tarkistettu: tammikuu 2012
SIVUVAIKUTUKSET
Kontrolloiduissa kliinisissä tutkimuksissa TEMOVATE® Creamin yleisimmät haittavaikutukset olivat polttava ja pistely tunne 1 %:lla hoidetuista potilaista. Harvempia haittavaikutuksia olivat kutina, ihon surkastuminen sekä ihon halkeilu ja halkeilu.
Kontrolloiduissa kliinisissä tutkimuksissa TEMOVATE® Ointmentin yleisimmät haittatapahtumat olivat polttava tunne, ärsytys ja kutina 0,5 %:lla hoidetuista potilaista. Harvempia haittavaikutuksia olivat pistely, halkeilu, eryteema, follikuliitti, sormien puutuminen, ihon surkastuminen ja telangiektasia.
Cushingin oireyhtymää on raportoitu imeväisillä ja aikuisilla paikallisten klobetasolipropionaattivalmisteiden pitkäaikaisen käytön seurauksena.
Seuraavia muita paikallisia haittavaikutuksia on raportoitu paikallisten kortikosteroidien yhteydessä, ja niitä saattaa esiintyä useammin käytettäessä okklusiivisia sidoksia ja voimakkaampia kortikosteroideja. Nämä reaktiot on lueteltu suunnilleen alenevassa esiintymisjärjestyksessä: kuivuus, aknetyyppiset ihottumat, hypopigmentaatio, perioraalinen ihotulehdus, allerginen kosketusihottuma, sekundaarinen infektio, ärsytys, striae ja miliaria.

HUUMEIDEN VUOROVAIKUTUKSET
Tietoja ei ole annettu.
VAROITUKSET
Tietoja ei ole annettu. Ole hyvä ja katso ENNAKKOOHJEET osio alla.
VAROTOIMENPITEET
Kenraali
TEMOVATE® emulsiovoidetta ja -voidetta ei tule käyttää ruusufinnien tai perioraalisen ihotulehduksen hoitoon, eikä sitä saa käyttää kasvoille, nivusille tai kainaloihin.
Paikallisten kortikosteroidien systeeminen imeytyminen voi aiheuttaa palautuvaa HPA-akselin suppressiota, mikä voi aiheuttaa glukokortikosteroidien vajaatoimintaa hoidon lopettamisen jälkeen. Cushingin oireyhtymän, hyperglykemian ja glukosurian ilmenemismuotoja voi myös aiheuttaa joillakin potilailla paikallisten kortikosteroidien systeeminen imeytyminen hoidon aikana.
Potilaat, jotka käyttävät paikallista steroidia suurelle pinta-alalle tai tukkeutuneille alueille, tulee arvioida säännöllisesti HPA-akselin suppression varalta. Tämä voidaan tehdä käyttämällä ACTH-stimulaatiota, AM-plasmakortisoli- ja virtsan vapaan kortisolin testejä. Potilaita, jotka saavat erittäin tehokkaita kortikosteroideja, ei tule hoitaa yli 2 viikkoa kerrallaan, ja vain pieniä alueita tulee hoitaa kerrallaan lisääntyneen HPA-suppression riskin vuoksi.
TEMOVATE®-voide ja -voide aiheuttivat HPA-akselin suppression, kun niitä käytettiin niinkin pieninä annoksina kuin 2 g/vrk 1 viikon ajan ekseemapotilailla.
Jos havaitaan HPA-akselin suppressiota, lääke on yritettävä vetää pois käytöstä, vähentää annostelutiheyttä tai korvata se vähemmän tehokkaalla kortikosteroidilla. HPA-akselin toiminta palautuu yleensä nopeasti, kun paikallisten kortikosteroidien käyttö lopetetaan. Harvoin voi ilmaantua glukokortikosteroidien vajaatoiminnan merkkejä ja oireita, jotka vaativat täydentäviä systeemisiä kortikosteroideja. Lisätietoja systeemisestä lisäravinteesta on kyseisten valmisteiden ohjetiedoissa.
Lapsipotilaat voivat olla alttiimpia vastaavien annosten systeemiselle toksisille vaikutuksille, koska heidän ihon pinta-ala ja kehon massa on suurempia (ks. VAROTOIMENPITEET : Käyttö lapsille ).
Jos ärsytystä kehittyy, TEMOVATE® Cream and Ointment -voide ja -voide on lopetettava ja aloitettava asianmukainen hoito. Kortikosteroidien aiheuttama allerginen kosketusihottuma diagnosoidaan yleensä havaitsemalla parantumisen epäonnistuminen sen sijaan, että havaitaan kliininen paheneminen, kuten useimpien kortikosteroideja sisältämättömien paikallisten tuotteiden kohdalla. Tällainen havainto on vahvistettava asianmukaisella diagnostisella laastaritestillä.
Jos samanaikaisia ihoinfektioita esiintyy tai kehittyy, tulee käyttää asianmukaista sieni- tai antibakteerista ainetta. Jos myönteistä vastetta ei ilmene välittömästi, TEMOVATE®-emulsiovoiteen ja -voiteen käyttö on lopetettava, kunnes infektio on saatu riittävästi hallintaan.
Laboratoriotestit
Seuraavat testit voivat olla hyödyllisiä arvioitaessa potilaiden HPA-akselin suppressiota:
ACTH-stimulaatiotesti AM plasman kortisolitesti Virtsan vapaa kortisolitesti
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Klobetasolipropionaatin karsinogeenisen potentiaalin arvioimiseksi ei ole tehty pitkäaikaisia eläinkokeita.
Rotilla tehdyt tutkimukset ihonalaisen annostelun jälkeen 50 mikrogrammaa/kg/vrk asti osoittivat, että naarailla havaittiin resorboituneiden alkioiden määrän lisääntymistä ja elävien sikiöiden määrän laskua suurimmalla annoksella.
Klobetasolipropionaatti ei ollut mutageeninen kolmessa eri testijärjestelmässä: Ames-testissä, Saccharomyces cerevisiaen geenikonversiomäärityksessä ja E. coli B WP2 -vaihtelutestissä.
Raskaus
Teratogeeniset vaikutukset
Raskausluokka C. Kortikosteroidien on osoitettu olevan teratogeenisiä koe-eläimissä, kun niitä annetaan systeemisesti suhteellisen pieninä annoksina. Joidenkin kortikosteroidien on osoitettu olevan teratogeenisiä koe-eläimille ihon kautta levitettynä.
Klobetasolipropionaatin teratogeenisuutta ei ole testattu paikallisesti käytettynä; se kuitenkin imeytyy perkutaanisesti, ja ihonalaisesti annettuna se oli merkittävä teratogeeni sekä kaniinilla että hiirellä. Klobetasolipropionaatilla on suurempi teratogeeninen potentiaali kuin vähemmän tehokkailla steroideilla.
Hiirillä tehdyt teratogeenisuustutkimukset ihonalaisesti johtivat sikiötoksisuuteen suurimmalla testatulla annoksella (1 mg/kg) ja teratogeenisuuteen kaikilla testatuilla annostasoilla 0,03 mg/kg asti. Nämä annokset ovat noin 1,4-kertaisia ja 0,04-kertaisia verrattuna TEMOVATE®-emulsiovoiteen ja -voiteen paikalliseen annokseen. Nähtyihin poikkeavuuksiin kuuluivat suulakihalkio ja luuston poikkeavuudet.
Kaneissa klobetasolipropionaatti oli teratogeeninen annoksilla 3 ja 10 mikrog/kg. Nämä annokset ovat noin 0,02-kertaisia ja vastaavasti 0,05-kertaisia TEMOVATE®-emulsiovoiteen ja -voiteen paikalliseen annokseen verrattuna. Havaittuihin poikkeavuuksiin sisältyi kitalakihalkeama, kranioskisi ja muut luuston poikkeavuudet.
Ei ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia klobetasolipropionaatin teratogeenisesta potentiaalista raskaana oleville naisille. TEMOVATE®-voidetta ja -voidetta tulee käyttää raskauden aikana vain, jos mahdollinen hyöty oikeuttaa sikiölle mahdollisesti aiheutuvan riskin.
Imettävät äidit
Systeemisesti annettavia kortikosteroideja erittyy äidinmaitoon ja ne voivat hidastaa kasvua, häiritä endogeenisten kortikosteroidien tuotantoa tai aiheuttaa muita epäsuotuisia vaikutuksia. Ei tiedetä, voisiko kortikosteroidien paikallinen anto johtaa riittävään systeemiseen imeytymiseen tuottamaan havaittavia määriä äidinmaitoon. Koska monet lääkkeet erittyvät äidinmaitoon, on noudatettava varovaisuutta, kun TEMOVATE®-voidetta tai -voidetta annetaan imettävälle naiselle.
Käyttö lapsille
TEMOVATE® emulsiovoiteen ja -voiteen turvallisuutta ja tehokkuutta lapsipotilailla ei ole osoitettu. Käyttöä alle 12-vuotiaille lapsipotilaille ei suositella. Koska ihon pinta-alan suhde kehon painoon on suurempi, lapsipotilailla on suurempi riski saada HPA-akselin suppressio ja Cushingin oireyhtymä, kun heitä hoidetaan paikallisilla kortikosteroideilla. Siksi heillä on myös suurempi riski saada lisämunuaisten vajaatoiminta hoidon aikana tai sen jälkeen. Haittavaikutuksia, mukaan lukien striat, on raportoitu paikallisten kortikosteroidien epäasianmukaisesta käytöstä imeväisille ja lapsille.
HPA-akselin suppressiota, Cushingin oireyhtymää, lineaarista kasvun hidastumista, viivästynyttä painonnousua ja kallonsisäistä hypertensiota on raportoitu paikallisia kortikosteroideja saavilla lapsilla. Lisämunuaisen suppression ilmenemismuotoja lapsilla ovat alhaiset plasman kortisolitasot ja vasteen puuttuminen ACTH-stimulaatiosta. Kallonsisäisen kohonneen verenpaineen ilmenemismuotoja ovat pullistuneet fontanellit, päänsärky ja molemminpuolinen papillideema.
Geriatrinen käyttö
Rajoitettu määrä 65-vuotiaita tai sitä vanhempia potilaita on hoidettu TEMOVATE® Cream -voiteella (n = 231) ja TEMOVATE® Ointment -voiteella (n = 101) Yhdysvalloissa ja Yhdysvaltojen ulkopuolella tehdyissä kliinisissä tutkimuksissa. Vaikka potilaiden määrä on liian pieni tehon ja turvallisuuden erillisen analyysin mahdollistamiseksi, tässä populaatiossa raportoidut haittavaikutukset olivat samanlaisia kuin nuorempien potilaiden raportoimat haittavaikutukset. Saatavilla olevien tietojen perusteella TEMOVATE® emulsiovoiteen ja -voiteen annostusta ei tarvitse muuttaa iäkkäillä potilailla.
YLIANNOSTUS
Paikallisesti levitetty TEMOVATE®-voide ja -voide voidaan imeytyä riittävä määrä systeemisten vaikutusten aikaansaamiseksi (ks. VAROTOIMENPITEET ).
VASTA-AIHEET
TEMOVATE® (klobetasolipropionaattivoide ja -voide) Cream ja Ointment, 0,05% ovat vasta-aiheisia potilaille, joilla on aiemmin ollut yliherkkyyttä jollekin valmisteen aineosalle.
KLIININEN FARMAKOLOGIA
Kuten muillakin paikallisilla kortikosteroideilla, klobetasolipropionaatilla on anti-inflammatorisia, kutinaa estäviä ja verisuonia supistavia ominaisuuksia. Paikallisten steroidien anti-inflammatorisen vaikutuksen mekanismi on yleensä epäselvä. Kortikosteroidien uskotaan kuitenkin toimivan indusoimalla fosfolipaasi A2:ta estäviä proteiineja, joita kutsutaan yhteisesti lipokortiineiksi. Oletetaan, että nämä proteiinit säätelevät voimakkaiden tulehduksen välittäjien, kuten prostaglandiinien ja leukotrieenien, biosynteesiä estämällä niiden yhteisen esiasteen, arakidonihapon, vapautumista. Fosfolipaasi A2 vapauttaa arakidonihappoa kalvon fosfolipideistä.
Farmakokinetiikka
Paikallisten kortikosteroidien ihon kautta tapahtuvan imeytymisen laajuus määräytyy monien tekijöiden mukaan, mukaan lukien vehikkeli ja epidermaalisen esteen eheys. Enintään 24 tuntia kestävän okklusiivisen sidoksen ei ole osoitettu lisäävän tunkeutumista; hydrokortisonin tukkeutuminen 96 tunnin ajaksi parantaa kuitenkin merkittävästi tunkeutumista. Paikalliset kortikosteroidit voivat imeytyä normaalista ehjästä ihosta. Ihon tulehdus ja/tai muut sairausprosessit voivat lisätä ihon kautta tapahtuvaa imeytymistä.
TEMOVATE® Cream and Ointment -voiteella tehdyt tutkimukset osoittavat, että niiden teho on erittäin korkea verrattuna muihin paikallisiin kortikosteroideihin.
POTILASTIEDOT
Paikallisia kortikosteroideja käyttävien potilaiden tulee saada seuraavat tiedot ja ohjeet:
