Microzide 25mg Hydrochlorothiazide Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Microzide 25mg on ja miten sitä käytetään?
Microzide on reseptilääke, jota käytetään korkean verenpaineen (hypertension) ja turvotuksen (ödeeman) oireiden hoitoon. Microzidea voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Microzide kuuluu lääkeluokkaan, jota kutsutaan diureetteiksi, tiatsidiksi.
Ei tiedetä, onko Microzide turvallinen ja tehokas alle 6 kuukauden ikäisille lapsille.
Mitkä ovat Microziden mahdolliset sivuvaikutukset?
Microzide voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- huimaus,
- silmäkipu,
- näköongelmia,
- ihon tai silmien keltaisuus (keltatauti),
- kalpea iho,
- helppo mustelma,
- epätavallinen verenvuoto (nenä, suu, emätin tai peräsuolen),
- hengenahdistus,
- hengityksen vinkuminen,
- yskä, jossa on vaahtoavaa limaa,
- rintakipu,
- kuiva suu,
- jano,
- uneliaisuus,
- energian puute,
- levottomuus,
- lihaskipu tai -heikkous,
- nopea syke,
- pahoinvointi,
- oksentelua,
- vähän tai ei ollenkaan virtsaa,
- kuume,
- kipeä kurkku,
- turvotus kasvoissasi tai kielessäsi,
- polttaa silmissäsi ja
- ihokipu, jota seuraa punainen tai violetti ihottuma, joka leviää (etenkin kasvoille tai ylävartalolle) ja aiheuttaa rakkuloita ja hilseilyä
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Microziden yleisimmät sivuvaikutukset ovat:
- pahoinvointi,
- oksentelua,
- ruokahalun menetys,
- ripuli,
- ummetus,
- lihaskouristus,
- huimaus ja
- päänsärky
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikkia Microziden mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Soita lääkärillesi saadaksesi lääketieteellisiä neuvoja sivuvaikutuksista. Voit ilmoittaa sivuvaikutuksista FDA:lle numerossa 1-800-FDA-1088.
KUVAUS
MICROZIDE® (hydroklooritiatsidi, USP 12,5 mg) on klooritiatsidin 3,4-dihydrojohdannainen. Sen kemiallinen nimi on 6-kloori-3,4-dihydro-2H-1,2,4-bentsotiadiatsiini-7-sulfonamidi-1,1-dioksidi. Sen empiirinen kaava on C7H8CIN304S2; sen molekyylipaino on 297,74; ja sen rakennekaava on:
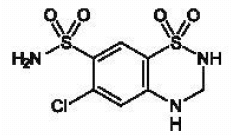
Se on valkoinen tai käytännössä valkoinen kiteinen jauhe, joka liukenee heikosti veteen, mutta liukenee vapaasti natriumhydroksidiliuokseen.
MICROZIDE (hydroklooritiatsidikapseli) toimitetaan 12,5 mg:n kapseleina oraaliseen käyttöön.
Inaktiiviset ainesosat : kolloidinen piidioksidi, maissitärkkelys, laktoosimonohydraatti, magnesiumstearaatti. Gelatiinikapselit sisältävät D&C Red No. 28, D&C Yellow No. 10, FD&C Blue No. 1, gelatiini, titaanidioksidi. Kapselit on painettu syötävällä musteella, joka sisältää mustaa rautaoksidia, D&C Yellow No. 10, FD&C Blue No. 1, FD&C Blue No. 2, FD&C Red No. 40.
INDIKAATIOT
MICROZIDE (hydroklooritiatsidikapseli) on tarkoitettu verenpaineen hoitoon joko ainoana terapeuttisena aineena tai yhdessä muiden verenpainelääkkeiden kanssa. Toisin kuin kaliumia säästävät yhdistelmädiureetit, MICROZIDE-valmistetta (hydroklooritiatsidikapselia) voidaan käyttää potilailla, joilla hyperkalemian kehittymistä ei voida vaarantaa, mukaan lukien ACE:n estäjiä käyttävät potilaat.
Käyttö raskauden aikana
Diureettien rutiinikäyttö muuten terveellä naisella on sopimatonta ja altistaa äidin ja sikiön tarpeettomalle vaaralle. Diureetit eivät estä raskauden toksemian kehittymistä, eikä ole olemassa tyydyttäviä todisteita niiden käyttökelpoisuudesta kehittyneen toksemian hoidossa.
Raskaudenaikainen turvotus voi johtua patologisista syistä tai raskauden fysiologisista ja mekaanisista seurauksista. Diureetit on tarkoitettu raskauden aikana, kun turvotus johtuu patologisista syistä, aivan kuten ne ovat myös raskauden puuttuessa. Riippuvainen turvotus raskauden aikana, joka johtuu laajentuneen kohdun aiheuttamasta laskimoiden palautumisesta, hoidetaan asianmukaisesti nostamalla alaraajoja ja käyttämällä tukiletkua; diureettien käyttö suonensisäisen tilavuuden pienentämiseksi on tässä tapauksessa epäloogista ja tarpeetonta. Normaalin raskauden aikana esiintyy hypervolemiaa, joka ei ole haitallista sikiölle eikä äidille (sydän- ja verisuonitautien puuttuessa), mutta johon liittyy turvotusta, mukaan lukien yleistynyt turvotus useimmilla raskaana olevilla naisilla. Jos tämä turvotus aiheuttaa epämukavuutta, lisääntynyt makuuase tarjoaa usein helpotusta. Harvinaisissa tapauksissa tämä turvotus voi aiheuttaa äärimmäistä epämukavuutta, jota lepo ei helpota. Näissä tapauksissa lyhyt diureettihoito saattaa helpottaa ja olla tarkoituksenmukaista.
ANNOSTELU JA HALLINNOINTI
Hypertension hallintaan : MICROZIDEn (hydroklooritiatsidikapseli) aikuisten aloitusannos on yksi kapseli kerran päivässä joko yksinään tai yhdessä muiden verenpainelääkkeiden kanssa. Yli 50 mg:n päivittäisiä kokonaisannoksia ei suositella.
MITEN TOIMITETAAN
MICROZIDE (hydroklooritiatsidikapseli) -kapselit ovat #4 Teal Opaque/Teal Opaque kaksiosaisia kovia gelatiinikapseleita, joihin on painettu MICROZIDE (hydrochlorothiazide-kapseli) ja 12,5 mg mustalla musteella. Ne toimitetaan 100 pulloissa lapsiturvallisilla sulkimilla ( NDC 52544-622-01).
Annostele tiiviissä, valonkestävässä astiassa USP:n mukaisesti.
Pitää poissa lasten ulottuvilta.
Säilytä 20°-25°C (68°-77°F). [Katso USP-ohjattu huonelämpötila.] Suojaa valolta, kosteudelta, jäätymiseltä, -20°C (-4°F). Pidä säiliö tiiviisti suljettuna.
Osoita lääketieteelliset tiedustelut: WATSON., Medical Communications PO Box 1953, Morristown, NJ 07962-1953. 800-272-5525. Valmistaja: Watson Pharma Private Limited. Verna, Salcette, Goa 403 722 INTIA. Jakelija: Watson Pharma, Inc. Morristown, NJ 07962 USA. Tarkistettu: helmikuussa 2011
SIVUVAIKUTUKSET
Hydroklooritiatsidiin liittyvien haittavaikutusten on osoitettu olevan annosriippuvaisia. Kontrolloiduissa kliinisissä tutkimuksissa 12,5 mg:n hydroklooritiatsidiannoksella kerran vuorokaudessa raportoidut haittatapahtumat olivat verrattavissa lumelääkkeeseen. Seuraavat haittavaikutukset on raportoitu vähintään 25 mg:n hydroklooritiatsidiannoksilla, ja ne on lueteltu kunkin luokan sisällä alenevassa järjestyksessä.
Runko kokonaisuutena : Heikkous.
Kardiovaskulaarinen : Hypotensio, mukaan lukien ortostaattinen hypotensio (alkoholi, barbituraatit, huumeet tai verenpainelääkkeet voivat pahentaa sitä).
Ruoansulatus Haimatulehdus, keltaisuus (intrahepaattinen kolestaattinen keltaisuus), ripuli, oksentelu, sialadeniitti, kouristukset, ummetus, mahalaukun ärsytys, pahoinvointi, anoreksia.
Hematologinen : Aplastinen anemia, agranulosytoosi, leukopenia, hemolyyttinen anemia, trombosytopenia.
Yliherkkyys : Anafylaktiset reaktiot, nekrotisoiva angiiitti (vaskuliitti ja ihovaskuliitti), hengitysvaikeudet mukaan lukien keuhkotulehdus ja keuhkopöhö, valoherkkyys, kuume, urtikaria, ihottuma, purppura.
Metabolinen : Elektrolyyttitasapainohäiriö (katso VAROTOIMENPITEET ), hyperglykemia, glykosuria, hyperurikemia.
Tuki- ja liikuntaelimistön : Lihaskouristus.
Hermosto/Psykiatrinen : Huimaus, parestesia, huimaus, päänsärky, levottomuus.
Munuaiset : Munuaisten vajaatoiminta, munuaisten vajaatoiminta, interstitiaalinen nefriitti (ks VAROITUKSET ).
Iho : Erythema multiforme, mukaan lukien Stevens-Johnsonin oireyhtymä, eksfoliatiivinen dermatiitti mukaan lukien toksinen epidermaalinen nekrolyysi, hiustenlähtö.
Erityiset aistit Ohimenevä näön hämärtyminen, ksanthopsia.
Urogenitaalinen : Impotenssi.
Aina kun haittavaikutukset ovat kohtalaisia tai vakavia, tiatsidiannostusta tulee pienentää tai hoito lopettaa.
HUUMEIDEN VUOROVAIKUTUKSET
Seuraavilla lääkkeillä voi olla yhteisvaikutuksia tiatsididiureettien kanssa, kun niitä annetaan samanaikaisesti:
Alkoholi, barbituraatit tai huumeet - ortostaattinen hypotensio voi voimistua.
Diabeteslääkkeet - (oraaliset lääkkeet ja insuliini) diabeteslääkkeen annoksen muuttaminen saattaa olla tarpeen.
Muut verenpainelääkkeet - lisävaikutus tai tehostaminen.
Kolestyramiini ja kolestipolihartsit - Kolestyramiini ja kolestipolihartsit sitovat hydroklooritiatsidia ja vähentävät sen imeytymistä maha-suolikanavasta jopa 85 ja kolestipolihartsit vastaavasti 43 prosenttia.
Kortikosteroidi, ACTH - voimistunut elektrolyyttivajaus, erityisesti hypokalemia.
Painetta aiheuttavat amiinit (esim. norepinefriini) - mahdollinen heikentynyt vaste paineita aiheuttaville amiineille, mutta ei riitä estämään niiden käyttöä.
Luuston lihasrelaksantit, ei-depolarisoivat (esim. tubokurariini) mahdollinen lisääntynyt vaste lihasrelaksantille.
Litium - Ei yleensä tule antaa diureettien kanssa. Diureetit vähentävät litiumin munuaispuhdistumaa ja lisäävät huomattavasti litiumtoksisuuden riskiä. Katso litiumvalmisteiden pakkausseloste ennen tällaisten valmisteiden käyttöä MICROZIDEn (hydroklooritiatsidikapselin) kanssa.
Ei-steroidiset tulehduskipulääkkeet - Joillakin potilailla ei-steroidisten tulehduskipulääkkeiden antaminen voi vähentää loop-, kaliumia säästävien ja tiatsididiureettien diureettisia, natriureettisia ja verenpainetta alentavia vaikutuksia. Kun MICROZIDE-valmistetta (hydroklooritiatsidikapseli) ja ei-steroidisia tulehduskipulääkkeitä käytetään samanaikaisesti, potilaita tulee tarkkailla tarkasti sen määrittämiseksi, saavutetaanko diureetin haluttu vaikutus.
Lääke/laboratoriotestien vuorovaikutukset
Tiatsidihoito tulee lopettaa ennen lisäkilpirauhasen toimintakokeiden suorittamista (ks VAROTOIMET, Yleistä ).
VAROITUKSET
Diabetes ja hypoglykemia: Piilevä diabetes mellitus saattaa ilmaantua, ja tiatsideja saavien diabeetikkojen insuliiniannosta on ehkä muutettava.
Munuaissairaus: Tiatsidien kumulatiiviset vaikutukset voivat kehittyä potilailla, joilla on munuaisten vajaatoiminta. Tällaisilla potilailla tiatsidit voivat aiheuttaa atsotemiaa.
VAROTOIMENPITEET
Elektrolyytti- ja nestetasapainon tila
Julkaistuissa tutkimuksissa kliinisesti merkittävä hypokalemia on ollut jatkuvasti harvinaisempaa potilailla, jotka ovat saaneet 12,5 mg hydroklooritiatsidia, kuin potilailla, jotka ovat saaneet suurempia annoksia. Tästä huolimatta seerumin elektrolyyttipitoisuudet on määritettävä säännöllisesti potilailla, joilla saattaa olla hypokalemian kehittymisen riski. Potilaita tulee tarkkailla neste- tai elektrolyyttihäiriöiden, kuten hyponatremia, hypokloreeminen alkaloosi, hypokalemia ja hypomagnesemia, varalta.
Neste- ja elektrolyyttitasapainohäiriön varoitusmerkkejä tai oireita ovat suun kuivuminen, jano, heikkous, letargia, uneliaisuus, levottomuus, lihaskivut tai -krampit, lihasväsymys, hypotensio, oliguria, takykardia ja ruoansulatuskanavan häiriöt, kuten pahoinvointi ja oksentelu.
Hypokalemia voi kehittyä, etenkin nopean diureesin yhteydessä, kun kyseessä on vaikea kirroosi, samanaikaisesti käytettäessä kortikosteroidia tai adrenokortikotrooppista hormonia (ACTH) tai pitkäaikaisen hoidon jälkeen. Riittävän suun elektrolyyttien saannin häiriintyminen edistää myös hypokalemiaa. Hypokalemia ja hypomagnesemia voivat aiheuttaa kammioiden rytmihäiriöitä tai herkistää tai liioitella sydämen vastetta digitaliksen toksisiin vaikutuksiin. Hypokalemiaa voidaan välttää tai hoitaa kaliumlisällä tai lisäämällä kaliumia sisältävien elintarvikkeiden saantia.
Laimeneva hyponatremia on hengenvaarallinen ja sitä voi esiintyä turvotuilla potilailla kuumalla säällä; sopiva hoito on veden rajoittaminen suolan antamisen sijaan, paitsi harvoissa tapauksissa, joissa hyponatremia on hengenvaarallinen. Varsinaisessa suolavajeessa sopiva korvaus on valinnanvarainen hoito.
Hyperurikemia
Tietyillä tiatsididiureetteja saavilla potilailla saattaa esiintyä hyperurikemiaa tai akuuttia kihtiä.
Maksan vajaatoiminta
Tiatsideja tulee käyttää varoen potilailla, joilla on maksan vajaatoiminta. Ne voivat aiheuttaa maksakooman potilailla, joilla on vaikea maksasairaus.
Lisäkilpirauhasen sairaus
Tiatsidit vähentävät kalsiumin erittymistä, ja muutamilla potilailla, jotka ovat saaneet pitkäaikaista tiatsidihoitoa, on havaittu patologisia muutoksia lisäkilpirauhasissa, joihin liittyy hyperkalsemiaa ja hypofosfatemiaa.
Karsinogeneesi, mutageneesi, hedelmällisyyden heikkeneminen
Kansallisen toksikologian ohjelman (NTP) alaisuudessa tehdyt kaksivuotiset ruokintatutkimukset hiirillä ja rotilla eivät paljastaneet näyttöä hydroklooritiatsidin syöpää aiheuttavasta potentiaalista naarashiirillä (annoksilla noin 600 mg/kg/vrk) tai uroksilla. ja naarasrotilla (annoksilla noin 100 mg/kg/vrk). NTP löysi kuitenkin kiistanalaisia todisteita hepatokarsinogeenisuudesta uroshiirillä. Hydroklooritiatsidi ei ollut genotoksinen in vitro Salmonella typhimurium -kantojen TA 98, TA 100, TA 1535, TA 1537 ja TA 1538 Amesin mutageenisuuskokeessa eikä kiinalaisen hamsterin munasarjan (CHO) testissä kromosomien in vivoation tai aberation in aberration hiiren itusolujen kromosomit, kiinanhamsterin luuytimen kromosomit ja Drosophilan sukupuoleen liittyvä resessiivinen tappava piirregeeni. Positiivisia testituloksia saatiin vain in vitro CHO Sister Chromatid Exchange (klastogeenisuus) ja hiiren lymfoomasolutesteissä (mutageenisuus), joissa käytettiin hydroklooritiatsidin pitoisuuksia 43 - 1300 mcg/ml, ja Aspergillus nidulans non-disjunktion -määrityksessä. määrittelemätön pitoisuus.
Hydroklooritiatsidilla ei ollut haitallisia vaikutuksia kummankaan sukupuolen hiirten ja rottien hedelmällisyyteen tutkimuksissa, joissa nämä lajit altistettiin ruokavalionsa kautta annoksille, jotka olivat 100 ja 4 mg/kg, vastaavasti ennen hedelmöittymistä ja koko tiineyden ajan.
Raskaus
Teratogeeniset vaikutukset
Raskausluokka B: Tutkimuksissa, joissa hydroklooritiatsidia annettiin suun kautta raskaana oleville hiirille ja rotille niiden merkittävien organogeneesijaksojen aikana annoksina 3 000 ja 1 000 mg hydroklooritiatsidia/kg, ei saatu näyttöä sikiölle aiheutuvasta haitasta.
Ei kuitenkaan ole olemassa riittäviä ja hyvin kontrolloituja tutkimuksia raskaana olevilla naisilla. Koska eläinten lisääntymistutkimukset eivät aina ennusta ihmisen vastetta, tätä lääkettä tulee käyttää raskauden aikana vain, jos se on selvästi tarpeen.
Ei-teratogeeniset vaikutukset
Tiatsidit läpäisevät istukan ja näkyvät napanuoraveressä. On olemassa sikiön tai vastasyntyneen keltaisuuden, trombosytopenian ja mahdollisesti muiden aikuisilla esiintyneiden haittavaikutusten riski.
Imettävät äidit
Tiatsidit erittyvät äidinmaitoon. Koska imeväisille voi aiheutua vakavia haittavaikutuksia, on päätettävä, lopetetaanko imetys vai hydroklooritiatsidihoito ottaen huomioon lääkkeen merkitys äidille.
Käyttö lapsille
Turvallisuutta ja tehokkuutta lapsipotilailla ei ole osoitettu.
Vanhusten käyttö
Hydroklooritiatsidia käytettäessä iäkkäillä (eli yli 65-vuotiailla) voidaan havaita voimakkaampaa verenpaineen laskua ja haittavaikutusten lisääntymistä. Siksi hoidon aloittamista pienimmällä saatavilla olevalla hydroklooritiatsidiannoksella (12,5 mg) suositellaan. Jos lisätitrausta tarvitaan, on käytettävä 12,5 mg:n lisäyksiä.
YLIANNOSTUS
Yleisimmät havaitut merkit ja oireet ovat elektrolyyttivajauksesta (hypokalemia, hypokloremia, hyponatremia) ja liiallisesta diureesista johtuvasta nestehukasta johtuvat oireet. Jos myös digitalista on annettu, hypokalemia voi pahentaa sydämen rytmihäiriöitä.
Yliannostustapauksissa tulee käyttää oireenmukaisia ja tukitoimenpiteitä. Oksentelu tulee aiheuttaa tai mahahuuhtelu. Korjaa nestehukka, elektrolyyttitasapaino, maksakooma ja hypotensio vakiintuneiden menetelmien mukaisesti. Tarvittaessa anna happea tai tekohengitystä hengitysvamman vuoksi. Sitä, missä määrin hydroklooritiatsidi poistuu hemodialyysillä, ei ole varmistettu.
Hydroklooritiatsidin suun LD50 on yli 10 g/kg hiirellä ja rotalla.
VASTA-AIHEET
Hydroklooritiatsidi on vasta-aiheinen potilailla, joilla on anuria. Yliherkkyys tälle tuotteelle tai muille sulfonamidijohdannaisille on myös vasta-aiheinen.
KLIININEN FARMAKOLOGIA
Hydroklooritiatsidi estää natrium- ja kloridi-ionien reabsorption ja lisää siten distaalisen tubuluksen läpi kulkevan natriumin määrää ja erittyvän veden määrää. Osa distaalitiehyessä olevasta lisänatriumista vaihdetaan siellä kalium- ja vetyioneiksi. Hydroklooritiatsidin jatkuvan käytön ja natriumin vähenemisen myötä kompensaatiomekanismit pyrkivät lisäämään tätä vaihtoa ja voivat aiheuttaa liiallista kalium-, vety- ja kloridi-ionien menetystä. Hydroklooritiatsidi vähentää myös kalsiumin ja virtsahapon erittymistä, voi lisätä jodidin erittymistä ja saattaa hidastaa glomerulusten suodatusnopeutta. Hydroklooritiatsidin aiheuttamiin liiallisiin elektrolyyttimuutoksiin liittyvien aineenvaihduntatoksisuuden on osoitettu olevan annosriippuvaisia.
Farmakokinetiikka ja aineenvaihdunta
Hydroklooritiatsidi imeytyy hyvin (65–75 %) suun kautta annetun annon jälkeen. Hydroklooritiatsidin imeytyminen on heikentynyt potilailla, joilla on kongestiivinen sydämen vajaatoiminta.
Plasman huippupitoisuudet havaitaan 1–5 tunnin kuluessa annostelusta, ja ne vaihtelevat 70–490 ng/ml 12,5–100 mg:n oraalisten annosten jälkeen. Plasman pitoisuudet ovat lineaarisessa suhteessa annettuun annokseen. Hydroklooritiatsidin pitoisuus kokoveressä on 1,6-1,8 kertaa suurempi kuin plasmassa. Sitoutumisen seerumin proteiineihin on raportoitu olevan noin 40-68 %. Plasman eliminaation puoliintumisajan on raportoitu olevan 6-15 tuntia. Hydroklooritiatsidi eliminoituu pääasiassa munuaisten kautta. Suun kautta annettujen 12,5–100 mg:n annosten jälkeen 55–77 % annetusta annoksesta erittyy virtsaan ja yli 95 % imeytyneestä annoksesta erittyy virtsaan muuttumattomana lääkkeenä. Potilailla, joilla on munuaissairaus, plasman hydroklooritiatsidipitoisuudet suurenevat ja eliminaation puoliintumisaika pitenee.
Kun MICROZIDE (hydroklooritiatsidikapseli) annetaan ruoan kanssa, sen hyötyosuus pienenee 10 %, plasman maksimipitoisuus pienenee 20 % ja aika huippupitoisuuteen kasvaa 1,6 tunnista 2,9 tunnista.
Farmakodynamiikka
Tiatsidien akuuttien verenpainetta alentavien vaikutusten uskotaan johtuvan veritilavuuden ja sydämen minuuttitilavuuden vähenemisestä natriureettisen vaikutuksen seurauksena, vaikka suoraa verisuonia laajentavaa mekanismia onkin ehdotettu. Kroonisessa annossa plasman tilavuus palautuu normaaliksi, mutta perifeerinen verisuonivastus pienenee. Hydroklooritiatsidin verenpainetta alentavan vaikutuksen tarkkaa mekanismia ei tunneta.
Tiatsidit eivät vaikuta normaaliin verenpaineeseen. Vaikutus alkaa 2 tunnin kuluessa annostelusta, huippuvaikutus havaitaan noin 4 tunnin kuluttua ja aktiivisuus säilyy jopa 24 tuntia.
Kliiniset tutkimukset
87 potilaan 4 viikon kaksoissokkoutetussa, lumekontrolloidussa rinnakkaisryhmätutkimuksessa potilailla, jotka saivat MICROZIDEA (hydroklooritiatsidikapselia), systolinen ja diastolinen verenpaine laskivat merkittävästi enemmän kuin lumelääkettä saaneilla potilailla. Julkaistuissa lumekontrolloiduissa tutkimuksissa, joissa verrattiin 12,5 mg hydroklooritiatsidia 25 mg:aan, 12,5 mg:n annos säilytti suurimman osan lumelääkekorjatusta verenpaineen laskusta, joka havaittiin 25 mg:lla.
POTILASTIEDOT
Tietoja ei ole annettu. Katso VAROITUKSET ja VAROTOIMENPITEET osiot.
