Alesse 0.15/0.03mg Levonorgestrel Käyttö, sivuvaikutukset ja annostus. Hinta verkkoapteekissa. Geneeriset lääkkeet ilman reseptiä.
Mitä Alesse on ja miten sitä käytetään?
Alesse 0,15 mg on reseptilääke, jota käytetään raskauden ehkäisyyn. Alessea voidaan käyttää yksinään tai muiden lääkkeiden kanssa.
Alesse kuuluu lääkeluokkaan, jota kutsutaan estrogeeniksi/progestiiniksi; Ehkäisyvälineet, Oraaliset.
Ei tiedetä, onko Alesse turvallinen ja tehokas lapsilla ennen kuukautisia.
Mitkä ovat Alessen mahdolliset sivuvaikutukset?
Alesse voi aiheuttaa vakavia sivuvaikutuksia, mukaan lukien:
- äkillinen tunnottomuus tai heikkous,
- kova päänsärky,
- sammaltava puhe,
- tasapainoongelmia,
- äkillinen näönmenetys,
- pistävä rintakipu,
- hengenahdistus,
- yskii verta,
- turvotus tai punoitus käsivarressa tai jalassa,
- rintakipu tai paine,
- kipu leviää leukaan tai olkapäähän,
- pahoinvointi,
- hikoilu,
- ruokahalun menetys,
- ylävatsakipu,
- väsymys,
- kuume,
- tumma virtsa,
- savenväriset ulosteet,
- ihon tai silmien keltaisuus (keltatauti),
- näön hämärtyminen,
- hakkaa niskassasi tai korvissasi,
- turvotus käsissäsi, nilkoissasi tai jaloissasi,
- muutokset migreenipäänsäryn rakenteessa tai vaikeusasteessa,
- rintojen kyhmy,
- unihäiriöt,
- heikkous,
- väsymys ja
- mielialan muutoksia
Hakeudu välittömästi lääkärin hoitoon, jos sinulla on jokin yllä mainituista oireista.
Alessen yleisimpiä sivuvaikutuksia ovat:
- pahoinvointi,
- oksentelua,
- rintojen arkuus,
- läpimurtoverenvuoto,
- akne,
- kasvojen ihon tummuminen,
- painonnousu ja
- ongelmia piilolinssien kanssa
Kerro lääkärille, jos sinulla on haittavaikutuksia, jotka häiritsevät sinua tai jotka eivät häviä.
Nämä eivät ole kaikki Alessen mahdollisia sivuvaikutuksia. Lisätietoja saat lääkäriltäsi tai apteekista.
Potilaita tulee neuvoa, että suun kautta otettavat ehkäisyvalmisteet eivät suojaa HIV:n (AIDS) ja muiden sukupuolitautien, kuten klamydian, sukupuolielinten herpesen, sukupuolielinten syylien, tippurien, hepatiitti B:n ja kupan, tarttumiselta.
KUVAUS
21 vaaleanpunaista aktiivista tablettia, joista jokainen sisältää 0,10 mg levonorgestreeliä, d(-)-13β-etyyli-17α-etinyyli-17β-hydroksigon-4-en-3-onia, täysin synteettistä progestiinia ja 0,02 mg etinyyliestradiolia, 17α- etinyyli-1,3,5(10)-estratrieeni-3,17p-dioli. Inaktiivisia aineosia ovat selluloosa, hypromelloosi, rautaoksidi, laktoosi, magnesiumstearaatti, polakriliinikalium, polyetyleeniglykoli, titaanidioksidi ja montaaniesterivaha.
7 vaaleanvihreää inerttiä tablettia, joista jokainen sisältää selluloosaa, FD&C sininen nro. 1, hypromelloosi, rautaoksidi, laktoosi, magnesiumstearaatti, polakriliinikalium, polyetyleeniglykoli, titaanidioksidi ja montaaniesterivaha.
INDIKAATIOT
ALESSE (levonorgestreeli ja etinyyliestradioli) on tarkoitettu raskauden ehkäisyyn naisille, jotka haluavat käyttää ehkäisymenetelmänä oraalisia ehkäisyvalmisteita.
Suun kautta otettavat ehkäisyvalmisteet ovat erittäin tehokkaita. Taulukossa II on lueteltu tyypilliset vahingossa tapahtuneiden raskauksien määrä oraalisten yhdistelmäehkäisyvalmisteiden ja muiden ehkäisymenetelmien käyttäjillä. Näiden ehkäisymenetelmien tehokkuus sterilointia, kierukkaa ja Norplant® Systemiä lukuun ottamatta riippuu niiden käytön luotettavuudesta. Menetelmien oikea ja johdonmukainen käyttö voi johtaa pienempään epäonnistumisasteeseen.
Kliinisessä ALESSE-tutkimuksessa (levonorgestreeli- ja etinyyliestradiolitabletit) 1 477 koehenkilöllä oli 7 720 käyttösykliä ja yhteensä 5 raskautta raportoitiin. Tämä vastaa yleistä raskauslukua 0,84/100 naisvuotta. Tämä luku sisältää potilaat, jotka eivät ottaneet lääkettä oikein. Yksi tai useampi pilleri jäi väliin 1 479 (18,8 %) aikana 7 870 syklistä; näin ollen kaikki tabletit otettiin 6 391 (81,2 %) aikana 7 870 syklistä. Yhteensä 7 870 syklistä yhteensä 150 sykliä jätettiin Pearl-indeksin laskennan ulkopuolelle varaehkäisyn käytön ja/tai kolmen tai useamman peräkkäisen pillerin puuttumisen vuoksi.
ANNOSTELU JA HALLINNOINTI
Maksimaalisen ehkäisytehon saavuttamiseksi ALESSE® (levonorgestreeli- ja etinyyliestradiolitabletit) on otettava täsmälleen ohjeiden mukaisesti ja enintään 24 tunnin välein. ALESSE (levonorgestreeli ja etinyyliestradioli) -28:n annos on yksi vaaleanpunainen tabletti päivässä 21 peräkkäisenä päivänä, jota seuraa yksi vaaleanvihreä inertti tabletti päivässä 7 peräkkäisenä päivänä määrätyn aikataulun mukaisesti. On suositeltavaa, että ALESSE (levonorgestreeli ja etinyyliestradioli) -28 tablettia otetaan samaan aikaan joka päivä.
Annostelija tulee säilyttää mukana toimitetussa lompakossa, jotta pillerit eivät haalistu. Jos pillerit haalistuvat, potilaiden tulee jatkaa niiden ottamista ohjeiden mukaan.
Ensimmäisen käyttöjakson aikana
Ovulaation ja hedelmöittymisen mahdollisuus tulee ottaa huomioon ennen lääkityksen aloittamista. Potilasta tulee neuvoa aloittamaan ALESSEN (levonorgestreeli ja etinyyliestradioli) ottaminen joko ensimmäisenä sunnuntaina kuukautisten alkamisen jälkeen (sunnuntai alkaa) tai ensimmäisenä kuukautispäivänä (päivän 1 aloitus).
Sunnuntai aloitus
Potilasta neuvotaan aloittamaan ALESSE (levonorgestreeli ja etinyyliestradioli) -28 -hoidon ensimmäisenä sunnuntaina kuukautisten alkamisen jälkeen. Jos kuukautiset alkavat sunnuntaina, ensimmäinen tabletti (vaaleanpunainen) otetaan samana päivänä. Yksi vaaleanpunainen tabletti tulee ottaa päivittäin 21 peräkkäisenä päivänä ja sen jälkeen yksi vaaleanvihreä inertti tabletti päivittäin 7 peräkkäisenä päivänä. Vetovuoto tulee yleensä ilmaantua 3 päivän kuluessa vaaleanpunaisten tablettien käytön lopettamisesta, eikä se välttämättä ole loppunut ennen seuraavan pakkauksen aloittamista. Ensimmäisen syklin aikana ehkäisyä ei pidä käyttää ALESSE (levonorgestreeli ja etinyyliestradioli) -28, ennen kuin vaaleanpunainen tabletti on otettu päivittäin 7 peräkkäisenä päivänä, ja näiden 7 päivän aikana tulee käyttää ei-hormonaalista ehkäisymenetelmää. päivää.
Päivä 1 alkaa
Ensimmäisen lääkitysjakson aikana potilasta neuvotaan aloittamaan ALESSE (levonorgestreeli ja etinyyliestradioli) -28 ottaminen kuukautistensa ensimmäisen 24 tunnin aikana (kuukautiskierron ensimmäinen päivä). Yksi vaaleanpunainen tabletti tulee ottaa päivittäin 21 peräkkäisenä päivänä ja sen jälkeen yksi vaaleanvihreä inertti tabletti päivittäin 7 peräkkäisenä päivänä. Vetovuoto tulee yleensä ilmaantua 3 päivän kuluessa vaaleanpunaisten tablettien käytön lopettamisesta, eikä se välttämättä ole loppunut ennen seuraavan pakkauksen aloittamista. Jos lääkitys aloitetaan kuukautiskierron ensimmäisenä päivänä, varaehkäisyä ei tarvita. Jos ALESSE (levonorgestreeli ja etinyyliestradioli) -28 tabletti aloitetaan myöhemmin kuin ensimmäisen kuukautiskierron ensimmäisenä päivänä tai synnytyksen jälkeen, ehkäisyä ei tulisi käyttää ALESSE (levonorgestreeli ja etinyyliestradioli) -28 tablettiin ennen kuin 7 ensimmäisen peräkkäisen päivän jälkeen. Näiden 7 päivän aikana tulee käyttää ei-hormonaalista ehkäisymenetelmää.
Ensimmäisen käyttökerran jälkeen
Potilas aloittaa seuraavan ja kaikki seuraavat tablettihoitonsa seuraavana päivänä viimeisen vaaleanvihreän tabletin ottamisen jälkeen. Hänen tulee noudattaa samaa annostusaikataulua: 21 päivää vaaleanpunaisilla tableteilla ja sen jälkeen 7 päivää vaaleanvihreillä tableteilla. Jos jossakin syklissä potilas aloittaa tablettien käytön myöhemmin kuin oikeana päivänä, hänen tulee suojautua raskaudelta käyttämällä ei-hormonaalista ehkäisymenetelmää, kunnes hän on ottanut vaaleanpunaisen tabletin päivittäin 7 peräkkäisenä päivänä.
Vaihtaminen toisesta hormonaalisesta ehkäisymenetelmästä
Kun potilas on vaihtamassa 21 päivän tablettihoitoa, hänen tulee odottaa 7 päivää viimeisen tabletin ottamisen jälkeen ennen kuin hän aloittaa ALESSE-hoidon (levonorgestreeli ja etinyyliestradioli). Hän kokee todennäköisesti vieroitusverenvuotoa tämän viikon aikana. Hänen tulee olla varma, että hänen edellisen 21 päivän hoito-ohjelmansa jälkeen ei kulu enempää kuin 7 päivää. Kun potilas on siirtymässä 28 päivän tablettihoitoon, hänen tulee aloittaa ensimmäinen ALESSE-pakkaus (levonorgestreeli ja etinyyliestradioli) viimeisen tabletin jälkeisenä päivänä. Hänen ei pitäisi odottaa päivääkään pakkausten välillä. Potilas voi vaihtaa vain progestiinia sisältävästä pilleristä minä päivänä tahansa, ja hänen tulee aloittaa ALESSE (levonorgestreeli ja etinyyliestradioli) seuraavana päivänä. Jos potilas siirtyy implantista tai injektiosta, potilaan tulee aloittaa ALESSE (levonorgestreeli ja etinyyliestradioli) implantin poistopäivänä tai injektiota käytettäessä seuraavana päivänä. Kun potilasta vaihdetaan pelkkää progestiinia sisältävästä pilleristä, injektiosta tai implantista, potilasta tulee neuvoa käyttämään ei-hormonaalista ehkäisymenetelmää ensimmäisten 7 päivän ajan tablettien ottamisesta.
Jos tiputtelu- tai läpäisyvuotoa esiintyy
Jos tiputtelu- tai läpäisyvuotoa ilmenee, potilasta neuvotaan jatkamaan samalla hoito-ohjelmalla. Tämäntyyppinen verenvuoto on yleensä ohimenevää ja merkityksetöntä; Jos verenvuoto on kuitenkin jatkuvaa tai pitkittynyttä, potilasta neuvotaan ottamaan yhteyttä lääkäriin.
Raskauden vaara, jos tabletit unohtuvat ottaa
Vaikka ovulaation todennäköisyys on pieni, jos vain yksi tai kaksi vaaleanpunaista tablettia unohtuvat, ovulaation mahdollisuus kasvaa jokaisena peräkkäisenä päivänä, jona aikataulun mukainen vaaleanpunainen tabletti unohtuu. Vaikka raskauden ilmaantuminen on epätodennäköistä, jos ALESSE:tä (levonorgestreeli ja etinyyliestradioli) otetaan ohjeiden mukaan, on raskauden mahdollisuus otettava huomioon, jos vieroitusvuotoa ei esiinny. Jos potilas ei ole noudattanut määrättyä aikataulua (jäänyt ottamatta yhden tai useamman tabletin tai aloittanut niiden ottamisen päivää myöhemmin kuin olisi pitänyt), tulee raskauden todennäköisyys ottaa huomioon ensimmäisten kuukautisten väliin jäämisen yhteydessä ja ryhtyä asianmukaisiin diagnostisiin toimenpiteisiin. . Jos potilas on noudattanut määrättyä hoito-ohjelmaa ja häneltä jää kaksi peräkkäistä kuukautisia väliin, raskaus on suljettava pois.
Raskauden riski kasvaa jokaisen aktiivisen (vaaleanpunaisen) tabletin unohtuessa. Katso lisätietoja potilaalle unohdetuista tableteista MITÄ TEHDÄ, JOS VÄLITÄÄN PILLEERIT -osiossa YKSITYISKOHTAINEN POTILASMERKINTÄ osio.
Käytä raskauden, abortin tai keskenmenon jälkeen
ALESSE (levonorgestreeli ja etinyyliestradioli) voidaan aloittaa aikaisintaan päivänä 28 synnytyksen jälkeen ei-imettävälle äidille tai toisen raskauskolmanneksen abortin jälkeen tromboembolian lisääntyneen riskin vuoksi (ks. VASTA-AIHEET , VAROITUKSET , ja VAROTOIMENPITEET tromboembolinen sairaus). Potilasta tulee neuvoa käyttämään ei-hormonaalista varamenetelmää ensimmäisten 7 päivän ajan tablettien ottamisesta.
ALESSE (levonorgestreeli ja etinyyliestradioli) voidaan aloittaa välittömästi ensimmäisen raskauskolmanneksen abortin tai keskenmenon jälkeen. Jos potilas aloittaa ALESSE-hoidon (levonorgestreeli ja etinyyliestradioli) välittömästi, varaehkäisyä ei tarvita.
MITEN TOIMITETAAN
ALESSE (levonorgestreeli ja etinyyliestradioli) ®-28 tablettia (0,10 mg levonorgestreeliä ja 0,02 mg etinyyliestradiolia) on saatavana 3 MINI-PACK™-annostelijan pakkauksissa, joissa kussakin 28 tablettia, NDC 0008-2576-02 seuraavasti:
21 aktiivista tablettia, NDC 0008-0912, vaaleanpunainen, pyöreä tabletti, jossa on merkinnät "W" ja "912".
7 inerttiä tablettia, NDC 0008-0650, vaaleanvihreä, pyöreä tabletti, jossa on merkinnät "W" ja "650".
Säilytä kontrolloidussa huoneenlämmössä 20–25 °C (68–77 °F).
Viitteet saatavilla pyynnöstä.
Wyeth Pharmaceuticals Inc., Philadelphia, PA 19101, tammikuu 2008.
SIVUVAIKUTUKSET
Seuraavien vakavien haittavaikutusten lisääntynyt riski (ks VAROITUKSET Lisätietoja) on liitetty ehkäisytablettien käyttöön: Tromboemboliset ja tromboottiset häiriöt ja muut verisuoniongelmat (mukaan lukien tromboflebiitti ja laskimotukos keuhkoembolialla tai ilman, suoliliepeen tromboosi, valtimotromboembolia, sydäninfarkti, aivoverenvuoto, aivoveritulppa) , lisääntymiselimien ja rintojen syöpä, maksan neoplasia (mukaan lukien maksan adenoomat tai hyvänlaatuiset maksakasvaimet), silmävauriot (mukaan lukien verkkokalvon verisuonitukos), sappirakon sairaus, hiilihydraatti- ja lipidivaikutukset, kohonnut verenpaine ja päänsärky, mukaan lukien migreeni.
Seuraavia haittavaikutuksia on raportoitu potilailla, jotka ovat saaneet oraalisia ehkäisyvalmisteita ja joiden uskotaan liittyvän lääkkeisiin (aakkosjärjestyksessä):
Akne Amenorrea Anafylaktiset/anafylaktoidiset reaktiot, mukaan lukien nokkosihottuma, angioedeema ja vaikeat reaktiot, joihin liittyy hengitys- ja verenkiertoelimistön oireita Rintojen muutokset: arkuus, kipu, suureneminen, eritys Budd-Chiarin oireyhtymä Kohdunkaulan eroosio ja eritys, kolestaattisen keltaisuuden muutos Korea, paksusuolentulehduksen paheneminen. , sarveiskalvon kaarevuuden sietokyvyttömyys (jyrkkyys), huimaus Turvotus/nesteen kertymä Erythema multiforme Erythema nodosum Ruoansulatuskanavan oireet (kuten vatsakipu, kouristukset ja turvotus) Hirsutismi Lapsettomuus hoidon lopettamisen jälkeen, tilapäinen imetys, pienennys välittömästi synnytyksen jälkeen Libido, melasman/kloasman muutos, joka saattaa jatkua Kuukautiskierto, mielialan muutokset, mukaan lukien masennus Pahoinvointi Hermostuneisuus Haimatulehdus Porfyria, ihottuman paheneminen (allerginen) Päänahan hiukset, seerumin folaattipitoisuuden väheneminen, systeeminen lupus erythematosus, ajoittamattoman paheneminen verenvuoto vaginiitti, mukaan lukien kandidiaasi suonikohjut, oksentelun paheneminen Paino tai ruokahalu (lisään tai vähenee),
Seuraavia haittavaikutuksia on raportoitu oraalisten ehkäisyvalmisteiden käyttäjillä:
Kaihi Kystiitin kaltainen oireyhtymä Dysmenorrea Hemolyyttinen ureeminen oireyhtymä Hemorraginen eruptio Optinen neuriitti, joka voi johtaa osittaiseen tai täydelliseen näön menetykseen Premenstruaalinen oireyhtymä Munuaisten toimintahäiriö
HUUMEIDEN VUOROVAIKUTUKSET
Muutokset ehkäisyn tehokkuudessa, jotka liittyvät muiden tuotteiden yhteiskäyttöön
Ehkäisyteho saattaa heikentyä, kun hormonaalisia ehkäisyvalmisteita käytetään samanaikaisesti antibioottien, kouristuslääkkeiden ja muiden ehkäisysteroidien metaboliaa kiihdyttävien lääkkeiden kanssa. Tämä voi johtaa tahattomaan raskauteen tai läpilyöntiverenvuotoon. Esimerkkejä ovat rifampiini, rifabutiini, barbituraatit, primidoni, fenyylibutatsoni, fenytoiini, deksametasoni, karbamatsepiini, felbamaatti, okskarbatsepiini, topiramaatti, griseofulviini ja modafiniili. Tällaisissa tapauksissa on harkittava ei-hormonaalista ehkäisymenetelmää.
Kirjallisuudessa on raportoitu useita tapauksia, joissa ehkäisyn epäonnistuminen ja läpilyöntiverenvuoto on aiheuttanut samanaikaisen antibioottien, kuten ampisilliinin ja muiden penisilliinien ja tetrasykliinien käytön. Kliinisissä farmakologisissa tutkimuksissa, joissa on selvitetty yhdistelmäehkäisytablettien ja näiden antibioottien välisiä yhteisvaikutuksia, on kuitenkin raportoitu epäjohdonmukaisia tuloksia.
Useita anti-HIV-proteaasi-inhibiittoreita on tutkittu yhdessä oraalisten hormonaalisten yhdistelmäehkäisyvalmisteiden kanssa; merkittäviä muutoksia (nousua ja laskua) plasman estrogeenin ja progestiinin pitoisuuksissa on havaittu joissakin tapauksissa. Suun kautta otettavien ehkäisyvalmisteiden turvallisuus ja teho voivat heikentyä, jos samanaikaisesti annetaan HIV-proteaasin estäjiä. Terveydenhuollon tarjoajien tulee katsoa yksittäisten HIV-proteaasi-inhibiittoreiden etiketistä lisätietoja lääkkeiden yhteisvaikutuksista.
Mäkikuismaa (Hypericum perforatum) sisältävät kasviperäiset tuotteet voivat indusoida maksaentsyymejä (sytokromi P 450) ja p-glykoproteiinin kuljettajaa ja heikentää ehkäisysteroidien tehoa. Tämä voi myös aiheuttaa läpimurtoverenvuotoa.
Samanaikaisesti käytettäviin lääkkeisiin liittyvä plasmapitoisuuden nousu
Atorvastatiinin ja tiettyjen etinyyliestradiolia sisältävien oraalisten ehkäisyvalmisteiden samanaikainen käyttö lisää etinyyliestradiolin AUC-arvoja noin 20 %. Askorbiinihappo ja asetaminofeeni lisäävät etinyyliestradiolin biologista hyötyosuutta, koska nämä lääkkeet toimivat kilpailevina estäjinä etinyyliestradiolin sulfaatiolle maha-suolikanavan seinämässä, mikä on tunnettu etinyyliestradiolin eliminaatioreitti. CYP 3A4:n estäjät, kuten indinaviiri, itrakonatsoli, ketokonatsoli, flukonatsoli ja troleandomysiini, voivat lisätä plasman hormonitasoja. Troleandomysiini voi myös lisätä maksansisäisen kolestaasin riskiä, kun sitä käytetään samanaikaisesti yhdistelmäehkäisyvalmisteiden kanssa.
Muutokset samanaikaisesti annettujen lääkkeiden plasmapitoisuuksissa
Joitakin synteettisiä estrogeeneja (esim. etinyyliestradiolia) sisältävät hormonaaliset yhdistelmäehkäisyvalmisteet voivat estää muiden yhdisteiden metaboliaa. Plasman siklosporiinin, prednisolonin ja muiden kortikosteroidien ja teofylliinin pitoisuuksia on raportoitu kohonneita, jos samanaikaisesti on käytetty oraalisia ehkäisyvalmisteita. Plasman asetaminofeenin pitoisuuksien pienenemistä ja tematsepaamin, salisyylihapon, morfiinin ja klofibriinihapon puhdistuman lisääntymistä on havaittu konjugaation (erityisesti glukuronidaation) induktion vuoksi, kun näitä lääkkeitä on annettu suun kautta otettavien ehkäisyvalmisteiden kanssa.
Samanaikaisten lääkkeiden reseptitiedot tulee tarkistaa mahdollisten yhteisvaikutusten tunnistamiseksi.
Vuorovaikutukset laboratoriotestien kanssa
Suun kautta otettavat ehkäisyvalmisteet voivat vaikuttaa tiettyihin endokriinisiin ja maksan toimintakokeisiin ja veren komponentteihin:
VAROITUKSET
Tupakointi lisää suun kautta otettavien ehkäisyvalmisteiden käytön aiheuttamien vakavien kardiovaskulaaristen sivuvaikutusten riskiä. Tämä riski kasvaa iän ja tupakoinnin laajuuden myötä (epidemiologisissa tutkimuksissa vähintään 15 savuketta päivässä liittyi merkittävästi lisääntyneeseen riskiin) ja se on melko merkittävä yli 35-vuotiailla naisilla. Naisia, jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, tulee ehdottomasti neuvoa olemaan tupakoimatta.
Suun kautta otettavien ehkäisyvalmisteiden käyttöön liittyy lisääntynyt riski saada useita vakavia sairauksia, mukaan lukien laskimo- ja valtimotromboottiset ja tromboemboliset tapahtumat (kuten sydäninfarkti, tromboembolia ja aivohalvaus), maksaneoplasia, sappirakon sairaus ja verenpainetauti, vaikka vakavan sairastuvuuden tai kuolleisuus on hyvin pieni terveillä naisilla ilman taustalla olevia riskitekijöitä. Sairastuvuuden ja kuolleisuuden riski kasvaa merkittävästi muiden taustalla olevien riskitekijöiden, kuten tiettyjen perinnöllisten tai hankittujen trombofilioiden, kohonneen verenpaineen, hyperlipidemioiden, liikalihavuuden, diabeteksen ja leikkausten tai traumojen, joihin liittyy lisääntynyt tromboosiriski (ks. VASTA-AIHEET ).
Oraalisia ehkäisyvalmisteita määräävien lääkärien tulee tuntea seuraavat näihin riskeihin liittyvät tiedot.
Tämän pakkausselosteen sisältämät tiedot perustuvat pääasiassa tutkimuksiin, jotka on suoritettu potilailla, jotka käyttivät suun kautta otettavia ehkäisyvalmisteita, joissa oli suurempia annoksia estrogeenia ja progestiinia kuin nykyisin yleisesti käytettyjä. Suun kautta otettavien ehkäisyvalmisteiden pitkäaikaisen käytön sekä estrogeeni- että progestiiniannoksilla pienempiä vaikutuksia ei ole vielä selvitetty.
Tämän merkinnän aikana raportoituja epidemiologisia tutkimuksia on kahdenlaisia: retrospektiiviset tai tapauskontrollitutkimukset ja prospektiiviset tai kohorttitutkimukset. Tapauskontrollitutkimukset tarjoavat mittarin suhteellisesta sairauden riskistä, nimittäin sairauden esiintyvyyden suhteesta oraalisten ehkäisyvalmisteiden käyttäjien keskuudessa verrattuna ei-käyttäjiin. Suhteellinen riski ei anna tietoa sairauden todellisesta kliinisestä esiintymisestä. Kohorttitutkimukset tarjoavat mittarin johtuvan riskin, joka on ero sairauksien ilmaantuvuus oraalisen ehkäisyn käyttäjien ja ei-käyttäjiä. Syyksi laskettava riski antaa tietoa taudin todellisesta esiintymisestä väestössä. Lisätietoa lukija saa epidemiologisia menetelmiä käsittelevästä tekstistä.
Tromboemboliset häiriöt ja muut verisuoniongelmat
Sydäninfarkti
Suun kautta otettavien ehkäisyvalmisteiden käytön on katsottu lisäävän sydäninfarktin riskiä. Tämä riski on ensisijaisesti tupakoitsijoilla tai naisilla, joilla on muita sepelvaltimotaudin taustalla olevia riskitekijöitä, kuten verenpainetauti, hyperkolesterolemia, sairaalloinen liikalihavuus ja diabetes. Suhteellisen sydänkohtauksen riskin nykyisten ehkäisyvalmisteiden käyttäjien on arvioitu olevan kahdesta kuuteen. Riski on erittäin pieni alle 30-vuotiailla.
Tupakoinnin yhdessä suun kautta otettavien ehkäisyvalmisteiden kanssa on osoitettu lisäävän merkittävästi sydäninfarktin ilmaantuvuutta yli 30-vuotiailla naisilla, ja tupakoinnin osuus on suurin osa tapauksista. Verenkiertosairauksiin liittyvän kuolleisuuden on osoitettu nousevan merkittävästi yli 35-vuotiailla tupakoitsijoilla ja yli 40-vuotiailla tupakoimattomilla (KUVA II) naisten keskuudessa, jotka käyttävät ehkäisyvalmisteita.
VERIVERENKIERTOTAUTEIDEN KUOLLISUUDEN 100 000 NAINEN VUOTTA KOHTA IKÄN, TUPAKOINTITILANNEN JA SUUSUN EHKÄISYN KÄYTÖN mukaan 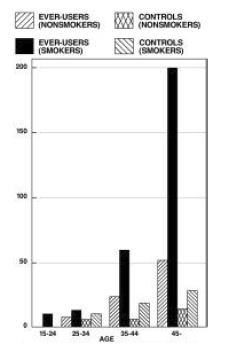 KUVIO II: (Muokattu julkaisusta PM Layde ja V. Beral, Lancet, 1:541–546, 1981.)
KUVIO II: (Muokattu julkaisusta PM Layde ja V. Beral, Lancet, 1:541–546, 1981.)
Suun kautta otettavat ehkäisyvalmisteet voivat lisätä tunnettujen riskitekijöiden, kuten verenpainetaudin, diabeteksen, hyperlipidemioiden, iän ja liikalihavuuden, vaikutuksia. Erityisesti joidenkin progestogeenien tiedetään alentavan HDL-kolesterolia ja aiheuttavan glukoosi-intoleranssia, kun taas estrogeenit voivat aiheuttaa hyperinsulinismin tilan. Suun kautta otettavien ehkäisyvalmisteiden on osoitettu nostavan verenpainetta käyttäjien keskuudessa. Samanlaisia vaikutuksia riskitekijöihin on liitetty kohonneeseen sydänsairauksien riskiin. Suun kautta otettavia ehkäisyvalmisteita tulee käyttää varoen naisilla, joilla on sydän- ja verisuonitautien riskitekijöitä.
Laskimotromboosi ja tromboembolia
Suun kautta otettavien ehkäisyvalmisteiden käyttöön liittyvä lisääntynyt laskimotromboembolisten ja tromboottisten sairauksien riski on vakiintunut. Tapauskontrollitutkimukset ovat osoittaneet, että käyttäjien suhteellinen riski verrattuna ei-käyttäjiin on 3 ensimmäisen pinnallisen laskimotromboosin episodin osalta, 4-11 syvän laskimotukoksen tai keuhkoembolian osalta ja 1,5-6 naisilla, joilla on altistava laskimotukos. tromboembolinen sairaus. Kohorttitutkimukset ovat osoittaneet suhteellisen riskin olevan hieman pienempi, noin 3 uusissa tapauksissa ja noin 4,5 uusissa sairaalahoitoa vaativissa tapauksissa. Syvän laskimotromboosin ja keuhkoembolian likimääräinen ilmaantuvuus pieniannoksisten (
Leikkauksen jälkeisten tromboembolisten komplikaatioiden suhteellisen riskin on raportoitu lisääntyneen kahdesta neljään kertaan oraalisten ehkäisyvalmisteiden käytön yhteydessä. Suhteellinen laskimotromboosin riski naisilla, joilla on altistavia sairauksia, on kaksi kertaa suurempi kuin naisilla, joilla ei ole tällaisia sairauksia. Jos mahdollista, ehkäisyvalmisteiden käyttö tulee lopettaa vähintään neljä viikkoa ennen ja kahdeksi viikoksi sen jälkeen elektiivistä leikkausta, johon liittyy tromboembolian riskin lisääntyminen, sekä pitkittyneen immobilisaation aikana ja sen jälkeen. Koska välittömästi synnytyksen jälkeiseen aikaan liittyy myös kohonnut tromboembolian riski, ehkäisytablettien käyttö tulee aloittaa aikaisintaan neljä viikkoa synnytyksen jälkeen naisilla, jotka eivät halua imettää, tai raskauden puolivälin jälkeen.
Aivoverenkierron sairaudet
Suun kautta otettavien ehkäisyvalmisteiden on osoitettu lisäävän aivoverisuonitapahtumien (tromboottisten ja verenvuotoa aiheuttavien aivohalvausten) sekä suhteellista että niiden aiheuttamaa riskiä, vaikka yleensä riski on suurin iäkkäillä (> 35-vuotiailla) verenpainepotilailla, jotka myös tupakoivat. Verenpainetaudin havaittiin olevan riskitekijä sekä käyttäjille että ei-käyttäjille molemmissa aivohalvaustyypeissä, kun taas tupakointi lisäsi verenvuotoa aiheuttavien aivohalvausten riskiä.
Laajassa tutkimuksessa tromboottisten aivohalvausten suhteellisen riskin on osoitettu vaihtelevan 3:sta normotensiivisillä käyttäjillä 14:ään potilailla, joilla on vaikea verenpaine. Hemorragisen aivohalvauksen suhteellisen riskin on raportoitu olevan 1,2 tupakoimattomilla, jotka käyttivät suun kautta otettavia ehkäisyvalmisteita, 2,6 tupakoitsijoilla, jotka eivät käyttäneet suun kautta otettavia ehkäisyvalmisteita, 7,6 tupakoitsijoilla, jotka käyttivät ehkäisyvalmisteita, 1,8 normaalia verenpainetta käyttävillä ja 25,7 käyttäjillä, joilla on vaikea verenpaine. Syynä oleva riski on myös suurempi iäkkäillä naisilla. Suun kautta otettavat ehkäisyvalmisteet lisäävät myös aivohalvauksen riskiä naisilla, joilla on muita taustalla olevia riskitekijöitä, kuten tiettyjä perinnöllisiä tai hankittuja trombofilioita. Naiset, joilla on migreeni (erityisesti migreeni/päänsärky, johon liittyy fokaalisia neurologisia oireita, ks VASTA-AIHEET ), jotka käyttävät yhdistelmäehkäisytabletteja, saattaa olla suurentunut aivohalvauksen riskissä.
Suun kautta otettavien ehkäisyvalmisteiden aiheuttama annoksesta riippuva verisuonisairauden riski
Positiivinen yhteys on havaittu oraalisissa ehkäisyvalmisteissa olevan estrogeenin ja progestiinin määrän ja verisuonisairauksien riskin välillä. Seerumin korkeatiheyksisten lipoproteiinien (HDL) vähenemistä on raportoitu monien progestaatiolääkkeiden yhteydessä. Seerumin korkeatiheyksisten lipoproteiinien väheneminen on yhdistetty iskeemisen sydänsairauden ilmaantuvuuden lisääntymiseen. Koska estrogeenit lisäävät HDL-kolesterolia, suun kautta otettavan ehkäisyvalmisteen nettovaikutus riippuu estrogeeni- ja progestiiniannosten välisestä tasapainosta ja ehkäisyssä käytetyn progestiinin luonteesta ja absoluuttisesta määrästä. Molempien hormonien määrä tulee ottaa huomioon suun kautta otettavaa ehkäisyä valittaessa.
Estrogeeni- ja progestiinialtistuksen minimointi on terapeuttisten periaatteiden mukaista. Jollekin tietylle estrogeeni/progestogeeni-yhdistelmälle määrätyn annostusohjelman tulee olla sellainen, joka sisältää vähiten estrogeenia ja progestiinia, mikä on yhteensopiva alhaisen epäonnistumisasteen ja yksittäisen potilaan tarpeiden kanssa. Oraalisten ehkäisyvalmisteiden uusien akseptorien käyttö tulee aloittaa valmisteilla, jotka sisältävät pienimmän estrogeenipitoisuuden, joka katsotaan sopivaksi yksittäiselle potilaalle.
Verisuonisairauksien riskin säilyminen
On olemassa kaksi tutkimusta, jotka ovat osoittaneet verisuonisairauksien riskin jatkuvan oraalisten ehkäisyvalmisteiden käyttäjillä. Yhdysvalloissa tehdyssä tutkimuksessa sydäninfarktin riski oraalisten ehkäisyvalmisteiden lopettamisen jälkeen säilyy vähintään 9 vuotta 40–49-vuotiailla naisilla, jotka olivat käyttäneet suun kautta otettavia ehkäisyvalmisteita vähintään viisi vuotta, mutta tätä lisääntynyttä riskiä ei ole osoitettu muissa ikäryhmät.
Eräässä toisessa Isossa-Britanniassa tehdyssä tutkimuksessa riski sairastua aivoverisuonisairauksiin säilyi vähintään 6 vuotta ehkäisytablettien lopettamisen jälkeen, vaikka ylimääräinen riski oli hyvin pieni. Molemmat tutkimukset suoritettiin kuitenkin oraalisilla ehkäisyvalmisteilla, jotka sisälsivät 50 mikrogrammaa tai enemmän estrogeenia.
Arviot ehkäisyn aiheuttamasta kuolleisuudesta
Eräässä tutkimuksessa kerättiin tietoja useista lähteistä, joissa on arvioitu eri ikäryhmien eri ehkäisymenetelmiin liittyvää kuolleisuutta (TAULUKKO III). Nämä arviot sisältävät ehkäisymenetelmiin liittyvän kuolemanriskin ja raskaudesta johtuvan riskin, jos menetelmä epäonnistuu. Jokaisella ehkäisymenetelmällä on omat etunsa ja riskinsä. Tutkimuksessa todettiin, että lukuun ottamatta 35-vuotiaita ja sitä vanhempia tupakoivia ja vähintään 40-vuotiaita, jotka eivät tupakoi, kaikkiin ehkäisymenetelmiin liittyvä kuolleisuus on pienempi kuin synnytykseen liittyvä kuolleisuus. Havainnot mahdollisesta kuolleisuusriskin lisääntymisestä iän myötä oraalisten ehkäisyvalmisteiden käyttäjillä perustuu tutkimuksessa kerättyihin tietoihin.
1970-luvulla – mutta raportoitu vasta 1983. Nykyiseen kliiniseen käytäntöön kuuluu kuitenkin pienempien estrogeeniannosvalmisteiden käyttö yhdistettynä suun kautta otettavien ehkäisyvälineiden käytön huolelliseen rajoittamiseen naisiin, joilla ei ole tässä merkinnässä lueteltuja erilaisia riskitekijöitä.
Näiden käytännön muutosten ja myös joidenkin rajallisten uusien tietojen vuoksi, jotka viittaavat siihen, että sydän- ja verisuonitautien riski suun kautta otettavien ehkäisyvalmisteiden käytön yhteydessä saattaa nyt olla pienempi kuin aiemmin havaittiin, hedelmällisyyden ja äitien terveyden lääkkeiden neuvoa-antavaa komiteaa pyydettiin tarkistamaan aiheesta vuonna 1989. Komitea totesi, että vaikka sydän- ja verisuonitautien riskit voivat lisääntyä suun kautta otettavien ehkäisyvalmisteiden käyttö 40 vuoden iän jälkeen terveillä tupakoimattomilla naisilla (jopa uudemmilla pieniannoksisilla formulaatioilla), iäkkäillä raskauteen liittyy suurempia mahdollisia terveysriskejä naisille ja vaihtoehtoisille kirurgisille ja lääketieteellisille toimenpiteille, jotka voivat olla tarpeen, jos näillä naisilla ei ole saatavilla tehokkaita ja hyväksyttäviä ehkäisykeinoja.
Siksi komitea suositteli, että terveiden yli 40-vuotiaiden tupakoimattomien naisten oraalisten ehkäisyvalmisteiden käytön hyödyt voivat olla mahdollisia riskejä suuremmat. Tietenkin iäkkäiden naisten, kuten kaikkien naisten, jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, tulee ottaa pienin mahdollinen annosmuoto, joka on tehokas.
TAULUKKO III: SYNTYMISEEN TAI MENETELMIIN LIITTYVIEN KUOLEMAN VUOSITTAMINEN 100 000 EI STERIIILIÄ NAISTA kohden HEDELLYTYKSENVALVONTAMENETELMÄN JA IKÄN MUKAAN
Sukuelinten ja rintojen karsinooma
Lukuisat epidemiologiset tutkimukset ovat tutkineet oraalisten ehkäisyvalmisteiden käytön sekä rinta- ja kohdunkaulasyövän ilmaantuvuuden välistä yhteyttä.
Rintasyöpädiagnoosin riski saattaa olla hieman lisääntynyt oraalisten yhdistelmäehkäisyvalmisteiden nykyisillä ja viimeaikaisilla käyttäjillä. Tämä ylimääräinen riski näyttää kuitenkin pienenevän ajan myötä oraalisten yhdistelmäehkäisyvalmisteiden käytön lopettamisen jälkeen, ja lisääntynyt riski katoaa 10 vuoden kuluttua lopettamisesta. Jotkut tutkimukset raportoivat lisääntyneen riskin käytön keston myötä, kun taas toiset tutkimukset eivät, eikä johdonmukaisia suhteita ole löydetty steroidien annoksen tai tyypin kanssa. Jotkut tutkimukset ovat raportoineet riskin pienen lisääntyneen naisilla, jotka käyttävät ensimmäistä kertaa yhdistelmäehkäisytabletteja nuorempana. Useimmat tutkimukset osoittavat samanlaisen riskimallin oraalisten yhdistelmäehkäisyvalmisteiden käytössä riippumatta naisen lisääntymishistoriasta tai hänen perheen rintasyöpähistoriastaan.
Nykyisillä tai aiemmilla OC-käyttäjillä diagnosoidut rintasyövät ovat yleensä kliinisesti vähemmän edenneitä kuin ei-käyttäjillä.
Naisten, joilla on tunnettu tai epäilty rintasyöpä tai joilla on rintasyöpä anamneesissa, ei tule käyttää ehkäisyvalmisteita, koska rintasyöpä on yleensä hormonaalisesti herkkä kasvain.
Jotkut tutkimukset viittaavat siihen, että suun kautta otettavien ehkäisyvalmisteiden käyttö on yhdistetty kohdunkaulan intraepiteliaalisen neoplasian tai invasiivisen kohdunkaulasyövän riskin lisääntymiseen joissakin naisryhmissä. Siitä huolimatta, missä määrin tällaiset havainnot voivat johtua eroista seksuaalisessa käyttäytymisessä ja muista tekijöistä, on edelleen kiistaa.
Huolimatta monista tutkimuksista oraalisten yhdistelmäehkäisyvalmisteiden käytön sekä rinta- ja kohdunkaulasyövän välisestä suhteesta, syy-seuraussuhdetta ei ole osoitettu.
Maksan neoplasia
Hyvänlaatuiset maksaadenoomit liittyvät ehkäisyvalmisteiden käyttöön, vaikka näiden hyvänlaatuisten kasvainten ilmaantuvuus on harvinaista Yhdysvalloissa. Epäsuorat laskelmat ovat arvioineet, että käyttäjästä johtuva riski on 3,3 tapausta/100 000, mikä kasvaa neljän tai useamman vuoden käytön jälkeen. Harvinaisten hyvänlaatuisten maksaadenoomien repeämä voi aiheuttaa kuoleman vatsansisäisen verenvuodon seurauksena.
Isossa-Britanniassa tehdyt tutkimukset ovat osoittaneet lisääntyneen hepatosellulaarisen karsinooman riskin pitkäaikaisilla (> 8-vuotiailla) oraalisten ehkäisyvalmisteiden käyttäjillä. Nämä syövät ovat kuitenkin erittäin harvinaisia Yhdysvalloissa, ja suun kautta otettavien ehkäisyvalmisteiden käyttäjillä maksasyöpien aiheuttama riski (ylimääräinen ilmaantuvuus) on alle yksi miljoonaa käyttäjää kohden.
Silmävauriot
Oraalisten ehkäisyvalmisteiden käyttöön on raportoitu kliinisiä tapauksia verkkokalvon tromboosista, joka voi johtaa osittaiseen tai täydelliseen näön menetykseen. Suun kautta otettavien ehkäisyvalmisteiden käyttö tulee lopettaa, jos näön menetys on selittämätön osittainen tai kokonaan. proptoosin tai diplopian puhkeaminen; papillideema; tai verkkokalvon verisuonivauriot. Asianmukaisiin diagnostisiin ja terapeuttisiin toimenpiteisiin on ryhdyttävä välittömästi.
Suun kautta otettavan ehkäisyn käyttö ennen raskautta tai sen aikana
Laajat epidemiologiset tutkimukset eivät ole osoittaneet lisääntynyttä synnynnäisten epämuodostumien riskiä imeväisillä, jotka ovat syntyneet naisille, jotka ovat käyttäneet ehkäisyä ennen raskautta. Tutkimukset eivät myöskään viittaa teratogeeniseen vaikutukseen, etenkään mitä tulee sydänhäiriöihin ja raajojen supistumishäiriöihin, kun niitä otetaan vahingossa raskauden alkuvaiheessa (ks. VASTA-AIHEET jakso).
Suun kautta otettavien ehkäisyvalmisteiden käyttöä vieroitusverenvuotoa varten ei tule käyttää raskaustestinä. Suun kautta otettavia ehkäisyvalmisteita ei tule käyttää raskauden aikana uhkaavan tai tavanomaisen abortin hoitoon.
On suositeltavaa sulkea pois raskaus, jos potilaalla on jäänyt kaksi peräkkäistä kuukautisia. Jos potilas ei ole noudattanut määrättyä aikataulua, raskauden mahdollisuus tulee ottaa huomioon ensimmäisten kuukautisten väliin jäämisen yhteydessä. Suun kautta otettavien ehkäisyvalmisteiden käyttö tulee lopettaa, jos raskaus varmistuu.
Sappirakon sairaus
Suun kautta otettavat yhdistelmäehkäisyvalmisteet voivat pahentaa olemassa olevaa sappirakon sairautta ja nopeuttaa tämän taudin kehittymistä aiemmin oireettomilla naisilla. Aiemmissa tutkimuksissa on raportoitu lisääntyneen elinikäisen sappirakon leikkauksen suhteellisen riskin oraalisten ehkäisyvalmisteiden ja estrogeenien käyttäjillä. Uusimmat tutkimukset ovat kuitenkin osoittaneet, että suhteellinen riski sairastua sappirakon sairauksiin suun kautta otettavien ehkäisyvalmisteiden käyttäjien keskuudessa voi olla minimaalinen. Viimeaikaiset havainnot minimaalisesta riskistä voivat liittyä oraalisten ehkäisyvalmisteiden käyttöön, jotka sisältävät pienempiä hormonaalisia annoksia estrogeenia ja progestogeeneja.
Hiilihydraattien ja lipidien metaboliset vaikutukset
Suun kautta otettavien ehkäisyvalmisteiden on osoitettu aiheuttavan glukoosi-intoleranssia merkittävällä osalla käyttäjistä. Yli 75 mikrogrammaa estrogeenia sisältävät suun kautta otettavat ehkäisyvalmisteet aiheuttavat hyperinsulinismia, kun taas pienemmät estrogeeniannokset vähentävät glukoosi-intoleranssia. Progestogeenit lisäävät insuliinin eritystä ja luovat insuliiniresistenssiä, tämä vaikutus vaihtelee eri progestatiivisten aineiden mukaan. Ei-diabeettisilla naisilla suun kautta otetuilla ehkäisyvalmisteilla ei kuitenkaan näytä olevan vaikutusta paastoverensokeriin. Näiden todistettujen vaikutusten vuoksi prediabeettisia ja diabeettisia naisia tulee tarkkailla huolellisesti oraalisten ehkäisyvalmisteiden käytön aikana.
Pienellä osalla naisista on jatkuva hypertriglyseridemia pillereiden käytön aikana. Kuten aiemmin mainittiin (katso VAROITUKSET ja VAROTOIMENPITEET .), muutoksia seerumin triglyseridi- ja lipoproteiinitasoissa on raportoitu oraalisten ehkäisyvalmisteiden käyttäjillä.
Kohonnut verenpaine
Verenpaineen nousua on raportoitu naisilla, jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, ja tämä nousu on todennäköisempää iäkkäillä ehkäisyvalmisteiden käyttäjillä ja käytön jatkuessa. Royal College of General Practitioners -yliopiston tiedot ja myöhemmät satunnaistetut tutkimukset ovat osoittaneet, että verenpainetaudin ilmaantuvuus lisääntyy progestogeenien lisääntyessä.
Naisia, joilla on ollut verenpainetauti tai verenpaineeseen liittyviä sairauksia tai munuaissairaus, tulee rohkaista käyttämään muuta ehkäisymenetelmää. Jos verenpainetautia sairastavat naiset päättävät käyttää suun kautta otettavia ehkäisyvalmisteita, heitä tulee seurata tarkasti ja jos verenpaine kohoaa merkittävästi, ehkäisytablettien käyttö on lopetettava (ks. VASTA-AIHEET jakso). Useimmilla naisilla kohonnut verenpaine palautuu normaaliksi suun kautta otettavien ehkäisyvalmisteiden lopettamisen jälkeen, eikä verenpainetaudin esiintymisessä ole eroa aina ja ei koskaan käyttäneiden kesken.
Päänsärky
Migreenin puhkeaminen tai paheneminen tai päänsäryn kehittyminen uudella tavalla, joka on toistuva, jatkuva tai vaikea, vaatii ehkäisyvalmisteiden käytön lopettamista ja syyn selvittämistä. (Katso VAROITUKSET ja VASTA-AIHEET .)
Verenvuotohäiriöt
Oraalista ehkäisyvalmistetta käyttävillä potilailla esiintyy joskus läpimurto- ja tiputteluvuotoa, erityisesti kolmen ensimmäisen käyttökuukauden aikana. Progestogeenin tyyppi ja annos voivat olla tärkeitä. Jos verenvuoto jatkuu tai uusiutuu, on harkittava ei-hormonaalisia syitä ja ryhdyttävä riittäviin diagnostisiin toimenpiteisiin pahanlaatuisuuden tai raskauden poissulkemiseksi läpilyöntiverenvuodon yhteydessä, kuten minkä tahansa epänormaalin emättimen verenvuodon tapauksessa. Jos patologia on suljettu pois, aika tai muutos toiseen formulaatioon voi ratkaista ongelman. Amenorrean tapauksessa raskaus on suljettava pois.
Jotkut naiset voivat kohdata pillereiden jälkeistä amenorreaa tai oligomenorreaa (mahdollisesti anovulaatiolla), varsinkin kun tällainen tila on ollut olemassa.
Kohdunulkoinen raskaus
Kohdunulkoinen ja kohdunsisäinen raskaus voi ilmetä, jos ehkäisy epäonnistuu.
VAROTOIMENPITEET
Kenraali
Potilaita tulee neuvoa, että suun kautta otettavat ehkäisyvalmisteet eivät suojaa HIV:n (AIDS) ja muiden sukupuolitautien, kuten klamydian, sukupuolielinten herpesen, sukupuolielinten syylien, tippurien, hepatiitti B:n ja kupan, tarttumiselta.
Fyysinen tarkastus ja seuranta
Säännöllinen henkilökohtainen ja perheen sairaushistoria ja täydellinen fyysinen tarkastus ovat asianmukaisia kaikille naisille, myös naisille, jotka käyttävät ehkäisyvalmisteita. Fyysistä tarkastusta voidaan kuitenkin lykätä suun kautta otettavien ehkäisyvalmisteiden käytön aloittamisen jälkeen, jos nainen sitä pyytää ja kliinikko katsoo sopivaksi. Fyysisessä tutkimuksessa tulee erityisesti huomioida verenpaine, rinnat, vatsa ja lantion elimet, mukaan lukien kohdunkaulan sytologia, ja asiaankuuluvat laboratoriotutkimukset. Jos emättimestä ilmenee diagnosoimatonta, jatkuvaa tai toistuvaa epänormaalia verenvuotoa, on suoritettava asianmukaiset diagnostiset toimenpiteet pahanlaatuisuuden sulkemiseksi pois. Naisia, joilla on vahva suvussa rintasyöpä tai joilla on rintakyhmyjä, tulee seurata erityisen huolellisesti.
Lipidihäiriöt
Naisia, joita hoidetaan hyperlipidemioiden vuoksi, tulee seurata tarkasti, jos he päättävät käyttää suun kautta otettavia ehkäisyvalmisteita. Jotkut progestogeenit voivat nostaa LDL-tasoja ja vaikeuttaa hyperlipidemioiden hallintaa. (Katso VAROITUKSET )
Pienellä osalla naisia esiintyy haitallisia lipidimuutoksia oraalisten ehkäisyvalmisteiden käytön aikana. Ei-hormonaalista ehkäisyä tulee harkita naisilla, joilla on hallitsematon dyslipidemia. Pysyvää hypertriglyseridemiaa voi esiintyä pienellä yhdistelmäehkäisytablettien käyttäjillä. Plasman triglyseridien nousu voi johtaa haimatulehdukseen ja muihin komplikaatioihin.
Maksan toiminta
Jos jollakin tällaisia lääkkeitä saaneella naisella kehittyy keltaisuutta, lääkitys on lopetettava. Steroidihormonit saattavat metaboloitua heikosti potilailla, joilla on maksan vajaatoiminta.
Nesteenpidätys
Suun kautta otettavat ehkäisyvalmisteet voivat aiheuttaa jonkin verran nesteretentiota. Niitä tulee määrätä varoen ja vain huolellisella seurannalla potilaille, joilla on sairauksia, joita nesteretentio saattaa pahentaa.
Emotionaaliset häiriöt
Potilaiden, jotka masentuvat merkittävästi oraalisten ehkäisyvalmisteiden käytön aikana, tulee lopettaa lääkitys ja käyttää vaihtoehtoista ehkäisymenetelmää selvittääkseen, liittyykö oire lääkkeeseen. Naisia, joilla on aiemmin ollut masennusta, tulee tarkkailla huolellisesti ja lääkkeen käyttö lopettaa, jos masennus uusiutuu vakavasti.
Piilolinssit
Silmälääkärin tulee arvioida piilolinssien käyttäjien, joille kehittyy näkömuutoksia tai muutoksia linssien sietokyvyssä.
Ruoansulatuskanava
Ripuli ja/tai oksentelu voivat heikentää hormonin imeytymistä, mikä johtaa seerumin pitoisuuksien laskuun.
Karsinogeneesi
Katso VAROITUKSET osio.
Raskaus
Raskausluokka X. Katso VASTA-AIHEET ja VAROITUKSET osiot.
Imettävät äidit
Pieniä määriä suun kautta otettavia ehkäisyvalmisteita ja/tai aineenvaihduntatuotteita on havaittu imettävien äitien maidosta, ja muutamia lapseen kohdistuvia haittavaikutuksia on raportoitu, mukaan lukien keltaisuus ja rintojen suureneminen. Lisäksi synnytyksen jälkeen annetut yhdistelmäehkäisyvalmisteet voivat häiritä imetystä heikentämällä rintamaidon määrää ja laatua. Jos mahdollista, imettävää äitiä tulee neuvoa olemaan käyttämättä yhdistelmäehkäisyvalmisteita, vaan käyttämään muita ehkäisymuotoja, kunnes hän on täysin vieroittanut lapsensa.
Käyttö lapsille
ALESSE (levonorgestreeli ja etinyyliestradioli) -tablettien turvallisuus ja teho on osoitettu lisääntymisiässä olevilla naisilla. Turvallisuuden ja tehon odotetaan olevan sama alle 16-vuotiailla murrosikäisillä nuorilla ja 16-vuotiailla ja sitä vanhemmilla käyttäjillä. ALESSE:n (levonorgestreeli ja etinyyliestradioli) käyttö ennen kuukautisia ei ole aiheellista.
Geriatrinen käyttö
ALESSE:tä (levonorgestreeli ja etinyyliestradioli) ei ole tutkittu yli 65-vuotiailla naisilla, eikä sitä ole tarkoitettu tälle populaatiolle.
Tietoa potilaalle
Katso Potilaan merkintä .
YLIANNOSTUS
Oraalisten ehkäisyvalmisteiden yliannostuksen oireita aikuisilla ja lapsilla voivat olla pahoinvointi, oksentelu ja uneliaisuus/väsymys; vieroitusvuotoa voi esiintyä naisilla. Spesifistä vastalääkettä ei ole ja yliannostuksen jatkohoitoa ohjataan tarvittaessa oireisiin.
EHKÄISYYDYÖT
Epidemiologiset tutkimukset, joissa suurelta osin käytettiin suun kautta otettavia ehkäisyvalmisteita, jotka sisälsivät annoksia yli 0,035 mg etinyyliestradiolia tai 0,05 mg mestranolia, tukevat seuraavia oraalisten ehkäisyvalmisteiden käyttöön liittyviä terveyshyötyjä.
Vaikutukset kuukautisiin:
Lisääntynyt kuukautiskierron säännöllisyys
Vähentynyt verenhukka ja vähentynyt raudanpuuteanemian esiintyvyys
Vähentynyt dysmenorrea
Ovulaation estoon liittyvät vaikutukset:
Vähentynyt toiminnallisten munasarjakystien esiintyvyys
Kohdunulkoisten raskauksien esiintyvyys on vähentynyt
Pitkäaikaisen käytön vaikutukset:
Vähentynyt fibroadenoomien ja rintojen fibrokystisen sairauden esiintyvyys
Akuutin lantion alueen tulehdussairauden ilmaantuvuus on vähentynyt
Vähentynyt kohdun limakalvon syövän ilmaantuvuus
Vähentynyt munasarjasyövän ilmaantuvuus
VASTA-AIHEET
Suun kautta otettavia yhdistelmäehkäisyvalmisteita ei pidä käyttää naisilla, joilla on jokin seuraavista sairauksista:
Tromboflebiitti tai tromboemboliset häiriöt
Aiempi syvä laskimotromboflebiitti tai tromboembolinen häiriö
Aivo- tai sepelvaltimotauti (nykyinen tai aiempi historia) Trombogeeniset läppäsairaudet
Trombogeeniset rytmihäiriöt
Suuri leikkaus, johon liittyy pitkittynyt immobilisaatio Diabetes, johon liittyy verisuonihäiriö Päänsärky, johon liittyy fokaalisia neurologisia oireita Hallitsematon verenpainetauti
Tunnettu tai epäilty rintasyöpä tai henkilökohtainen rintasyöpähistoria
Endometriumin karsinooma tai muu tunnettu tai epäilty estrogeeniriippuvainen neoplasia
Diagnosoimaton epänormaali sukuelinten verenvuoto
Kolestaattinen keltaisuus raskauden aikana tai keltaisuus aiemman pillereiden käytön yhteydessä
Maksan adenoomat tai karsinoomat tai aktiivinen maksasairaus, kunhan maksan toiminta ei ole palautunut normaaliksi
Tunnettu tai epäilty raskaus
Yliherkkyys jollekin Alessen aineosalle (levonorgestreeli ja etinyyliestradioli)
KLIININEN FARMAKOLOGIA
Toimintatapa
Suun kautta otettavat yhdistelmäehkäisyvalmisteet estävät gonadotropiinien määrää. Vaikka tämän vaikutuksen ensisijainen mekanismi on ovulaation estäminen, muita muutoksia ovat muutokset kohdunkaulan limassa (jotka vaikeuttavat siittiöiden pääsyä kohtuun) ja endometriumissa (jotka vähentävät implantaation todennäköisyyttä).
Farmakokinetiikka
Imeytyminen
ALESSE:n (levonorgestreeli ja etinyyliestradioli) absoluuttisesta biologisesta hyötyosuudesta ihmisillä ei ole tehty erityisiä tutkimuksia. Kirjallisuus kuitenkin osoittaa, että levonorgestreeli imeytyy nopeasti ja täydellisesti oraalisen annon jälkeen (biologinen hyötyosuus noin 100 %) eikä se ole alttiina ensikierron metabolialle. Etinyyliestradioli imeytyy nopeasti ja lähes täydellisesti maha-suolikanavasta, mutta ensikierron metabolian vuoksi suolen limakalvolla ja maksassa etinyyliestradiolin hyötyosuus on 38–48 %.
Kun kerta-annos ALESSE:tä (levonorgestreeli ja etinyyliestradioli) on annettu 22 naiselle paastoolosuhteissa, levonorgestreelin enimmäispitoisuudet seerumissa ovat 2,8 ± 0,9 ng/ml (keskiarvo ± SD) 1,6 ± 0,9 tunnin kohdalla. Vakaassa tilassa, joka saavutetaan päivästä 19 eteenpäin, levonorgestreelin maksimipitoisuudet 6,0 ± 2,7 ng/ml saavutetaan 1,5 ± 0,5 tunnin kuluttua päivittäisestä annoksesta. Levonorgestreelin vähimmäistaso seerumissa vakaassa tilassa on 1,9 ± 1,0 ng/ml. Havaitut levonorgestreelipitoisuudet nousivat päivästä 1 (kerta-annos) päiviin 6 ja 21 (useita annoksia) 34 % ja 96 % (kuva 1). Sitoutumattoman levonorgestreelin pitoisuudet nousivat päivästä 1 päivään 6 ja 21 25 % ja 83 %. Kokonaislevonorgestreelin kinetiikka on epälineaarinen johtuen levonorgestreelin lisääntyneestä sitoutumisesta sukupuolihormonia sitovaan globuliiniin (SHBG), mikä johtuu etinyyliestradiolin päivittäisen antamisen aiheuttamista kohonneista SHBG-tasoista.
Kerta-annoksen jälkeen etinyyliestradiolin huippupitoisuus seerumissa, 62 ± 21 pg/ml, saavutetaan 1,5 ± 0,5 tunnin kuluttua. Vakaassa tilassa, joka saavutettiin vähintään päivästä 6 eteenpäin, etinyyliestradiolin enimmäispitoisuudet olivat 77 ± 30 pg/ml, ja ne saavutettiin 1,3 ± 0,7 tunnin kuluttua päivittäisestä annoksesta. Etinyyliestradiolin vähimmäistaso seerumissa vakaassa tilassa on 10,5 ± 5,1 pg/ml. Etinyyliestradiolipitoisuudet eivät nousseet päivistä 1 - 6, mutta nousivat 19 % päivistä 1 - 21 (kuvio I).
KUVIO I: Keskimääräiset (SE) levonorgestreelin ja etinyyliestradiolin seerumipitoisuudet 22 koehenkilöllä, jotka saivat ALESSE:tä (levonorgestreeli ja etinyyliestradioli) (100 μg levonorgestreeliä ja 20 μg etinyyliestradiolia) 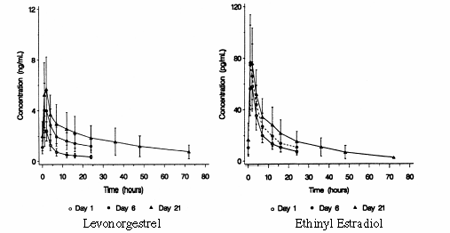
Taulukko I tarjoaa yhteenvedon levonorgestreelin ja etinyyliestradiolin farmakokineettisistä parametreista.
TAULUKKO I: ALESSEN (levonorgestreeli ja etinyyliestradioli) KESKIMÄÄRÄISET (SD) FARMAKOKINEETTISET PARAMETRIT 21 PÄIVÄN ANNOSTUSJAKSOLLA
Jakelu
Seerumin levonorgestreeli sitoutuu ensisijaisesti SHBG:hen. Etinyyliestradiolista noin 97 % sitoutuu plasman albumiiniin. Etinyyliestradioli ei sitoudu SHBG:hen, mutta indusoi SHBG:n synteesiä.
Aineenvaihdunta
Levonorgestreeli: Tärkein metabolinen reitti tapahtuu Δ4-3-oksoryhmän pelkistymisessä ja hydroksylaatiossa asemissa 2α, 1β ja 16β, mitä seuraa konjugaatio. Suurin osa veressä kiertävistä metaboliiteista on 3α,5β-tetrahydrolevonorgestreelin sulfaatteja, kun taas erittyminen tapahtuu pääasiassa glukuronidien muodossa. Osa alkuperäisestä levonorgestreelistä kiertää myös 17β-sulfaattina. Metabolinen puhdistuma voi vaihdella yksilöiden välillä moninkertaisesti, ja tämä voi osittain selittää levonorgestreelipitoisuuksien laajaa vaihtelua käyttäjien välillä.
Etinyyliestradioli: Sytokromi P450 -entsyymit (CYP3A4) maksassa ovat vastuussa 2-hydroksylaatiosta, joka on tärkein oksidatiivinen reaktio. 2-hydroksimetaboliitti muuttuu edelleen metylaatiolla ja glukuronidaatiolla ennen kuin se erittyy virtsaan ja ulosteeseen. Sytokromi P450:n (CYP3A) tasot vaihtelevat suuresti yksilöiden välillä ja voivat selittää etinyyliestradiolin 2-hydroksylaationopeuden vaihtelun. Etinyyliestradioli erittyy virtsaan ja ulosteisiin glukuronidi- ja sulfaattikonjugaatteina ja käy enterohepaattisen verenkierron läpi.
Erittyminen
Levonorgestreelin eliminaation puoliintumisaika vakaassa tilassa on noin 36 ± 13 tuntia. Levonorgestreeli ja sen metaboliitit erittyvät pääasiassa virtsaan (40–68 %) ja noin 16–48 % ulosteeseen. Etinyyliestradiolin eliminaation puoliintumisaika vakaassa tilassa on 18 ± 4,7 tuntia.
Erikoispopulaatiot
Rotu
ALESSE-valmisteella (levonorgestreeli ja etinyyliestradioli) tehdyn farmakokineettisen tutkimuksen perusteella farmakokineettisissä parametreissa ei ole ilmeisiä eroja eri rotuihin kuuluvien naisten välillä.
Maksan vajaatoiminta
Muodollisissa tutkimuksissa ei ole arvioitu maksasairauden vaikutusta ALESSE:n (levonorgestreeli ja etinyyliestradioli) jakautumiseen. Steroidihormonit voivat kuitenkin metaboloitua heikosti potilailla, joilla on maksan vajaatoiminta.
Munuaisten vajaatoiminta
Muodollisissa tutkimuksissa ei ole arvioitu munuaissairauden vaikutusta ALESSE:n (levonorgestreeli ja etinyyliestradioli) jakautumiseen.
Lääkkeiden väliset vuorovaikutukset
Katso VAROTOIMENPITEET -osio - LÄÄKEMUOTOTIEDOT
POTILASTIEDOT
Lyhyt yhteenveto Potilaspakkausseloste
Tämä tuote (kuten kaikki suun kautta otettavat ehkäisyvalmisteet) on tarkoitettu raskauden estämiseen. Suun kautta otettavat ehkäisyvalmisteet eivät suojaa HIV:ltä (AIDS) ja muilta sukupuolitaudeilta, kuten klamydialta, genitaaliherpekseltä, sukupuolielinten syyliltä, tippurilta, hepatiitti B:ltä ja kupalta.
Suun kautta otettavia ehkäisyvalmisteita, jotka tunnetaan myös nimellä "ehkäisytabletit" tai "pillerit", käytetään raskauden ehkäisemiseksi, ja oikein käytettynä niiden epäonnistumisprosentti on noin 1,0 % vuodessa (1 raskaus 100 naista kohden käyttövuotta kohti). käytettäessä pillereitä puuttumatta. Keskimääräinen epäonnistumisprosentti suurella määrällä pillereiden käyttäjiä on noin 5 % vuodessa (5 raskautta 100:aa naista kohden käyttövuotta kohti), kun mukaan luetaan naiset, jotka jäävät ottamatta pillereitä. Useimmille naisille suun kautta otettavat ehkäisyvalmisteet eivät myöskään aiheuta vakavia tai epämiellyttäviä sivuvaikutuksia. Pillereiden ottamisen unohtaminen lisää kuitenkin huomattavasti raskauden todennäköisyyttä.
Suurin osa naisista voi ottaa suun kautta otettavat ehkäisyvalmisteet turvallisesti. Mutta joillakin naisilla on suuri riski saada tiettyjä vakavia sairauksia, jotka voivat olla hengenvaarallisia tai aiheuttaa tilapäisen tai pysyvän vamman tai kuoleman. Suun kautta otettavien ehkäisyvalmisteiden käyttöön liittyvät riskit lisääntyvät merkittävästi, jos:
- savu.
- sinulla on korkea verenpaine, diabetes, korkea kolesteroli tai taipumus muodostaa verihyytymiä.
- sinulla on tai on ollut hyytymishäiriöitä, sydänkohtaus, aivohalvaus, angina pectoris, rintasyöpä tai sukupuolielinten syöpä, keltaisuus, pahanlaatuiset tai hyvänlaatuiset maksakasvaimet tai suuri leikkaus, johon liittyy pitkittynyt immobilisaatio.
- sinulla on päänsärkyä, johon liittyy neurologisia oireita.
Älä ota pilleriä, jos epäilet olevasi raskaana tai jos sinulla on selittämätöntä verenvuotoa emättimestä.
Vaikka sydän- ja verisuonitautien riskit voivat lisääntyä suun kautta otettavien ehkäisyvalmisteiden käytön jälkeen 40 vuoden iän jälkeen terveillä, tupakoimattomilla naisilla, on myös suurempia mahdollisia terveysriskejä, jotka liittyvät raskauteen vanhemmilla naisilla.
Tupakointi lisää vakavien haitallisten vaikutusten riskiä sydämeen ja verisuoniin suun kautta otettavien ehkäisyvalmisteiden käytöstä. Tämä riski kasvaa iän ja tupakoinnin lisääntyessä (vähintään 15 savuketta päivässä on liitetty merkittävästi lisääntyneeseen riskiin) ja se on varsin huomattava yli 35-vuotiailla naisilla. Naiset, jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, eivät saa tupakoida.
Useimmat pillereiden sivuvaikutukset eivät ole vakavia. Yleisimmät tällaiset vaikutukset ovat pahoinvointi, oksentelu, verenvuoto kuukautisten välillä, painonnousu, rintojen arkuus ja piilolinssien käyttövaikeudet. Nämä haittavaikutukset, erityisesti pahoinvointi ja oksentelu, voivat hävitä kolmen ensimmäisen käyttökuukauden aikana.
Pillereiden vakavia sivuvaikutuksia esiintyy hyvin harvoin, varsinkin jos olet hyvässä kunnossa etkä tupakoi. Sinun tulee kuitenkin tietää, että pillereihin on liitetty seuraavat sairaudet tai ne ovat pahentuneet:
Näihin vakaviin sivuvaikutuksiin liittyviä oireita käsitellään yksityiskohtaisessa pakkausselosteessa, joka annetaan sinulle pilleritoimituksen mukana. Ilmoita terveydenhuollon tarjoajallesi, jos havaitset epätavallisia fyysisiä häiriöitä pillereiden ottamisen aikana. Lisäksi lääkkeet, kuten rifampiini, sekä jotkin epilepsialääkkeet ja jotkin antibiootit, mäkikuismaa (Hypericum perforatum) sisältävät rohdosvalmisteet ja HIV/AIDS-lääkkeet voivat heikentää suun kautta otettavien ehkäisyvalmisteiden tehoa.
Useat tutkimukset antavat ristiriitaisia raportteja rintasyövän ja ehkäisyvälineiden välisestä suhteesta.
Suun kautta otettavien ehkäisyvalmisteiden käyttö saattaa hieman lisätä todennäköisyyttäsi saada rintasyöpä, varsinkin jos aloitit hormonaalisen ehkäisyn käytön nuorempana.
Kun lopetat hormonaalisten ehkäisyvalmisteiden käytön, rintasyövän todennäköisyys alkaa laskea ja häviää 10 vuoden kuluttua pillereiden käytön lopettamisesta. Ei tiedetä, johtuuko tämä hieman lisääntynyt rintasyöpädiagnoosin riski pilleristä. Saattaa olla, että pilleriä käyttäviä naisia tutkittiin useammin, jolloin rintasyöpä todettiin todennäköisemmin.
Sinun tulee käydä rintojen tarkastuksessa säännöllisesti terveydenhuollon ammattilaisella ja tarkistaa omat rinnasi kuukausittain. Kerro terveydenhuollon tarjoajallesi, jos sinulla on suvussa rintasyöpää tai jos sinulla on ollut rintojen kyhmyjä tai epänormaali mammografia. Naisten, joilla on tai on ollut rintasyöpä, ei tule käyttää ehkäisyvalmisteita, koska rintasyöpä on yleensä hormoniherkkä kasvain.
Joissakin tutkimuksissa on havaittu lisääntyneen kohdunkaulan syövän ilmaantuvuus naisilla, jotka käyttävät ehkäisyvalmisteita. Tämä havainto voi kuitenkin liittyä muihin tekijöihin kuin suun kautta otettavien ehkäisyvalmisteiden käyttöön.
Pillereiden ottaminen tarjoaa tärkeitä ei-ehkäisyvaikutuksia. Näitä ovat vähemmän kivuliaita kuukautisia, vähemmän kuukautisten verenhukkaa ja anemiaa, vähemmän lantion infektioita ja vähemmän munasarjojen ja kohdun limakalvon syöpiä.
Muista keskustella terveydenhuollon tarjoajasi kanssa mahdollisista lääketieteellisistä tiloistasi. Terveydenhuollon tarjoaja ottaa lääketieteellisen ja sukuhistorian ennen ehkäisytablettien määräämistä ja tutkii sinut. Fyysinen tarkastus voidaan siirtää toiseen ajankohtaan, jos pyydät sitä ja terveydenhuollon tarjoaja katsoo, että sen lykkääminen on aiheellista. Sinut tulee tutkia uudelleen vähintään kerran vuodessa, kun käytät ehkäisyvalmisteita. Yksityiskohtainen potilastietolehtinen antaa sinulle lisätietoja, jotka sinun tulee lukea ja keskustella terveydenhuollon tarjoajan kanssa.
MITEN ALESSE OTETAAN (levonorgestreeli ja etinyyliestradioli)
TÄRKEÄÄ MUISTAA
ENNEN KUIN ALOITAT ALESSEN (levonorgestreeli ja etinyyliestradioli) OTtamisen:
1. MUISTA LUE NÄMÄ OHJEET:
Ennen kuin aloitat ALESSEN (levonorgestreeli ja etinyyliestradioli) käytön.
Ja
Aina kun et ole varma mitä tehdä.
2. OIKEIN TAPA OTTA PILLER ON OTTA YKSI PILLE JOKA PÄIVÄ SAMAAN AIKAAN.
Jos unohdat ottaa pillerit, voit tulla raskaaksi. Tämä sisältää paketin aloittamisen myöhässä. Mitä enemmän pillereitä unohdat, sitä todennäköisemmin tulet raskaaksi. Katso kohta "MITÄ TEHDÄ, JOS SINÄ MITTAAT PILLEERIT" alla.
3. MONEILLA NAISILLA ON TÄPPILLE TAI VÄKEVÄÄ VUOTOA TAI VOITTAA OLLA PAHOILLE vatsaan ENSIMMÄISEN 1-3 PILLERIPAKKAUKSEN AIKANA.
Jos tunnet pahoinvointia vatsassasi, älä lopeta ALESSEN (levonorgestreeli ja etinyyliestradioli) ottamista. Ongelma yleensä poistuu. Jos se ei häviä, ota yhteyttä terveydenhuollon tarjoajaan.
4. PILLEERIT VOIVAT MYÖS AIHEUTTAA TÄPPILLE TAI KELPAA VUOTOA, vaikka korvaisit nämä unohtaneet pillerit.
Niinä päivinä, kun otat 2 pilleriä korvataksesi unohdetut pillerit, saatat myös tuntea olosi hieman pahoinvoitavaksi.
5. JOS Oksentelet (4 tunnin kuluessa pillerin ottamisen jälkeen), sinun tulee noudattaa ohjeita, jotka ovat kohdassa MITÄ TEHDÄ, JOS SINÄ MITTAAT PILLEERIT. JOS SINULLA ON Ripuli tai JOS KÄYTÄT JOITAKIN LÄÄKKEITÄ, mukaan lukien jotkin antibiootit, pillerisi eivät ehkä toimi yhtä hyvin.
Käytä ei-hormonaalista varamenetelmää (kuten kondomia tai spermisidiä), kunnes otat yhteyttä terveydenhuollon tarjoajaan.
6. JOS SINULLA ON ONGELMIA MUISTUTTA PILLERIN OTTAMISESSA, keskustele terveydenhuollon tarjoajan kanssa siitä, kuinka voit helpottaa pillereiden ottamista tai käyttää jotakin muuta ehkäisymenetelmää.
7. JOS SINULLA ON KYSYMYKSIÄ TAI ETET EPÄVARMISTA TÄMÄN ESITTEEN TIEDOT, soita terveydenhuollon tarjoajallesi.
ENNEN KUIN ALOITAT ALESSEN OTtamisen (levonorgestreeli ja etinyyliestradioli)
1. PÄÄTTÄ MINÄ KÄYNNISSÄ HALUAT OTTA PILLERIN. On tärkeää ottaa se suunnilleen samaan aikaan joka päivä.
2. KATSO PILLEPAKKAUKSIASI.
Pilleripakkauksessa on 21 "aktiivista" vaaleanpunaista pilleriä (hormoneilla) otettavaksi 3 viikon ajan, jonka jälkeen 1 viikon muistutusvaaleanvihreät pillerit (ilman hormoneja).
3. ETSI:
1. mistä pakkauksesta aloita pillereiden käyttö ja
2. missä järjestyksessä pillerit otetaan (seuraa nuolta).
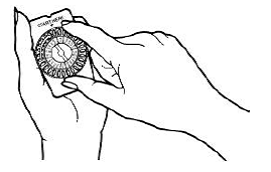
4. VARMISTA, ETTÄ OLET AINA VALMIS:
TOINEN SYNTYVYYSVÄLITYS (kuten kondomit tai siittiöiden torjunta-aineet) käytettäväksi varakeinona siltä varalta, että unohdat ottaa pillerit.
EXTRA, TÄYSI PILLIPAKETTI.
MILLOIN ALOITTAA ENSIMMÄISEN PILLERIPAKETTI
Voit valita, minä päivänä aloitat ensimmäisen pilleripakkauksen ottamisen.
Päätä terveydenhuollon tarjoajasi kanssa, mikä päivä on sinulle paras. Valitse kellonaika, joka on helppo muistaa.
PÄIVÄ 1 ALOITUS
1. Ota ensimmäinen "aktiivinen" vaaleanpunainen pilleri ensimmäisestä pakkauksesta kuukautistenne ensimmäisten 24 tunnin aikana.
2. Sinun ei tarvitse käyttää ei-hormonaalista varaehkäisymenetelmää, koska aloitat pillereiden käytön kuukautistenne alussa.
SUNNUNTAI ALOITUS
1. Ota ensimmäinen "aktiivinen" vaaleanpunainen pilleri ensimmäisestä pakkauksesta kuukautisten alkamisen jälkeisenä sunnuntaina, vaikka verenvuoto jatkuisikin. Jos kuukautisesi alkavat sunnuntaina, aloita pakkaus samana päivänä.
2. Käytä ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiöiden torjunta-ainetta) varamenetelmänä, jos harrastat seksiä milloin tahansa ensimmäisen pakkauksen aloittamisen sunnuntaista seuraavaan sunnuntaihin (7 päivää).
MITÄ TEHDÄ KUUKAUDEN AIKANA
1. Ota yksi pilleri samaan aikaan joka päivä, kunnes pakkaus on tyhjä.
Älä jätä pillereitä väliin, vaikka tiputtelut tai verenvuoto olisivat kuukautisten välillä tai vatsasi pahoinvointi (pahoinvointi).
Älä jätä pillereitä väliin, vaikka et harrastaisikaan seksiä kovin usein.
2. Kun saat pakkauksen valmiiksi:
Aloita seuraava pakkaus viimeisenä "muistutuspillerin" jälkeisenä päivänä. Älä odota päivääkään pakkausten välillä.
JOS VAIHDAT TOISESTA MERKINNÄSTÄ Yhdistelmäpillereistä
Jos edellisellä tuotemerkilläsi oli 21 pilleriä: Odota 7 päivää ennen kuin aloitat ALESSE:n (levonorgestreeli ja etinyyliestradioli) ottamisen. Sinulla on luultavasti kuukautisesi tällä viikolla. Varmista, että 21 päivän pakkauksen ja ensimmäisen vaaleanpunaisen ALESSE (levonorgestreeli ja etinyyliestradioli) pillerin ("aktiivinen" hormonipitoinen) ottamisen välillä ei kulu yli 7 päivää.
Jos edellisellä tuotemerkilläsi oli 28 pilleriä: Aloita ensimmäisen vaaleanpunaisen ALESSE (levonorgestreeli ja etinyyliestradioli) pilleri (hormonin kanssa aktiivinen) ottaminen viimeisenä muistutuspilleriä seuraavana päivänä. Älä odota päivääkään pakkausten välillä.
MITÄ TEHDÄ, JOS VÄLITÄÄN PILLEERIT
ALESSE (levonorgestreeli ja etinyyliestradioli) ei ehkä ole yhtä tehokas, jos unohdat saada vaaleanpunaisia "aktiivisia" pillereitä ja varsinkin jos unohdat muutaman ensimmäisen tai viimeiset vaaleanpunaiset "aktiiviset" pillerit pakkauksesta.
Jos sinä MISS 1 vaaleanpunainen "aktiivinen" pilleri:

1. Ota se heti kun muistat. Ota seuraava pilleri normaaliin aikaan. Tämä tarkoittaa, että voit ottaa 2 pilleriä 1 päivässä.
2. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta. Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos sinä MISS 2 vaaleanpunaiset "aktiiviset" pillerit peräkkäin VIIKKO 1 TAI VIIKKO 2 paketistasi:
1. Ota 2 pilleriä sinä päivänä, jonka muistat, ja 2 pilleriä seuraavana päivänä.
2. Ota sitten 1 pilleri päivässä, kunnes pakkaus on valmis.
3. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta. Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos sinä MISS 2 vaaleanpunaiset "aktiiviset" pillerit peräkkäin 3. VIIKKO:
1 Jos olet 1. päivän aloittaja:
HEITÄ POIS pilleripakkauksen loppuosa ja aloita uusi pakkaus samana päivänä.
Jos olet sunnuntain aloittaja:
Ota 1 pilleri joka päivä sunnuntaihin asti.
Sunnuntaina HEITÄ POIS loput pakkauksesta ja aloita uusi pilleripakkaus samana päivänä.
2. Sinulla ei ehkä ole kuukautisia tässä kuussa, mutta tämä on odotettavissa
Jos kuukautiset jäävät kuitenkin 2 kuukautta peräkkäin, soita terveydenhuollon tarjoajallesi, koska saatat olla raskaana.
3. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta. Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos sinä MISS 3 tai ENEMMÄN vaaleanpunaiset "aktiiviset" pillerit peräkkäin (ensimmäisten 3 viikon aikana):
1 Jos olet 1. päivän aloittaja:
HEITÄ POIS pilleripakkauksen loppuosa ja aloita uusi pakkaus samana päivänä.
Jos olet sunnuntain aloittaja:
Ota 1 pilleri joka päivä sunnuntaihin asti.
Sunnuntaina HEITÄ POIS loput pakkauksesta ja aloita uusi pilleripakkaus samana päivänä.
2. Sinulla ei ehkä ole kuukautisia tässä kuussa, mutta tämä on odotettavissa.
Jos kuukautiset jäävät kuitenkin 2 kuukautta peräkkäin, soita terveydenhuollon tarjoajallesi, koska saatat olla raskaana.
3. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta.
Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos unohdat jonkin seitsemästä vaaleanvihreästä "muistutuspillereistä" viikolla 4:
Heitä pois pillerit, jotka olet unohtanut.
Ota 1 pilleri joka päivä, kunnes pakkaus on tyhjä.
Et tarvitse ei-hormonaalista ehkäisymenetelmää, jos aloitat seuraavan pakkauksen ajoissa.
LOPPUUN, JOS ET OLE VIELÄ VARMA, MITÄ TEHDÄ PILLEILLE, JOITA OLET MYÖNTÄNE
Käytä EI-HORMONAALISTA SYNTYMISMENETELMIÄ aina, kun harrastat seksiä.
JATKA YKSI PILLER JOKA PÄIVÄ, kunnes tavoitat terveydenhuollon tarjoajasi.
SYNTYMÄSTÄÄNTÖ Pillereiden LOPETTAMISEN JÄLKEEN
Jos et halua tulla raskaaksi pillereiden lopettamisen jälkeen, keskustele terveydenhuollon tarjoajasi kanssa toisesta ehkäisymenetelmästä.
YKSITYISKOHTAINEN POTILASMERKINTÄ
Tämä tuote (kuten kaikki suun kautta otettavat ehkäisyvalmisteet) on tarkoitettu raskauden estämiseen. Suun kautta otettavat ehkäisyvalmisteet eivät suojaa HIV:ltä (AIDS) ja muilta sukupuolitaudeilta, kuten klamydialta, genitaaliherpekseltä, sukupuolielinten syyliltä, tippurilta, hepatiitti B:ltä ja kupalta.
JOHDANTO
Jokaisen naisen, joka harkitsee oraalisten ehkäisyvalmisteiden ("ehkäisypilleri" tai "pilleri") käyttöä, tulee ymmärtää tämän ehkäisymuodon käytön edut ja riskit. Tämä pakkausseloste antaa sinulle suuren osan tiedoista, joita tarvitset tämän päätöksen tekemiseen, ja se auttaa myös sinua määrittämään, onko sinulla riski saada jokin pillereiden vakavista sivuvaikutuksista. Siinä kerrotaan, kuinka pilleriä käytetään oikein, jotta se olisi mahdollisimman tehokas. Tämä esite ei kuitenkaan korvaa huolellista keskustelua sinun ja terveydenhuollon tarjoajasi välillä. Sinun tulee keskustella tässä pakkausselosteessa annetuista tiedoista hänen kanssaan sekä kun aloitat pillereiden käytön ensimmäisen kerran että uusintakäyntien aikana. Sinun tulee myös noudattaa terveydenhuollon tarjoajasi neuvoja säännöllisissä tarkastuksissa, kun käytät pillereitä.
ORAALISTEN EHKÄISYAINEIDEN TEHOKKUUS
Suun kautta otettavia ehkäisyvalmisteita tai "ehkäisypillereitä" tai "pillereitä" käytetään raskauden ehkäisyyn, ja ne ovat tehokkaampia kuin useimmat muut ei-kirurgiset ehkäisymenetelmät. Kun ne otetaan oikein ilman pillereiden puuttumista, raskaaksi tulemisen mahdollisuus on noin 1 % vuodessa (1 raskaus 100 naista kohti käyttövuotta kohti). Tyypilliset epäonnistumisluvut ovat noin 5 % vuodessa (5 raskautta 100 naista kohden käyttövuotta kohden), kun mukaan luetaan naiset, jotka jäävät ottamatta pillereitä. Mahdollisuus tulla raskaaksi kasvaa jokaisella unohdetulla pillerillä jokaisen 28 päivän käyttöjakson aikana.
Vertailun vuoksi muiden ehkäisymenetelmien keskimääräiset epäonnistumisluvut ensimmäisen käyttövuoden aikana ovat seuraavat:
KENEN EI PIDÄ OTTAA ORAALISIA EHKÄISYVÄLINEITÄ
Tupakointi lisää vakavien haitallisten vaikutusten riskiä sydämeen ja verisuoniin suun kautta otettavien ehkäisyvalmisteiden käytöstä. Tämä riski kasvaa iän ja tupakoinnin lisääntyessä (vähintään 15 savuketta päivässä on liitetty merkittävästi lisääntyneeseen riskiin) ja se on varsin huomattava yli 35-vuotiailla naisilla. Naiset, jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, eivät saa tupakoida.
Jotkut naiset eivät saa käyttää pilleriä. Älä esimerkiksi ota pilleriä, jos sinulla on jokin seuraavista tiloista:
- Sydänkohtauksen tai aivohalvauksen historia.
- Veritulppa jaloissa (tromboflebiitti), keuhkoissa (keuhkoembolia) tai silmissä.
- Aiempi veritulppa jalkojen syvissä laskimoissa.
- Rintakipu (angina pectoris).
- Tunnettu tai epäilty rintasyöpä tai kohdun, kohdunkaulan tai emättimen limakalvosyöpä tai tietyt hormonaalisesti herkät syövät.
- Selittämätön verenvuoto emättimestä (kunnes terveydenhuollon tarjoaja on saanut diagnoosin).
- Maksakasvain (hyvänlaatuinen tai syöpä) tai aktiivinen maksasairaus.
- Silmänvalkuaisten tai ihon keltaisuus (keltaisuus) raskauden tai pillereiden aikaisemman käytön aikana.
- Tunnettu tai epäilty raskaus.
- Leikkauksen tarve pitkittyneellä vuodetuella.
- Sydänläppä- tai sydämen rytmihäiriöt, jotka voivat liittyä verihyytymien muodostumiseen.
- Diabetes vaikuttaa verenkiertoosi.
- Päänsärkyä ja neurologisia oireita.
- Hallitsematon korkea verenpaine.
- Allergia tai yliherkkyys jollekin ALESSE:n aineosalle (levonorgestreeli ja etinyyliestradiolitabletit).
Kerro terveydenhuollon tarjoajallesi, jos sinulla on ollut jokin näistä tiloista. Terveydenhuollon tarjoaja voi suositella toista ehkäisymenetelmää.
MUUT NÄKÖKOHDAT ENNEN ORAALISTEN EHKÄISYAINEIDEN OTTOA
Kerro terveydenhuollon tarjoajallesi, jos sinulla tai jollain perheenjäsenelläsi on koskaan ollut:
- Rintojen kyhmyt, rintojen fibrokystinen sairaus, epänormaali rintojen röntgenkuva tai mammografia.
- Diabetes.
- Kohonnut kolesteroli tai triglyseridit.
- Korkea verenpaine.
- Taipumus muodostaa verihyytymiä.
- Migreeni tai muu päänsärky tai epilepsia.
- Masennus.
- Sappirakon, maksan, sydämen tai munuaisten sairaus.
- Aiemmat niukat tai epäsäännölliset kuukautiset.
Naisten, joilla on jokin näistä sairauksista, tulee usein tarkastaa terveydenhuollon tarjoaja, jos he päättävät käyttää suun kautta otettavia ehkäisyvalmisteita. Muista myös ilmoittaa terveydenhuollon tarjoajallesi, jos tupakoit tai käytät lääkkeitä.
Vaikka sydän- ja verisuonitautien riskit voivat lisääntyä suun kautta otettavien ehkäisyvalmisteiden käyttö terveillä, tupakoimattomilla yli 40-vuotiailla naisilla (jopa uudemmilla pieniannoksisilla formulaatioilla), iäkkäillä naisilla on myös suurempia mahdollisia raskauteen liittyviä terveysriskejä.
ORAALISTEN EHKÄISYAINEIDEN OTTAMISEN RISKIT
1. Veritulppien muodostumisriskit
Veritulpat ja verisuonten tukkeutuminen ovat oraalisten ehkäisyvalmisteiden käytön vakavimpia sivuvaikutuksia ja voivat aiheuttaa kuoleman tai vakavan vamman. Erityisesti jaloissa oleva hyytymä voi aiheuttaa tromboflebiitin ja keuhkoihin kulkeutunut hyytymä voi aiheuttaa äkillisen tukkeuman verta keuhkoihin kuljettavan suonen. Harvoin silmän verisuonissa esiintyy hyytymiä, jotka voivat aiheuttaa sokeutta, kaksoisnäön tai näön heikkenemistä.
Yhdistelmäehkäisytablettien käyttäjillä on suurempi riski saada veritulppia kuin ei-käyttäjillä. Tämä riski on suurin suun kautta otettavan yhdistelmäehkäisyvalmisteen ensimmäisen vuoden aikana.
Jos käytät ehkäisytabletteja ja tarvitset valinnaista leikkausta, joudut olemaan sängyssä pitkäaikaisen sairauden tai vamman vuoksi tai olet äskettäin synnyttänyt lapsen, sinulla voi olla veritulppien riski. Sinun tulee neuvotella terveydenhuollon tarjoajasi kanssa ehkäisytablettien lopettamisesta 3–4 viikkoa ennen leikkausta ja ehkäisytablettien käyttämättä jättämisestä kahteen viikkoon leikkauksen jälkeen tai vuodelevon aikana. Sinun ei myöskään pidä ottaa ehkäisyvalmisteita pian synnytyksen jälkeen tai raskauden puolivälin jälkeen. On suositeltavaa odottaa vähintään neljä viikkoa synnytyksen jälkeen, jos et imetä. Jos imetät, sinun tulee odottaa, kunnes olet vieroittanut lapsesi ennen pillereiden käyttöä. (Katso myös kohta Imetyksen aikana YLEISET VAROTOIMET .)
Veritulppien riski on suurempi oraalisten yhdistelmäehkäisyvalmisteiden käyttäjillä verrattuna ei-käyttäjiin. Tämä riski voi olla suurempi käyttäjillä suuriannoksisia pillereitä (ne, jotka sisältävät vähintään 50 mikrogrammaa estrogeenia), ja se voi olla suurempi myös pidemmällä käytöllä. Lisäksi osa näistä lisääntyneistä riskeistä voi jatkua useita vuosia oraalisten yhdistelmäehkäisyvalmisteiden käytön lopettamisen jälkeen. Epänormaalin veren hyytymisen riski kasvaa iän myötä sekä suun kautta otettavien yhdistelmäehkäisyvalmisteiden käyttäjillä että ei-käyttäjillä, mutta oraalisten ehkäisyvalmisteiden aiheuttama lisääntynyt riski näyttää olevan läsnä kaikissa ikäryhmissä.
Veritulppien liiallinen riski on suurin ensimmäisen vuoden aikana, jona nainen käyttää yhdistelmäehkäisyä. Tämä lisääntynyt riski on pienempi kuin raskauteen liittyvät verihyytymät. Suun kautta otettavien yhdistelmäehkäisyvalmisteiden käyttö lisää myös muiden hyytymishäiriöiden, mukaan lukien sydänkohtauksen ja aivohalvauksen, riskiä. Veritulpat suonissa aiheuttavat kuoleman 1–2 prosentissa tapauksista. Hyytymisriski lisääntyy entisestään naisilla, joilla on muita sairauksia. Esimerkkejä ovat: tupakointi, korkea verenpaine, epänormaalit lipiditasot, tietyt perinnölliset tai hankitut hyytymishäiriöt, liikalihavuus, leikkaus tai vamma, äskettäinen synnytys tai toisen raskauskolmanneksen abortti, pitkittynyt passiivisuus tai vuodepaikka. Suun kautta otettavat yhdistelmäehkäisyvalmisteet tulee mahdollisuuksien mukaan lopettaa ennen leikkausta ja pitkittyneen passiivisuuden tai nukkumaanmenon aikana.
Tupakointi lisää vakavien sydän- ja verisuonitapahtumien riskiä. Tämä riski kasvaa iän ja tupakoinnin myötä, ja se on melko voimakas yli 35-vuotiailla naisilla. Naisia, jotka käyttävät yhdistelmäehkäisytabletteja, tulee ehdottomasti neuvoa olemaan tupakoimatta. Jos tupakoit, keskustele terveydenhuollon ammattilaisen kanssa ennen kuin käytät yhdistelmäehkäisyvalmisteita.
2. Sydänkohtaukset ja aivohalvaukset
Suun kautta otettavat ehkäisyvalmisteet voivat lisätä taipumusta aivohalvauksiin tai ohimeneviin iskeemisiin kohtauksiin (aivojen verisuonten tukkeutuminen tai repeämä) sekä angina pectorikseen ja sydänkohtauksiin (sydämen verisuonten tukkeutuminen). Mikä tahansa näistä tiloista voi aiheuttaa kuoleman tai vakavan vamman.
Tupakointi lisää suuresti sydänkohtausten ja aivohalvausten riskiä. Lisäksi tupakointi ja suun kautta otettavien ehkäisyvalmisteiden käyttö lisäävät suuresti sydänsairauksien kehittymisen ja kuoleman mahdollisuuksia.
Naisilla, joilla on migreeni (erityisesti migreeni/päänsärky, johon liittyy neurologisia oireita) ja jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, saattaa myös olla suurempi aivohalvauksen riski, eivätkä he saa käyttää yhdistelmäehkäisyvalmisteita (katso kohta KENEN EI PIDÄ OTTAA ORAALISIA EHKÄISYVÄLINEITÄ ).
3. Sappirakon sairaus
Ehkäisytablettien käyttäjillä on luultavasti suurempi riski saada sappirakon sairaus kuin ei-käyttäjillä, vaikka tämä riski saattaa liittyä pillereihin, jotka sisältävät suuria annoksia estrogeenia. Suun kautta otettavat ehkäisyvalmisteet voivat pahentaa olemassa olevaa sappirakon sairautta tai kiihdyttää sappirakon sairauden kehittymistä naisilla, joilla ei ole aiemmin ollut oireita.
4. Maksakasvaimet
Harvinaisissa tapauksissa suun kautta otettavat ehkäisyvalmisteet voivat aiheuttaa hyvänlaatuisia mutta vaarallisia maksakasvaimia. Nämä hyvänlaatuiset maksakasvaimet voivat repeytyä ja aiheuttaa kuolemaan johtavan sisäisen verenvuodon. Lisäksi mahdollinen mutta ei varma yhteys pillereiden ja maksasyöpien kanssa on löydetty kahdessa tutkimuksessa, joissa muutamat naiset, joille kehittyi nämä erittäin harvinaiset syövät, todettiin käyttäneen suun kautta otettavia ehkäisyvalmisteita pitkiä aikoja. Maksasyövät ovat kuitenkin erittäin harvinaisia. Mahdollisuus sairastua maksasyöpään pillereiden käytöstä on siis vielä harvinaisempi.
5. Sukuelinten ja rintojen syöpä
Useat tutkimukset antavat ristiriitaisia raportteja rintasyövän ja ehkäisyvälineiden välisestä suhteesta.
Suun kautta otettavien ehkäisyvalmisteiden käyttö saattaa hieman lisätä todennäköisyyttäsi saada rintasyöpä, varsinkin jos aloitit hormonaalisen ehkäisyn käytön nuorempana.
Kun lopetat hormonaalisten ehkäisyvalmisteiden käytön, rintasyövän todennäköisyys alkaa laskea ja häviää 10 vuoden kuluttua pillereiden käytön lopettamisesta. Ei tiedetä, johtuuko tämä hieman lisääntynyt rintasyöpädiagnoosin riski pilleristä. Saattaa olla, että pilleriä käyttäviä naisia tutkittiin useammin, jolloin rintasyöpä todettiin todennäköisemmin.
Sinun tulee käydä rintojen tarkastuksessa säännöllisesti terveydenhuollon ammattilaisella ja tarkistaa omat rinnasi kuukausittain. Kerro terveydenhuollon tarjoajallesi, jos sinulla on suvussa rintasyöpää tai jos sinulla on ollut rintojen kyhmyjä tai epänormaali mammografia. Naisten, joilla on tai on ollut rintasyöpä, ei tule käyttää ehkäisyvalmisteita, koska rintasyöpä on yleensä hormoniherkkä kasvain.
Joissakin tutkimuksissa on havaittu lisääntyneen kohdunkaulan syövän ilmaantuvuus naisilla, jotka käyttävät ehkäisyvalmisteita. Tämä havainto voi kuitenkin liittyä muihin tekijöihin kuin suun kautta otettavien ehkäisyvalmisteiden käyttöön.
6. Lipidiaineenvaihdunta ja haimatulehdus
Oraalisten yhdistelmäehkäisyvalmisteiden käyttäjillä on raportoitu veren kolesteroli- ja triglyseridien nousua. Triglyseridien nousu on joissakin tapauksissa johtanut haimatulehdukseen (haimatulehdus).
ARVIOITU KUOLEMARISKI SYNTYVYYSMENETELMÄSTÄ TAI RASKAUDESTA
Kaikki ehkäisymenetelmät ja raskaus liittyvät riskiin sairastua tiettyihin sairauksiin, jotka voivat johtaa vammaisuuteen tai kuolemaan. Arvio erilaisiin ehkäisymenetelmiin ja raskauteen liittyvistä kuolemantapauksista on laskettu, ja se on esitetty seuraavassa taulukossa.
HEDELMÄLLYYDEN HALLINTAAN LIITTYVIEN SYNTYMÄN TAI MENETELMIIN LIITTYVIEN KULEMIEN VUOSImäärä 100 000 EI STERIILIÄ NAISTA kohden hedelmöitysmenetelmällä JA IKÄN MUKAAN
Yllä olevassa taulukossa minkä tahansa ehkäisymenetelmän aiheuttama kuolemanriski on pienempi kuin synnytysriski, lukuun ottamatta yli 35-vuotiaita tupakoivia ehkäisyn käyttäjiä ja yli 40-vuotiaita pillereiden käyttäjiä, vaikka he eivät tupakoi. . Taulukosta näkyy, että 15–39-vuotiailla naisilla kuolinriski oli suurin raskauden aikana (7–26 kuolemaa 100 000 naista kohden iästä riippuen). Tupakoimattomilla pillereiden käyttäjillä kuolinriski oli aina pienempi kuin raskauteen liittyvä missä tahansa ikäryhmässä, paitsi yli 40-vuotiailla naisilla, jolloin riski nousee 32 kuolemaan 100 000 naista kohti verrattuna 28:aan. raskauden kanssa tuossa iässä. Kuitenkin tupakoivien ja yli 35-vuotiaiden pillereiden käyttäjien kuolemien arvioitu määrä on suurempi kuin muilla ehkäisymenetelmillä. Jos nainen on yli 40-vuotias ja tupakoi, hänen arvioitu kuolemanriskinsä on neljä kertaa suurempi (117/100 000 naista) kuin arvioitu raskauteen liittyvä riski (28/100 000 naista) kyseisessä ikäryhmässä.
Ehdotus, että yli 40-vuotiaat naiset, jotka eivät tupakoi, eivät saisi käyttää ehkäisyvalmisteita, perustuu vanhemmista suuriannoksisista pillereistä saatuihin tietoihin. FDA:n neuvoa-antava komitea keskusteli tästä aiheesta vuonna 1989 ja suositteli, että terveiden, tupakoimattomien yli 40-vuotiaiden naisten suun kautta otettavien ehkäisyvalmisteiden käytön edut voivat olla suurempia kuin mahdolliset riskit. Ikääntyneiden naisten, kuten kaikkien naisten, jotka käyttävät suun kautta otettavia ehkäisyvalmisteita, tulee ottaa ehkäisyväline, joka sisältää vähiten estrogeenia ja progestiinia, mikä sopii potilaan yksilöllisiin tarpeisiin.
VAROITUSMERKIT
Jos jokin näistä haittavaikutuksista ilmenee, kun käytät ehkäisyvalmisteita, soita välittömästi terveydenhuollon tarjoajallesi:
- Terävä rintakipu, veren yskiminen tai äkillinen hengenahdistus (osoitus mahdollisesta hyytymisestä keuhkoissa).
- Kipu pohkeessa (osoittaa mahdollista hyytymistä jalassa).
- Puristava rintakipu tai raskaus rinnassa (osoitus mahdollisesta sydänkohtauksesta).
- Äkillinen voimakas päänsärky tai oksentelu, huimaus tai pyörtyminen, näkö- tai puhehäiriöt, heikkous tai tunnottomuus käsivarressa tai jalassa (osoitus mahdollisesta aivohalvauksesta).
- Äkillinen osittainen tai täydellinen näön menetys (osoittaa mahdollista hyytymistä silmässä).
- Rintojen kyhmyt (osoitus mahdollisesta rintasyövästä tai rintojen fibrokystisesta sairaudesta; pyydä terveydenhuollon tarjoajaa näyttämään sinulle, kuinka rintasi tutkitaan).
- Vakava kipu tai arkuus vatsan alueella (osoittaa mahdollisesti repeytyneestä maksakasvaimesta).
- Nukkumisvaikeudet, heikkous, energian puute, väsymys tai mielialan muutos (mahdollisesti osoitus vakavasta masennuksesta).
- Keltaisuus tai ihon tai silmämunien keltaisuus, johon liittyy usein kuumetta, väsymystä, ruokahaluttomuutta, tummaa virtsaa tai vaaleaa suolen liikkeitä (osoittaa mahdollisista maksaongelmista).
ORAALISTEN EHKÄISYAINEIDEN HAITTAVAIKUTUKSET
1. Suunnittelematon tai läpimurto emättimen verenvuoto tai tiputtelu
Suunnittelematonta emättimen verenvuotoa tai tiputtelua saattaa esiintyä pillereiden käytön aikana. Suunnittelematon verenvuoto voi vaihdella lievästä värjäytymisestä kuukautisten välillä läpimurtoverenvuotoon, joka on säännöllisten kuukautisten kaltaista vuotoa. Suunnittelematonta verenvuotoa esiintyy useimmiten suun kautta otettavien ehkäisyvalmisteiden ensimmäisten kuukausien aikana, mutta sitä voi esiintyä myös sen jälkeen, kun olet käyttänyt pilleriä jonkin aikaa. Tällainen verenvuoto voi olla tilapäistä, eikä se yleensä osoita vakavia ongelmia. On tärkeää jatkaa pillereiden ottamista aikataulun mukaisesti. Jos verenvuoto esiintyy useammassa kuin yhdessä syklissä tai kestää yli muutaman päivän, keskustele terveydenhuollon tarjoajan kanssa.
2. Piilolinssit
Jos käytät piilolinssejä ja huomaat näkösi muuttuvan tai et pysty käyttämään linssejäsi, ota yhteyttä terveydenhuollon tarjoajaasi.
3. Nesteenpidätys
Suun kautta otettavat ehkäisyvalmisteet voivat aiheuttaa turvotusta (nesteen kertymistä), johon liittyy sormien tai nilkkojen turvotusta, ja ne voivat nostaa verenpainetta. Jos havaitset nesteen kertymistä, ota yhteyttä terveydenhuollon tarjoajaasi.
4. Melasma
Ihon täplikäs tummuminen on mahdollista, erityisesti kasvojen.
5. Muut sivuvaikutukset
Muita sivuvaikutuksia voivat olla pahoinvointi, rintojen arkuus, ruokahalun muutos, päänsärky, hermostuneisuus, masennus, huimaus, päänahan karvojen menetys, ihottuma, emättimen infektiot, haimatulehdus ja allergiset reaktiot.
Jos jokin näistä haittavaikutuksista vaivaa sinua, soita terveydenhuollon tarjoajallesi.
YLEISET VAROTOIMET
1. Kuukautisten puuttuminen ja ehkäisyvälineiden käyttö ennen raskautta tai sen aikana
Saattaa olla aikoja, jolloin kuukautiset eivät ehkä tule säännöllisin väliajoin, kun olet lopettanut pillerisyklin. Jos olet ottanut pillereitäsi säännöllisesti ja yksi kuukautiset jäävät väliin, jatka pillereiden ottamista seuraavan syklin ajan, mutta muista ilmoittaa asiasta terveydenhuollon tarjoajallesi ennen kuin teet niin. Jos et ole ottanut pillereitä päivittäin ohjeiden mukaisesti ja kuukautiset jäivät väliin tai jos sinulla on jäänyt kaksi peräkkäistä kuukautisia, saatat olla raskaana. Tarkista välittömästi terveydenhuollon tarjoajalta, oletko raskaana. Lopeta ehkäisytablettien käyttö, jos olet raskaana.
Ei ole olemassa vakuuttavaa näyttöä siitä, että suun kautta otettavien ehkäisyvalmisteiden käyttö liittyisi synnynnäisten epämuodostumien lisääntymiseen, jos niitä otetaan vahingossa raskauden alkuvaiheessa. Aiemmin muutamat tutkimukset olivat raportoineet, että suun kautta otettavat ehkäisyvalmisteet voivat liittyä synnynnäisiin epämuodostumisiin, mutta näitä tutkimuksia ei ole vahvistettu. Suun kautta otettavia ehkäisyvalmisteita ei kuitenkaan tule käyttää raskauden aikana. Sinun tulee tarkistaa terveydenhuollon tarjoajasi riskeistä, joita raskauden aikana otetut lääkkeet aiheuttavat sikiölle.
2. Imetyksen aikana
Jos imetät, keskustele terveydenhuollon tarjoajasi kanssa ennen kuin aloitat ehkäisytablettien käytön. Osa lääkkeestä siirtyy lapselle maidon mukana. Muutamia lapseen kohdistuvia haittavaikutuksia on raportoitu, mukaan lukien ihon kellastuminen (keltatauti) ja rintojen suureneminen. Lisäksi suun kautta otettavat ehkäisyvalmisteet voivat heikentää maidon määrää ja laatua. Jos mahdollista, älä käytä ehkäisyvalmisteita imetyksen aikana. Sinun tulee käyttää toista ehkäisymenetelmää, koska imetys antaa vain osittaisen suojan raskaaksi tulemiselta ja tämä osittainen suoja heikkenee merkittävästi, kun imetät pidempiä aikoja. Sinun tulee harkita suun kautta otettavien ehkäisyvalmisteiden aloittamista vasta, kun olet vieroittanut lapsesi kokonaan.
3. Laboratoriotutkimukset
Jos sinulle on määrä tehdä laboratoriotutkimuksia, kerro lääkärillesi, että käytät ehkäisypillereitä. Ehkäisypillerit voivat vaikuttaa tiettyihin verikokeisiin.
4. Lääkkeiden yhteisvaikutukset
Tietyt lääkkeet voivat olla vuorovaikutuksessa ehkäisypillereiden kanssa tehdäkseen niistä vähemmän tehokkaita raskauden ehkäisyssä tai lisätäkseen läpimurtoverenvuotoa. Tällaisia lääkkeitä ovat rifampiini, epilepsialääkkeet, kuten barbituraatit (esimerkiksi fenobarbitaali) ja fenytoiini (Dilantin® on yksi tämän lääkkeen merkki), primidoni (Mysoline®), topiramaatti (Topamax®), karbamatsepiini (Tegretol® on yksi tuotemerkki tämän lääkkeen), fenyylibutatsoni (Butazolidin® on yksi tuotemerkki), jotkin HIV- tai AIDS-lääkkeet, kuten ritonaviiri (Norvir®), modafiniili (Provigil®) ja mahdollisesti tietyt antibiootit (kuten ampisilliini ja muut penisilliinit ja tetrasykliinit), ja mäkikuismaa (Hypericum perforatum) sisältävät kasviperäiset tuotteet. Saatat myös joutua käyttämään ei-hormonaalista ehkäisymenetelmää minkä tahansa syklin aikana, kun käytät lääkkeitä, jotka voivat heikentää oraalisten ehkäisyvalmisteiden tehoa.
Sinulla saattaa olla suurempi riski saada tietyntyyppinen maksan toimintahäiriö, jos käytät troleandomysiiniä ja suun kautta otettavia ehkäisyvalmisteita samanaikaisesti.
Sinun tulee ilmoittaa terveydenhuollon tarjoajallesi kaikista käyttämistäsi lääkkeistä, mukaan lukien reseptivapaat tuotteet.
5. Sukupuolitaudit
Tämä tuote (kuten kaikki suun kautta otettavat ehkäisyvalmisteet) on tarkoitettu raskauden estämiseen. Se ei suojaa HIV:ltä (AIDS) ja muilta sukupuolitaudeilta, kuten klamydialta, genitaaliherpekseltä, sukupuolielinten syyliltä, tippurilta, hepatiitti B:ltä ja kupalta.
MITEN ALESSE OTETAAN (levonorgestreeli ja etinyyliestradioli)
TÄRKEÄÄ MUISTAA
ENNEN KUIN ALOITAT ALESSEN (levonorgestreeli ja etinyyliestradioli) OTtamisen:
1. MUISTA LUE NÄMÄ OHJEET:
Ennen kuin aloitat ALESSEN (levonorgestreeli ja etinyyliestradioli) käytön.
Ja
Aina kun et ole varma mitä tehdä.
2. OIKEIN TAPA OTTA PILLER ON OTTA YKSI PILLE JOKA PÄIVÄ SAMAAN AIKAAN.
Jos unohdat ottaa pillerit, voit tulla raskaaksi. Tämä sisältää paketin aloittamisen myöhässä. Mitä enemmän pillereitä unohdat, sitä todennäköisemmin tulet raskaaksi. Katso kohta "MITÄ TEHDÄ, JOS SINÄ MITTAAT PILLEERIT" alla.
3. MONEILLA NAISILLA ON TÄPPILLE TAI VÄKEVÄÄ VUOTOA TAI VOITTAA OLLA PAHOILLE vatsaan ENSIMMÄISEN 1-3 PILLERIPAKKAUKSEN AIKANA.
Jos tunnet pahoinvointia vatsassasi, älä lopeta ALESSEN (levonorgestreeli ja etinyyliestradioli) ottamista. Ongelma yleensä poistuu. Jos se ei häviä, ota yhteyttä terveydenhuollon tarjoajaan.
4. PILLEERIT VOIVAT MYÖS AIHEUTTAA TÄPPILLE TAI KELPAA VUOTOA, vaikka korvaisit nämä unohtaneet pillerit.
Niinä päivinä, kun otat 2 pilleriä korvataksesi unohdetut pillerit, saatat myös tuntea olosi hieman pahoinvoitavaksi.
5. JOS Oksentelet (4 tunnin kuluessa pillerin ottamisen jälkeen), sinun tulee noudattaa ohjeita, jotka ovat kohdassa MITÄ TEHDÄ, JOS SINÄ MITTAAT PILLEERIT. JOS SINULLA ON Ripuli tai JOS KÄYTÄT JOITAKIN LÄÄKKEITÄ, mukaan lukien jotkin antibiootit, pillerisi eivät ehkä toimi yhtä hyvin.
Käytä ei-hormonaalista varamenetelmää (kuten kondomia tai spermisidiä), kunnes otat yhteyttä terveydenhuollon tarjoajaan.
6. JOS SINULLA ON ONGELMIA MUISTUTTA PILLERIN OTTAMISESSA, keskustele terveydenhuollon tarjoajan kanssa siitä, kuinka voit helpottaa pillereiden ottamista tai käyttää jotakin muuta ehkäisymenetelmää.
7. JOS SINULLA ON KYSYMYKSIÄ TAI ETET EPÄVARMISTA TÄMÄN ESITTEEN TIEDOT, ota yhteyttä terveydenhuollon tarjoajaasi.
ENNEN KUIN ALOITAT ALESSEN OTtamisen (levonorgestreeli ja etinyyliestradioli)
1. PÄÄTTÄ MINÄ KÄYNNISSÄ HALUAT OTTA PILLERIN. On tärkeää ottaa se suunnilleen samaan aikaan joka päivä.
2. KATSO PILLEPAKKAUKSIASI.
Pilleripakkauksessa on 21 "aktiivista" vaaleanpunaista pilleriä (hormoneilla) otettavaksi 3 viikon ajan, jonka jälkeen
1 viikko muistutusvaaleanvihreitä pillereitä (ilman hormoneja).
3. ETSI:
1. mistä pakkauksesta aloita pillereiden käyttö ja
2. missä järjestyksessä pillerit otetaan (seuraa nuolta).
4. VARMISTA, ETTÄ OLET AINA VALMIS:
TOINEN SYNTYVYYSVÄLITYS (kuten kondomit tai siittiöiden torjunta-aineet) käytettäväksi varakeinona siltä varalta, että unohdat ottaa pillerit.
EXTRA, TÄYSI PILLIPAKETTI.
MILLOIN ALOITTAA ENSIMMÄISEN PILLERIPAKETTI
Voit valita, minä päivänä aloitat ensimmäisen pilleripakkauksen ottamisen.
Päätä terveydenhuollon tarjoajasi kanssa, mikä päivä on sinulle paras. Valitse kellonaika, joka on helppo muistaa.
PÄIVÄ 1 ALOITUS
1. Ota ensimmäinen "aktiivinen" vaaleanpunainen pilleri ensimmäisestä pakkauksesta kuukautistenne ensimmäisten 24 tunnin aikana.
2. Sinun ei tarvitse käyttää ei-hormonaalista varaehkäisymenetelmää, koska aloitat pillereiden käytön kuukautistenne alussa.
SUNNUNTAI ALOITUS
1. Ota ensimmäinen "aktiivinen" vaaleanpunainen pilleri ensimmäisestä pakkauksesta kuukautisten alkamisen jälkeisenä sunnuntaina, vaikka verenvuoto jatkuisikin. Jos kuukautisesi alkavat sunnuntaina, aloita pakkaus samana päivänä.
2. Käytä ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiöiden torjunta-ainetta) varamenetelmänä, jos harrastat seksiä milloin tahansa ensimmäisen pakkauksen aloittamisen sunnuntaista seuraavaan sunnuntaihin (7 päivää).
MITÄ TEHDÄ KUUKAUDEN AIKANA
1. Ota yksi pilleri samaan aikaan joka päivä, kunnes pakkaus on tyhjä.
Älä jätä pillereitä väliin, vaikka tiputtelut tai verenvuoto olisivat kuukautisten välillä tai vatsasi pahoinvointi (pahoinvointi).
Älä jätä pillereitä väliin, vaikka et harrastaisikaan seksiä kovin usein.
2. Kun saat pakkauksen valmiiksi:
Aloita seuraava pakkaus viimeisenä "muistutuspillerin" jälkeisenä päivänä. Älä odota päivääkään pakkausten välillä.
JOS VAIHDAT TOISESTA MERKINNÄSTÄ Yhdistelmäpillereistä
Jos edellisellä tuotemerkilläsi oli 21 pilleriä: Odota 7 päivää ennen kuin aloitat ALESSE:n (levonorgestreeli ja etinyyliestradioli) ottamisen. Sinulla on luultavasti kuukautisesi tällä viikolla. Varmista, että 21 päivän pakkauksen ja ensimmäisen vaaleanpunaisen ALESSE (levonorgestreeli ja etinyyliestradioli) pillerin ("aktiivinen" hormonipitoinen) ottamisen välillä ei kulu yli 7 päivää.
Jos edellisellä tuotemerkilläsi oli 28 pilleriä: Aloita ensimmäisen vaaleanpunaisen ALESSE (levonorgestreeli ja etinyyliestradioli) pilleri (hormonin kanssa aktiivinen) ottaminen viimeisenä muistutuspilleriä seuraavana päivänä. Älä odota päivääkään pakkausten välillä.
MITÄ TEHDÄ, JOS VÄLITÄÄN PILLEERIT
ALESSE (levonorgestreeli ja etinyyliestradioli) ei ehkä ole yhtä tehokas, jos unohdat saada vaaleanpunaisia "aktiivisia" pillereitä ja varsinkin jos unohdat muutaman ensimmäisen tai viimeiset vaaleanpunaiset "aktiiviset" pillerit pakkauksesta.
Jos sinä MISS 1 vaaleanpunainen "aktiivinen" pilleri:
1. Ota se heti kun muistat. Ota seuraava pilleri normaaliin aikaan. Tämä tarkoittaa, että voit ottaa 2 pilleriä 1 päivässä.
2. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta. Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos sinä MISS 2 vaaleanpunaiset "aktiiviset" pillerit peräkkäin VIIKKO 1 TAI VIIKKO 2 paketistasi:
1. Ota 2 pilleriä sinä päivänä, jonka muistat, ja 2 pilleriä seuraavana päivänä.
2. Ota sitten 1 pilleri päivässä, kunnes pakkaus on valmis.
3. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta. Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos sinä MISS 2 vaaleanpunaiset "aktiiviset" pillerit peräkkäin 3. VIIKKO:
1 Jos olet 1. päivän aloittaja:
HEITÄ POIS pilleripakkauksen loppuosa ja aloita uusi pakkaus samana päivänä.
Jos olet sunnuntain aloittaja:
Ota 1 pilleri joka päivä sunnuntaihin asti.
Sunnuntaina HEITÄ POIS loput pakkauksesta ja aloita uusi pilleripakkaus samana päivänä.
2. Sinulla ei ehkä ole kuukautisia tässä kuussa, mutta sen odotetaan olevan odotettavissa. Jos kuukautiset jäävät kuitenkin 2 kuukautta peräkkäin, soita terveydenhuollon ammattilaiselle, koska saatat olla raskaana.
3. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta. Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos sinä MISS 3 tai ENEMMÄN vaaleanpunaiset "aktiiviset" pillerit peräkkäin (ensimmäisten 3 viikon aikana):
1 Jos olet 1. päivän aloittaja:
HEITÄ POIS pilleripakkauksen loppuosa ja aloita uusi pakkaus samana päivänä.
Jos olet sunnuntain aloittaja:
Ota 1 pilleri joka päivä sunnuntaihin asti.
Sunnuntaina HEITÄ POIS loput pakkauksesta ja aloita uusi pilleripakkaus samana päivänä.
2. Sinulla ei ehkä ole kuukautisia tässä kuussa, mutta tämä on odotettavissa.
Jos kuukautiset jäävät kuitenkin 2 kuukautta peräkkäin, soita terveydenhuollon tarjoajallesi, koska saatat olla raskaana.
3. VOITTAA tulla raskaaksi, jos harrastatte seksiä 7 päivän kuluessa pillereiden uudelleen aloittamisesta.
Sinun TÄYTYY käyttää ei-hormonaalista ehkäisymenetelmää (kuten kondomia tai siittiömyrkkyä) varmuuskopiona näiden 7 päivän ajan.
Jos unohdat jonkin seitsemästä vaaleanvihreästä "muistutuspillereistä" viikolla 4:
Heitä pois pillerit, jotka olet unohtanut.
Ota 1 pilleri joka päivä, kunnes pakkaus on tyhjä.
Et tarvitse ei-hormonaalista ehkäisymenetelmää, jos aloitat seuraavan pakkauksen ajoissa.
LOPPUUN, JOS ET OLE VIELÄ VARMA, MITÄ TEHDÄ PILLEILLE, JOITA OLET MYÖNTÄNE
Käytä EI-HORMONAALISTA SYNTYMISMENETELMIÄ aina, kun harrastat seksiä.
JATKA YKSI PILLER JOKA PÄIVÄ, kunnes tavoitat terveydenhuollon tarjoajasi.
RASKAUS PILLEERIEN Epäonnistumisen vuoksi
Raskauteen johtavien pillereiden epäonnistumisen ilmaantuvuus on noin 1 tapaus vuodessa (1 raskaus 100 naista kohti käyttövuotta kohti), jos niitä otetaan joka päivä ohjeiden mukaisesti, mutta tyypillisempi epäonnistumisprosentti on noin 5 % vuodessa (5 raskautta 100 naista kohti per vuosi). käyttövuosi), mukaan lukien naiset, jotka eivät aina ota pillereitä täsmälleen ohjeiden mukaan ilman, että yksikään pilleri jää väliin. Jos sinusta tulee
raskaana, riski sikiölle on minimaalinen, mutta sinun tulee lopettaa pillereiden käyttö ja keskustella raskaudesta terveydenhuollon tarjoajan kanssa.
RASKAUS Pillereiden LOPETTAMISEN JÄLKEEN
Raskaus saattaa viivästyä, kun lopetat ehkäisytablettien käytön, varsinkin jos kuukautiskiertosi oli epäsäännöllinen ennen ehkäisyvalmisteiden käyttöä. Saattaa olla suositeltavaa lykätä hedelmöitystä, kunnes kuukautiset alkavat säännöllisesti, kun olet lopettanut pillereiden käytön ja haluat raskautta.
Vastasyntyneiden synnynnäisten epämuodostumien määrä ei näytä lisääntyvän, kun raskaus tulee pian pillereiden lopettamisen jälkeen.
SYNTYMÄSTÄÄNTÖ Pillereiden LOPETTAMISEN JÄLKEEN
Jos et halua tulla raskaaksi pillereiden lopettamisen jälkeen, sinun tulee käyttää jotakin muuta ehkäisymenetelmää heti ALESSE-hoidon lopettamisen jälkeen (levonorgestreeli ja etinyyliestradioli). Keskustele terveydenhuollon tarjoajasi kanssa toisesta ehkäisymenetelmästä.
YLIANNOSTUS
Yliannostus voi aiheuttaa pahoinvointia, oksentelua, rintojen arkuutta, huimausta, vatsakipua ja väsymystä/uneliaisuutta. Naisilla voi esiintyä vieroitusverenvuotoa. Yliannostustapauksissa ota yhteyttä terveydenhuollon tarjoajaan tai apteekkiin.
MUITA TIETOJA
Terveydenhuollon tarjoaja ottaa lääketieteellisen ja sukuhistorian ennen ehkäisytablettien määräämistä ja tutkii sinut. Fyysinen tarkastus voidaan siirtää toiseen ajankohtaan, jos pyydät sitä ja terveydenhuollon tarjoajasi katsoo, että sen lykkääminen on aiheellista. Sinun tulee käydä uudelleentarkastuksessa vähintään kerran vuodessa. Muista ilmoittaa terveydenhuollon tarjoajallesi, jos suvussasi on jokin tässä pakkausselosteessa aiemmin luetelluista sairauksista. Muista pitää kaikki tapaamiset terveydenhuollon tarjoajan kanssa, koska nyt on aika määrittää, onko oraalisten ehkäisyvalmisteiden käytön sivuvaikutuksista varhaisia merkkejä.
Älä käytä lääkettä mihinkään muuhun sairauteen kuin siihen, johon se on määrätty. Tämä lääke on määrätty erityisesti sinulle; Älä anna sitä muille, jotka haluavat ehkäisypillereitä.
ORAALISISTA EHKÄISYOHJEET TERVEYSEDUT
Raskauden ehkäisyn lisäksi suun kautta otettavien ehkäisyvalmisteiden käyttö voi tarjota tiettyjä etuja. He ovat:
Kuukautiskierto voi tulla säännöllisemmäksi.
Verenvirtaus kuukautisten aikana voi olla kevyempää ja vähemmän rautaa menetetään. Siksi raudan puutteesta johtuva anemia on vähemmän todennäköinen.
Kipua tai muita oireita kuukautisten aikana saattaa esiintyä harvemmin.
Munasarjakystat voivat ilmaantua harvemmin.
Kohdunulkoinen raskaus voi esiintyä harvemmin.
Ei-syöpää aiheuttavia kystoja tai kyhmyjä rinnoissa voi esiintyä harvemmin.
Akuuttia lantion alueen tulehdussairautta voi esiintyä harvemmin.
Suun kautta otettavien ehkäisyvalmisteiden käyttö voi tarjota jonkin verran suojaa kahden syövän muodon kehittymiseltä: munasarjasyövän ja kohdun limakalvon syövän.
Jos haluat lisätietoja ehkäisypillereistä, kysy terveydenhuollon tarjoajaltasi tai apteekista. Heillä on teknisempi esite, nimeltään Professional Labeling, jonka saatat haluta lukea.
Tämän tuotteen etiketti on saatettu päivittää. Saat nykyisen pakkausselosteen ja lisätietoja tuotteista vierailemalla osoitteessa www.wyeth.com tai soittamalla lääketieteellisen viestintäosastomme maksuttomaan numeroon 1-800-934-5556.
